一种基于分离的分段同源多糖组的多糖结构解析方法
本发明属于生物检测分析,具体涉及一种基于分离的分段同源多糖组的多糖结构解析方法。
背景技术:
1、多糖 (polysaccharide)是由十个单糖通过糖苷键连接形成,构成生物的重要的大分子物质之一,被证明具有丰富的生物活性,包括免疫活性,抗糖尿病,抗癌,抗炎等。常见多糖结构如图12所示(以香菇多糖示例)(ankaj kumar, rishi paliwal, arvindgulbake,lentinan: an unexplored novel biomaterial in drug and gene deliveryapplications, journal of controlled release, 2023, volume 356, 316-336),多糖结构决定其活性,多糖结构与活性的关系是多糖应用快速发展的指导。明确多糖结构,一是研究多糖构效关系的基础,进而为多糖的应用提供依据;二是多糖药理学以及毒理学研究的基础,对于医学多糖应用具有里程碑式的意义。但是多糖解析目前仍存在较大困难,多糖结构复杂,它由十个及以上的单糖通过糖苷键连接形成,相对分子质量从几万到几千万不等,具有丰富的分支结构,并折叠形成不同的空间结构。由于单糖类型丰富,连接位置以及连接顺序的不同使得多糖结构复杂,导致多糖的组合可能性多,结构解析十分困难(叶立斌,张劲松,潘迎捷.食药用菌多糖结构解析中的核磁共振技术[j].食用菌学报,2007(04):68-75.doi:10.16488/j.cnki.1005-9873.2007.04.012.;刘玉红,王凤山.核磁共振波谱法在多糖结构分析中的应用[j]. 食品与药品, 2007(08):39-43.)。
2、多糖结构解析的方法主要有四大类包括色谱法,质谱法,波谱法以及光谱法。波谱法中的核磁共振波谱法(nmr)是目前研究多糖结构的主流方法(杜秀菊,张劲松,潘迎捷.核磁共振技术在食用菌多糖结构分析中的作用[j].中国食用菌,2010,29(01):3-6+19.doi:10.13629/j.cnki.53-1054.2010.01.005.)。nmr能够得到较为全面的多糖结构信息,包括单糖组成,糖苷键,糖苷键连接顺序(刘玉红,王凤山.核磁共振波谱法在多糖结构分析中的应用[j].食品与药品,2007(08):39-43.)。目前常用于多糖结构解析的nmr的类型主要包括一维图谱,1h nmr谱,13c nmr谱,二维图谱包括hsqc谱、hmbc谱、cosy谱、noesy谱。一般来说,解析nmr图谱首先需要利用1h nmr谱,13c nmr谱获得简单的多糖结构信息,之后根据hsqc谱一一对应端基氢与端基碳,再利用cosy, noesy图谱从端基氢出发寻找其它位置的氢,等到氢全部归属完后,再利用hsqc谱归属所有的碳信号,最后利用hmbc、noesy验证归属的碳氢信号峰,并确认各个糖残基的连接位置和顺序。并结合单糖组成,糖苷键,分子量等信息便可解析多糖结构。
3、但是,现有技术利用nmr解析多糖结构的方法仍存在三个明显的问题:
4、(1)一次性只能解析一个多糖的结构:现有技术的方法一次性只能解析一个多糖的结构是指在一次nmr检测后得到一个多糖的各种nmr图谱,然后根据一个多糖的图谱分析这一个多糖的结构,如果要解析多个多糖的结构只能将每个多糖依次按照上述步骤分析,解析效率低,如李雪琴、张军银、曹长靓等人的研究中虽然文中有制备多个多糖,但在结构解析时均是利用一个多糖的甲基化分析、核磁共振波谱进行信号峰的归属分析,多个多糖之间的分析都是独立的、无相互比较分析;(李雪琴. 不同分子量柴胡多糖的结构解析及体外生物活性研究[d]. 山西:山西大学,2022.张军银. 多花黄精果聚糖和半乳聚糖的结构及其在益生菌中的应用[d]. 四川:成都中医药大学,2021.曹长靓. 海蒿子多糖的分离纯化、降血糖活性及其体外消化酵解研究[d]. 广东:华南理工大学,2021.)。
5、(2)弱信号峰的糖残基解析不准确甚至无法解析:由于核磁共振灵敏度低,检出限高,导致糖链中含量低的糖残基以及糖苷键等只能在核磁图谱中出弱信号峰或者不出峰。现有技术人员解析弱信号峰只能基于自身知识水平进行估计解析,或者直接舍弃该弱信号峰,因此导致弱信号峰对应的糖残基结构解析不准确甚至无法解析,进而使得多糖结构解析不完整。目前针对多糖结构的解析包括分子量,单糖组成,官能团,糖残基以及糖苷键连接方式等,主要解析多糖的主链以及含量丰富的侧链结构,但侧链结构因为含量低导致在检测图谱中表现为弱信号峰,在结构解析时解析不准确或无法解析导致多糖结构解析不完整。完整的多糖结构是指在分子量,单糖组成,官能团,糖残基以及糖苷键连接方式等解析的主链结构基础上,进一步解析多糖的侧链结构,并基于分子量,对重复单元数进行合理判断,如果只是解析了上述部分结构信息则得到的是不完整的多糖结构。例如李雪琴在利用核磁解析柴胡多糖结构时,因为部分核磁信号太弱,而未出峰,因此没有得到该部分的糖苷键连接方式(李雪琴. 不同分子量柴胡多糖的结构解析及体外生物活性研究[d]. 山西:山西大学,2022.);在dong yu-hao等人对桑葚多糖的研究中(yu-hao d, chun c, qiang h,xiong f. study on a novel spherical polysaccharide from fructus mori withgood antioxidant activity. carbohydr polym. 2021 mar 15;256:117516. ),可以看到氢谱中的信号峰5.07 ppm,4.99 ppm,4.60 ppm等和碳谱中的信号峰101.70ppm,77.51ppm等因信号太弱,而无法解析,所以被舍弃。国家标准gb/t 27417—2017中指出仪器检出限是指用仪器可靠地将目标分析物信号从背景(噪音)中识别出来时,分析物的最低浓度或量(陈雷,刘红兵,刘惠丽. 定量nmr中多种检出限评估方法的比较[j]. 波谱学杂志,2022,39(2):230-242. doi:10.11938/cjmr20212944.);王东云的研究中记载,在分析天然产物中,核磁共振仪的检出限较其它波谱分析仪器高,这对于产率较低的天然产物化合物来说无疑是一种瓶颈制约因素;同样的,刘雅琴等人的研究中记载,低灵敏度一直是(并将继续是)核磁共振生物分析应用的致命弱点,而提高核磁共振灵敏度一直是过去四十年来大多数技术发展的焦点。另外,由于多糖有结构复杂且分支结构丰富,各成分之间相互干扰导致核磁共振检出限高;(刘雅琴,余明新,何玲.核磁共振技术在药物检测中的应用进展[j].天然产物研究与开发,2022,34(11):1971-1977.doi:10.16333/j.1001-6880.2022.11.018.;王东云.核磁共振技术及应用研究进展[j].科技信息(学术研究),2008(27):353-354.);因此在检测条件的限制下,由于多糖分子量大,溶解度低,使得核磁出峰信号中,多糖中某些含量低的糖残基出峰信号弱,导致无法解析弱信号峰对应的结构,因此目前的多糖结构解析技术往往只解析了多糖中强信号部分,即多糖主链部分,而无法获得准确的多糖侧链信息。
6、(3)nmr信号峰解析困难,对解析人员的专业技术依赖性高:现有技术的多糖结构解析方法仅依赖待解析的一个多糖的所有图谱的信号峰进行结构解析,核磁图谱的信号峰量大复杂,包含诸多弱信号峰、重合峰增大了解析难度,因此对于解析人员的专业知识要求非常高,影响解析效率和解析准确性,无法广泛适用于常规技术人员的工作;具体的,尽管二维图谱已经极大的改善了一维图谱中的多糖信号峰重叠的问题,但是多糖结构复杂,仍然不可规避的存在信号峰重叠的问题,导致能够被解析的信号峰数量减少而增大解析难度、降低解析的完整性和准确性,如李雪琴的研究中记载,对柴胡多糖大分子进行核磁共振波谱分析,由于分子量大,有些信号会有重叠,导致核磁波谱法得到的糖苷键连接方式较少。(李雪琴. 不同分子量柴胡多糖的结构解析及体外生物活性研究[d]. 山西:山西大学,2022.屠鹏飞主编.(2013). 天然糖化学. 北京: 化学工业出版社.;景永帅,马云凤,李明松等.植物多糖结构解析方法研究进展[j].食品工业科技, 2022, 43(03):411-421.doi:10.13386/j.issn1002-0306.2021010181.);而且通过nmr解析多糖结构需要根据1h nmr谱、13c nmr谱、hsqc谱、hmbc谱、cosy谱、noesy谱等归属氢、碳、各个糖残基的连接位置和顺序,这些图谱的核磁信息量大且复杂,单纯依赖一个多糖的所有nmr出峰信号进行判断结构需要具备丰富的化学专业知识以及丰富的糖结构解析经验,解析难度大门槛高、解析不准确,对于解析人员的专业要求很高,普通科技工作者无法有效利用。
7、综上所述,现有技术解析多糖的方法仍存在一次性只能解析一个多糖的结构造成解析效率低、对解析人员的专业技术依赖性高的问题,尤其是针对弱信号峰对应的糖残基解析不准确或者无法解析导致多糖结构的解析是不完整的,极大的影响了多糖构效关系网的建立,限制了多糖的应用。
技术实现思路
1、针对现有技术存在的问题,本发明提供了一种基于分离的分段同源多糖组的多糖结构解析方法,首次将将现有技术中解析不准确或者舍弃的弱信号峰有效利用得到了完整的多糖结构,本发明创造性的首次分离并构建了特定的分段同源多糖组,对所述分段同源多糖组中每种多糖进行均一性分析,测定每种多糖的单糖组成、糖苷键和官能团判断每种多糖的结构相似性,利用特定的分段同源多糖组中每种多糖之间的结构相似性进行核磁解析,基于同源比较,尤其是将现有技术中解析不准确或者舍弃的弱信号峰有效利用,即利用所述分段同源多糖组中的每种多糖的强信号峰互相补充所述分段同源多糖组中的每种多糖的弱信号峰,使得多糖结构含量高的主链和含量低的侧链结构均能解析,从而达到准确、快速的一次性解析多个多糖的完整结构的目的,所述一次性解析多个多糖是指同时根据多个多糖的图谱分析多个多糖的结构,多个多糖的核磁信号进行互相比较分析,最终同时得到多个多糖的结构;基于特定的分段同源多糖组中每种多糖的结构相似性,对于弱信号峰的解析可以借助于同源多糖的强信号峰辅助比较解析,相比于现有技术单纯根据一个多糖的出峰信号依赖技术人员的专业知识判断结构,本发明的方法显著提高了弱信号峰的解析程度和解析准确性,进而显著提高了多糖的解析完整性,对于解析人员的技术要求明显降低。
2、本发明所述的强信号峰和弱信号峰是相对的概念,弱信号峰通常认为是信号强度低、出峰面积小或无法与噪声和干扰信号区分的信号峰,本发明定义所述弱信号峰是指核磁信号峰面积绝对值小于1000的信号峰,例如附图5中的b中 rh1, gh1的信号峰面积分别为291,677,均属于弱信号峰;所述强信号峰是指峰面积绝对值大于等于1000的信号峰。
3、本发明提供一种基于分离的分段同源多糖组的多糖结构解析方法,包括以下步骤:
4、(1)分离出同源多糖,绘制洗脱曲线;所述同源多糖是指绘制的同一条洗脱曲线上的所有多糖;
5、(2)从所述洗脱曲线上选出任意n种多糖,其中n为正整数且n≥2,构建分段同源多糖组;
6、(3)分别测定所述分段同源多糖组中每种多糖的纯度和分子量;
7、(4)分别对每种多糖的纯度进行均一性分析,判断分段同源多糖组的均一性;若为均一性多糖,则进行步骤(5),若不是均一性多糖,则进行步骤(2);所述均一性分析是指分析多糖的纯度,所述均一性多糖是指在渗透色谱图中具有单一高斯分布的多糖;
8、(5)多糖结构相似性判断,利用核磁解析得到完整的多糖结构:
9、(5-1):对所述分段同源多糖组中的每种多糖进行结构分析,测定其单糖组成、糖苷键和官能团;
10、(5-2):根据测得的单糖组成、糖苷键和官能团判断所述分段同源多糖组是否结构相似,若结构不相似,则进行步骤(2);若结构相似,则对所述分段同源多糖组进行核磁解析,得到所述分段同源多糖组中所有多糖的结构解析结果。所述结构相似指的是分段同源多糖组中的每种多糖之间有至少30%相同的单糖组成,糖苷键以和官能团。
11、本发明通过所述的基于分离的分段同源多糖组的多糖结构解析方法,得到了包括分子量,单糖组成,官能团,糖残基以及糖苷键连接方式等的主链结构以及多糖的侧链结构的信息的完整的多糖结构。
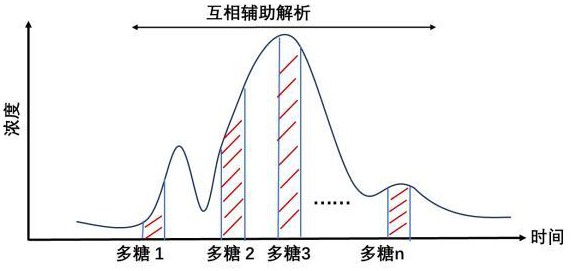
12、优选的,步骤(5)中,所述核磁解析包括将具有相似结构的同源多糖组内的多糖进行核磁分析,利用核磁信号的相似性,互相辅助解析完整的多糖结构,所述互相辅助解析的步骤如下:
13、1)根据分段同源多糖组中的每种多糖的一维图谱,包括碳谱和氢谱,相互对比分析同源多糖的相似性,所述同源多糖的相似性指的是分段同源组中的每种多糖的核磁信号谱图中有相同化学位移的出峰信号;
14、2)分别分析所述分段同源多糖组中的每种多糖核磁图谱中的强信号峰,解析强信号峰的糖残基;
15、3)根据同源多糖的相似性,利用所述分段同源多糖组中的每种多糖的强信号峰互相补充所述分段同源多糖组中的每种多糖的弱信号峰,并结合分子量,单糖组合和官能团信息,解析得到完整的多糖结构。
16、优选的,在步骤(1)分离出同源多糖之前,还包括粗多糖提取的步骤;更优选的,所述粗多糖分离提取,具体包括:采用热水提取法提取粗多糖。
17、优选的,在步骤(1)分离出同源多糖之前,还包括纯化粗多糖的步骤,所述纯化粗多糖包括去除色素和去除蛋白质的步骤,所述去除色素的物质选自丙酮、甲醇、ab-8大孔树脂或活性炭中的任意一种或多种;所述去除蛋白质采用sevag法去除蛋白质,其中sevag试剂的配制为v氯仿∶v正丁醇= 3∶1~5∶1,sevag试剂与粗多糖液体积比为3∶1~5∶1,重复操作,直至中间层无白色絮状物,取上清液冻干,采用bradford法测定纯化后的粗多糖中的蛋白质含量,根据蛋白质含量判断是否重复操作直至蛋白质含量低于5%。
18、优选的,步骤(1)中,所述分离出同源多糖的步骤为采用nacl全浓度(0-1m)或多浓度洗脱;所述多浓度是指根据实验要求,在0-1 m范围内,选取合适的nacl终浓度进行连续梯度洗脱。更优选的,所述洗脱的方法为粗多糖利用离子层析柱或进一步采用凝胶色谱柱进行洗脱分离。
19、优选的,步骤(1)中,所述绘制洗脱曲线的方法为利用苯酚硫酸法测定碳水化合物含量,从而绘制洗脱曲线。
20、优选的,步骤(2)中,所述构建分段同源多糖组可以任意选取多段洗脱曲线范围内的n种多糖,透析,冻干样品。
21、优选的,步骤(3)中,所述纯度和分子量采用凝胶渗透色谱测定;更优选的,采用凝胶渗透色谱搭配示差折光检测器测定所述分子量和纯度,流动相为0.1 m nano3。所述均一性多糖的判断方法是按照渗透色谱图出峰确定,如果所述分段同源多糖组中的每种多糖都出单一的信号峰,说明所述分段同源多糖组中的每种多糖均为均一性多糖;
22、优选的,步骤(5)中,所述单糖组成的测定方法为首先采用三氟乙酸将多糖酸解为单糖,之后用1-苯基-3-甲基-5-吡唑啉酮(pmp)对单糖进行衍生。更优选的,采用柱前衍生高效液相色谱法测定单糖组成,分析其单糖组成,比较其单糖组成;更优选的,所述高效液相色谱法的条件为:流动相乙腈(a相),0.1 m 乙酸铵溶液(b相);洗脱程序0~50 min, 19%a相,检测波长为254 nm;
23、优选的,步骤(5)中,所述糖苷键的分析采用酶解法;更优选的,所述酶解法的条件为将1~2 mg/ml的同源多糖糖液分别与α-1,5-阿拉伯聚糖内切酶,β-1,4-半乳聚糖内切酶,α-1,4-半乳聚糖内切酶混合,37~40 ℃反应16~24 h。
24、优选的,步骤(5)中,所述官能团的分析采用红外光谱法;所述红外光谱法的条件为称取适量同源多糖样品,以kbr压片,在4000~400 cm-1的范围内进行红外光谱扫描得到红外光谱图;
25、优选的,步骤(5)中,所述核磁解析的方法包括对同源多糖用d2o溶解后,冷冻干燥,再溶解于d2o中,进行核磁共振波谱(nmr)分析,所述核磁共振波谱(nmr)包括1h,13c,1h/1h cosy,1h/1h nosey,1h/13c hsqc 和1h/13c hmbc的任意一种或多种;更优选的,所述核磁共振波谱(nmr)分析中,利用丙酮(δ 30.89)作为内标,对碳谱的化学位移进行校准;
26、优选的,步骤(5)中,所述核磁解析的步骤具体包括:1)核磁共振波谱(nmr)分析所述分段同源多糖组中的每种多糖的结构信息;2)分析比较所述分段同源多糖组中的每种多糖的1h nmr图谱以及13c nmr图谱,确定所述分段同源多糖组中的每种多糖重合的信号峰,根据每种多糖之间的比较,确定重合的信号峰对应的糖残基;3)分别分析所述分段同源多糖组中的每种多糖的强信号峰,解析强信号峰的糖残基;根据同源多糖的相似性,利用所述分段同源多糖组中的每种多糖的强信号峰互相补充所述分段同源多糖组中的每种多糖的弱信号峰,解析得到完整的多糖结构;4)根据所述分段同源多糖组中的每种多糖的分子量,单糖组成,糖苷键,官能团、糖残基以及糖苷键连接顺序信息,判断多糖结构。
27、本发明的有益效果如下:
28、(1)本发明创造性的首次分离并构建了特定的分段同源多糖组,对所述分段同源多糖组中每种多糖进行均一性分析,测定每种多糖的单糖组成、糖苷键和官能团判断每种多糖的结构相似性,利用特定的分段同源多糖组中每种多糖之间的结构相似性进行核磁解析,基于同源比较,根据所述分段同源多糖组中的每种多糖的nmr图谱,互相辅助解析完整的多糖结构,使得多糖结构含量高的主链和含量低的侧链结构均能解析,从而达到准确、快速的一次性解析多个多糖的完整结构的目的,相比于现有技术的方法一次性只能解析一个多糖的结构,本发明解析效率显著提高,有望解析该洗脱曲线上所有的多糖,扩大了多糖研究者对于多糖的选择范围。
29、(2)本发明的解析方法利用特定的分段同源多糖组中每种多糖的结构相似性,基于同源比较,将现有技术中解析不准确或者舍弃的弱信号峰有效利用,即利用所述分段同源多糖组中的每种多糖的强信号峰互相补充所述分段同源多糖组中的每种多糖的弱信号峰,在多个多糖的出峰信号比对中解析弱信号峰、重合信号峰,显著提高了弱信号峰的解析程度和解析准确性,进而显著提高了多糖的解析完整性,解决了现有技术中含量低的弱信号峰对应的糖残基解析不准确或者无法解析的问题。
30、(3)本发明的解析方法基于特定的分段同源多糖组中每种多糖的结构相似性,对于弱信号峰的解析可以借助于同源多糖的强信号峰辅助比较解析,相比于现有技术单纯根据一个多糖的出峰信号依赖技术人员的专业知识判断结构,对于解析人员的技术要求明显降低。
31、(4)由于完整、准确、数量更多的同源多糖解析,对应的同源结构与其活性差异的研究更加清晰,可以更加准确的定位与单一差异结构变化的关系,进一步为多糖构效关系提供更加可靠丰富的数据资源。
- 还没有人留言评论。精彩留言会获得点赞!