一种临床试验电子数据采集系统及其测试方法与流程
1.本发明主要涉及信息技术领域,尤其涉及一种临床试验电子数据采集系统及其测试方法和计算机可读介质。
背景技术:
2.在用于满足多用户需求的临床试验电子数据采集系统中,不同的用户可存在多种不同的自定义需求。一种解决方案是根据不同的用户的需求,编写和开发具备不同特征的系统功能页面,分别满足不同的需求,但该方式的效率较低且成本高,无法应用于大规模的需求。而如果让不同的用户都可根据自身的需求将相应的功能的增加到系统中,实现不同用户编写的自定义逻辑的快速和有效测试又成为一大问题。
技术实现要素:
3.本发明要解决的技术问题是提供一种临床试验电子数据采集系统及其测试方法,既能够满足不同用户的数据采集和应用需求,同时能够对用户的自定义设计进行快速和有效的测试,减少测试成本,提供测试效率。
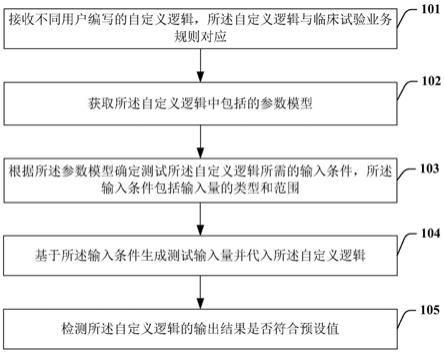
4.为解决上述技术问题,本发明提供了一种临床试验电子数据采集系统的测试方法,包括以下步骤:接收不同用户编写的自定义逻辑,所述自定义逻辑与临床试验业务规则对应;获取所述自定义逻辑中包括的参数模型;根据所述参数模型确定测试所述自定义逻辑所需的输入条件,所述输入条件包括输入量的类型和范围;基于所述输入条件生成测试输入量并代入所述自定义逻辑;检测所述自定义逻辑的输出结果是否符合预设值。
5.在本发明的一实施例中,所述参数模型包括不同类型的临床试验数据采集表单。
6.在本发明的一实施例中,所述自定义逻辑包括临床试验数据的分析与判断逻辑。
7.在本发明的一实施例中,所述业务规则包括临床试验数据采集的表单的设计规则与应用规则。
8.在本发明的一实施例中,所述输入量的类型包括数值型、符号型、布尔型和/或表单型。
9.在本发明的一实施例中,基于所述输入条件生成测试输入量通过随机数据生成工具实现。
10.在本发明的一实施例中,所述临床试验数据的分析与判断逻辑包括根据临床试验中得到的化验值、检查值、观测值和用药量发出药品不良反应事件提示、数据疑问标注和过程监测提醒。
11.在本发明的一实施例中,所述数据疑问标注包括数据的重复、缺损、遗漏和/或格式不符的标注。
12.本发明还提供一种临床试验电子数据采集系统,包括:存储器,用于存储可由处理器执行的指令;以及处理器,用于执行所述指令以实现如前所述的方法。
13.本发明还提供一种存储有计算机程序代码的计算机可读介质,所述计算机程序代
码在由处理器执行时实现如前所述的方法。
14.与现有技术相比,本发明具有以下优点:本申请的技术方案通过生成满足输入条件的测试输入量对用户编写的自定义逻辑进行测试,替代了实际临床试验流程的进行才可获得的数据,极大的降低了测试数据的获取成本,提高了测试效率,并保证测试的准确性,满足临床试验的准确与合规的要求。
附图说明
15.附图是为提供对本申请进一步的理解,它们被收录并构成本申请的一部分,附图示出了本申请的实施例,并与本说明书一起起到解释本发明原理的作用。附图中:
16.图1是本申请一实施例的临床试验电子数据采集系统的测试方法的流程图。
17.图2是本申请一实施例的临床试验电子数据采集系统的组成示意图。
具体实施方式
18.为让本发明的上述目的、特征和优点能更明显易懂,以下结合附图对本发明的具体实施方式作详细说明。
19.在下面的描述中阐述了很多具体细节以便于充分理解本发明,但是本发明还可以采用其它不同于在此描述的其它方式来实施,因此本发明不受下面公开的具体实施例的限制。
20.如本申请所示,除非上下文明确提示例外情形,“一”、“一个”、“一种”和/或“该”等词并非特指单数,也可包括复数。一般说来,术语“包括”与“包含”仅提示包括已明确标识的步骤和元素,而这些步骤和元素不构成一个排它性的罗列,方法或者设备也可能包含其他的步骤或元素。
21.本申请中使用了流程图用来说明根据本申请的实施例的系统所执行的操作。应当理解的是,前面或下面操作不一定按照顺序来精确地执行。相反,可以按照倒序或同时处理各种步骤。同时,或将其他操作添加到这些过程中,或从这些过程移除某一步或数步操作。
22.本申请的实施例描述一种临床试验电子数据采集系统及其测试方法和计算机可读介质。
23.图1是本申请一实施例的临床试验电子数据采集系统的测试方法的流程图。如图1所示,本申请的临床试验电子数据采集系统的测试方法可包括,步骤101,接收不同用户编写的自定义逻辑,所述自定义逻辑与临床试验业务规则对应。步骤102,获取所述自定义逻辑中包括的参数模型。步骤103,根据所述参数模型确定测试所述自定义逻辑所需的输入条件,所述输入条件包括输入量的类型和范围。步骤104,基于所述输入条件生成测试输入量并代入所述自定义逻辑。步骤105,检测所述自定义逻辑的输出结果是否符合预设值。
24.具体地,在步骤101,接收不同用户编写的自定义逻辑,所述自定义逻辑与临床试验业务规则对应。在一实施例中,临床试验业务规则可包括临床试验数据采集的表单的设计规则与应用规则。表单例如为临床试验过程中与受试者信息的采集、汇总等相关的表单,或是与药物发放、回收等相关的表单,也可为与化验过程相关的化验单等类型的表单,这些表单的设计与应用规则可根据不同的用户,或是不同类型的临床试验,抑或是临床试验的不同阶段而产生不同的需求。
25.在步骤102,获取所述自定义逻辑中包括的参数模型。在一实施例中,所述参数模型包括不同类型的临床试验数据采集表单。自定义逻辑还可包括临床试验数据的分析与判断逻辑。
26.在一些实施例中,临床试验数据的分析与判断逻辑可包括根据临床试验中得到的各项化验值、检查值、观测值和用药量发出药品不良反应事件提示、数据疑问标注和过程监测提醒。
27.在步骤103,根据所述参数模型确定测试所述自定义逻辑所需的输入条件,所述输入条件包括输入量的类型和范围。所述输入量的类型可包括数值型、符号型、布尔型和/或表单型,也可为根据实际需求设定的其他数据类型,例如时间段的选择、药品种类的选择等。在一实施例中,当输入量的类型为数值或符号时,此时其范围例如为数值的上下限,符号的分布范围等。当输入量的类型为表单时,其范围可为表单包括的内容项的范围。布尔型数据例如为布尔逻辑的“是”、“否”等类型的数据。
28.在步骤104,基于所述输入条件生成测试输入量并代入所述自定义逻辑。以及在步骤105,检测所述自定义逻辑的输出结果是否符合预设值。
29.基于所述输入条件生成测试输入量可通过随机数据生成工具实现。随机数据生成工具例如可为mock.js。随机数据生成也可通过随机数生成函数配合特定的基础数据产生。
30.在本申请的临床试验电子数据采集系统的设计与应用中,为满足不同用户(或称为不同租户)的自定义需求,其需要编写相应的自定义逻辑。为测试用户编写的自定义逻辑是否能够实现预期的功能或按预想的方式运行,就需要对其进行测试。但临床试验属于医学这一特殊领域,试验数据的获取并非轻而易举。很多试验数据的实际获取都与受试者相关,需要受试者的配合和多方面的操作,例如如果自定义逻辑是对某一类的血液化验单的分析与判断,则如果通过实际的试验数据对其进行测试,则需要实际进行一次血液采集,并进行血液化验操作,得到血液样本的化验值后,代入自定义逻辑,然后检测自定义逻辑是否能够输出预设的结果。这样的测试过程无疑极为耗时,成本很大。但临床试验电子数据采集系统又需要能够满足临床试验的严谨、准确与合规的要求,故其各项功能都需要经过严格的测试。
31.本申请的技术方案中,在步骤101,接收不同用户编写的自定义逻辑,在步骤102,获取所述自定义逻辑中包括的参数模型之后,在步骤103,根据所述参数模型确定测试所述自定义逻辑所需的输入条件,所述输入条件包括输入量的类型和范围。而后,在步骤104,基于所述输入条件生成测试输入量并代入所述自定义逻辑,以及在步骤105,检测所述自定义逻辑的输出结果是否符合预设值。
32.如前述,基于所述输入条件生成测试输入量可通过随机数据生成工具实现,即通过随机数据生成工具生成满足输入条件的数据。输入条件包括输入值的类型和范围。本申请的技术方案中,输入值的类型和范围实际上是基于医学领域的知识经验、试验过程与操作规范最终确定,并可根据不同用户的需求进行微调,以满足不同用户的试验需求,或是不同的检验设备、检验环境等方面的差异。
33.在一更具体的实施例中,例如用户的自定义逻辑为多表单查重。设在一特定的访视n中有m张多记录表单,每一张多记录表单记录受试者的生命体征(vital signs,vs)信息。每一张多记录表单的formoid(object id,实体id)相同。在每一张多记录表单中,包括
vsterm字段。自定义逻辑具体为检查每一张vs表单里的vsterm是否存在重复值。如果存在重复值则在所有非首次出现的重复值上发出数据质疑的提醒。该数据质疑可提示表单填写者注意表单的内容项是否被正确的填写。同一个访视内的m张vs表单分别查重且不合并重复表单。
34.此时,就需要根据该自定义逻辑中的参数模型,即采集vs信息的多记录表单(可简称为vs表单),来产生所述自定义逻辑所需的输入条件。这是的输入条件即为多张多记录表单,例如可通过随机数据生成工具生成多张表单,每一张表单可对应为json格式的数据。
35.在一实施例中,通过mock.js可设置如下的表单生成命令,
[0036][0037]
通过此命令可生成10张不同的多记录表单,每一张多记录表单中,vsterm字段可包括不同的数值。数值例如可为在上下限范围内生成。生命体征在更具体的层面例如可为血压、血样、心跳、脉搏等数据。
[0038]
通过前述的表单生成命令生成的表单数据例如可为:
[0039]
[0040][0041]
在基于输入条件生成测试输入量后,将所述测试输入量代入自定义逻辑,并获得自定义逻辑的输出结果。而后,检测所述自定义逻辑的输出结果是否符合预设值,此处例如为检测自定义逻辑运行后,其在有重复表单输入的情况下,是否发出了质疑提醒。
[0042]
本申请的技术方案中,通过前述的测试输入量的生成,替代了实际试验流程的进行才可获得的数据,极大的降低了测试数据的获取成本,提高了测试效率,并可以保证测试的准确性。
[0043]
如前述,临床试验数据的分析与判断逻辑包括根据临床试验中得到的化验值、检查值、观测值和用药量发出药品不良反应事件提示、数据疑问标注和过程监测提醒。在一实施例中,数据疑问标注包括数据的重复、缺损、遗漏和/或格式不符的标注。药品不良反应事件提示根据采集到的数据,并基于医药领域的专业知识与经验,经过分析后发出。过程监测提醒例如与临床试验的不同的试验阶段对应。
[0044]
本申请还提供一种临床试验电子数据采集系统,包括存储器,用于存储可由处理器执行的指令;以及处理器,用于执行所述指令以实现如上所述的方法。
[0045]
图2是本申请一实施例的临床试验电子数据采集系统的组成示意图。
[0046]
如图2所示,本申请的临床试验电子数据采集系统200可包括通信线路201、处理器(processor)202、只读存储器(rom)203、随机存取存储器(ram)204、以及通信端口205。临床试验电子数据采集系统还可包括服务器a 206、服务器b 208,以及相应的服务器数据存储a 207和服务器数据存储b 209。
[0047]
通信线路201可以实现临床试验电子数据采集系统200服务器端各组件间的数据通信。处理器202可以进行判断和发出提示。在一些实施例中,处理器202可以由一个或多个处理器组成。通信端口205可以实现临床试验电子数据采集系统200与外部的数据通信。临床试验电子数据采集系统200还可以包括不同形式的程序储存单元以及数据储存单元,例如硬盘,只读存储器(rom)203和随机存取存储器(ram)204,能够存储计算机处理和/或通信
使用的各种数据文件,以及处理器202所执行的可能的程序指令。处理器执行这些指令以实现方法的主要部分。处理器处理的结果通过通信端口传给用户设备,在用户界面上显示。
[0048]
上述的临床试验电子数据采集系统的测试方法可以实施为计算机程序,保存在存储器中,并可传输到处理器202中执行,以实施本申请中的临床试验电子数据采集系统的测试方法。
[0049]
临床试验电子数据采集系统的测试方法实施为计算机程序时,也可以存储在计算机可读存储介质中作为制品。例如,计算机可读存储介质可以包括但不限于磁存储设备(例如,硬盘、软盘、磁条)、光盘(例如,压缩盘(cd)、数字多功能盘(dvd))、智能卡和闪存设备(例如,电可擦除可编程只读存储器(eprom)、卡、棒、键驱动)。此外,本文描述的各种存储介质能代表用于存储信息的一个或多个设备和/或其它机器可读介质。术语“机器可读介质”可以包括但不限于能存储、包含和/或承载代码和/或指令和/或数据的无线信道和各种其它介质(和/或存储介质)。
[0050]
应该理解,上文所描述的实施例仅是示意。本文描述的实施例可在硬件、软件、固件、中间件、微码或者其任意组合中实现。对于硬件实现,处理单元可以在一个或者多个特定用途集成电路(asic)、数字信号处理器(dsp)、数字信号处理设备(dspd)、可编程逻辑器件(pld)、现场可编程门阵列(fpga)、处理器、控制器、微控制器、微处理器和/或设计为执行本文所述功能的其它电子单元或者其结合内实现。
[0051]
上文已对基本概念做了描述,显然,对于本领域技术人员来说,上述发明披露仅仅作为示例,而并不构成对本申请的限定。虽然此处并没有明确说明,本领域技术人员可能会对本申请进行各种修改、改进和修正。该类修改、改进和修正在本申请中被建议,所以该类修改、改进、修正仍属于本申请示范实施例的精神和范围。
[0052]
同时,本申请使用了特定词语来描述本申请的实施例。如“一个实施例”、“一实施例”、和/或“一些实施例”意指与本申请至少一个实施例相关的某一特征、结构或特点。因此,应强调并注意的是,本说明书中在不同位置两次或多次提及的“一实施例”或“一个实施例”或“一替代性实施例”并不一定是指同一实施例。此外,本申请的一个或多个实施例中的某些特征、结构或特点可以进行适当的组合。
[0053]
本申请的一些方面可以完全由硬件执行、可以完全由软件(包括固件、常驻软件、微码等)执行、也可以由硬件和软件组合执行。以上硬件或软件均可被称为“数据块”、“模块”、“引擎”、“单元”、“组件”或“系统”。处理器可以是一个或多个专用集成电路(asic)、数字信号处理器(dsp)、数字信号处理器件(dapd)、可编程逻辑器件(pld)、现场可编程门阵列(fpga)、处理器、控制器、微控制器、微处理器或者其组合。此外,本申请的各方面可能表现为位于一个或多个计算机可读介质中的计算机产品,该产品包括计算机可读程序编码。例如,计算机可读介质可包括,但不限于,磁性存储设备(例如,硬盘、软盘、磁带
……
)、光盘(例如,压缩盘cd、数字多功能盘dvd
……
)、智能卡以及闪存设备(例如,卡、棒、键驱动器
……
)。
[0054]
计算机可读介质可能包含一个内含有计算机程序编码的传播数据信号,例如在基带上或作为载波的一部分。该传播信号可能有多种表现形式,包括电磁形式、光形式等等、或合适的组合形式。计算机可读介质可以是除计算机可读存储介质之外的任何计算机可读介质,该介质可以通过连接至一个指令执行系统、装置或设备以实现通讯、传播或传输供使
用的程序。位于计算机可读介质上的程序编码可以通过任何合适的介质进行传播,包括无线电、电缆、光纤电缆、射频信号、或类似介质、或任何上述介质的组合。
[0055]
同理,应当注意的是,为了简化本申请披露的表述,从而帮助对一个或多个发明实施例的理解,前文对本申请实施例的描述中,有时会将多种特征归并至一个实施例、附图或对其的描述中。但是,这种披露方法并不意味着本申请对象所需要的特征比权利要求中提及的特征多。实际上,实施例的特征要少于上述披露的单个实施例的全部特征。
[0056]
上文已对基本概念做了描述,显然,对于本领域技术人员来说,上述发明披露仅仅作为示例,而并不构成对本申请的限定。虽然此处并没有明确说明,本领域技术人员可能会对本申请进行各种修改、改进和修正。该类修改、改进和修正在本申请中被建议,所以该类修改、改进、修正仍属于本申请示范实施例的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1