医学图像分割方法、电子设备和存储介质与流程
1.本发明涉及图像处理技术领域,特别涉及一种医学图像分割方法、电子设备和存储介质。
背景技术:
2.心血管疾病是全球死亡率最高的疾病,并且发病率和死亡率逐年上升,严重威胁着人类的生命健康。由于心脏的复杂结构使得心脏的不同部位具有不同的特征,从而会在医生对患者的医学图像进行心脏结构分析时,带来很大的难度。因此对心脏医学图像进行精确分割尤为重要,精确分割能为医生提供高质量的心脏结构信息,有助于医生快速诊断。
3.目前心脏的分割方法:1、依靠经验丰富的医学专家进行手动分割;2、基于传统的模型匹配的方法;3基于图像或可变模型的方法;4、基于深度学习的分割方法。
4.上述几种分割方法存在以下问题:
5.1、手动心脏分割方法的结果不仅差异化大而且需要花费大量的时间和精力。
6.2、由于心脏不同部位特征不同,基于模型匹配方法的分割精度较低。
7.3、基于可变模型的方法,需要用户交互来完成分割,鲁棒性差,且分割精度低。
8.4、基于深度学习分割方法,相对传统方法有了一定精度提高,但大多数网络模型的卷积模块都是相同的,这会限制分割精度,导致分割精度难以提高。
技术实现要素:
9.本发明的目的在于提供一种医学图像分割方法、电子设备和存储介质,不仅可以有效减少人机交互的繁琐操作,同时也可以有效提高图像分割精度。
10.为达到上述目的,本发明提供一种医学图像分割方法,包括:
11.获取待分割医学图像;
12.采用预先训练好的第一神经网络模型对所述待分割医学图像进行分割,以获取第一分割图像;
13.将所述第一分割图像与所述待分割医学图像进行逻辑与操作,以获取感兴趣区域图像;
14.采用预先训练好的第二神经网络模型对所述感兴趣区域图像进行分割,以获取组织器官蒙板图像;
15.将所述组织器官蒙板图像与所述待分割医学图像进行逻辑与操作,以获取最终的组织器官图像。
16.可选的,所述第一神经网络模型和所述第二神经网络模型均为深度全卷积网络模型。
17.可选的,所述第一神经网络模型通过以下步骤训练得到:
18.获取第一原始训练样本,所述第一原始训练样本包括第一原始医学训练图像和与所述第一原始医学训练图像对应的第一标签图像,所述第一标签图像为已标注出组织器官
的第一医学图像;
19.对所述第一原始训练样本进行扩展,得到扩展后的第一训练样本,所述扩展后的第一训练样本包括扩展后的第一医学训练图像和与所述扩展后的第一医学训练图像对应的第一标签图像;
20.设置第一神经网络模型的模型参数的初始值;以及
21.根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值对预先搭建的第一神经网络模型进行训练,直至满足第一预设训练结束条件。
22.可选的,所述根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值对预先搭建的第一神经网络模型进行训练,包括:
23.根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第一神经网络模型进行训练。
24.可选的,所述第一预设训练结束条件为扩展后的第一训练样本中的第一医学训练图像的预测结果与对应的第一标签图像的误差值收敛到第一预设误差值。
25.可选的,所述根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第一神经网络模型进行训练,包括:
26.步骤a1、将扩展后的第一医学训练图像作为第一神经网络模型的输入,根据所述第一神经网络模型的模型参数的初始值,获取所述扩展后的第一医学训练图像的预测结果;
27.步骤b1、根据所述扩展后的第一医学训练图像的预测结果和所述扩展后的第一医学训练图像对应的第一标签图像,计算第一损失函数值;以及
28.步骤c1、判断所述第一损失函数值是否收敛到第一预设误差值,如果是,训练结束,如果否,调整所述第一神经网络模型的模型参数,并将所述第一神经网络模型的模型参数的初始值更新为调整后的模型参数,返回执行所述步骤a1。
29.可选的,所述第二神经网络模型通过以下步骤训练得到:
30.获取第二原始训练样本,所述第二原始训练样本包括第二原始医学训练图像和与所述第二原始医学训练图像对应的第二标签图像,所述第二原始医学训练图像为包含感兴趣区域的感兴趣区域训练图像,所述第二标签图像为已标注出组织器官的第二医学图像;
31.对所述第二原始训练样本进行扩展,得到扩展后的第二训练样本,所述扩展后的第二训练样本包括扩展后的第二医学训练图像和与所述扩展后的第二医学训练图像对应的第二标签图像;
32.设置第二神经网络模型的模型参数的初始值;以及
33.根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值对预先搭建的第二神经网络模型进行训练,直至满足第二预设训练结束条件。
34.可选的,所述根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值对预先搭建的第二神经网络模型进行训练,包括:
35.根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第二神经网络模型进行训练。
36.可选的,所述第二预设训练结束条件为扩展后的第二训练样本中的第二医学训练图像的预测结果与对应的第二标签图像的误差值收敛到第二预设误差值。
37.可选的,所述根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第二神经网络模型进行训练,包括:
38.步骤a2、将扩展后的第二医学训练图像作为第二神经网络模型的输入,根据所述第二神经网络模型的模型参数的初始值,获取所述扩展后的第二医学训练图像的预测结果;
39.步骤b2、根据所述扩展后的第二医学训练图像的预测结果和所述扩展后的第二医学训练图像对应的第二标签图像,计算第二损失函数值;以及
40.步骤c2、判断所述第二损失函数值是否收敛到第二预设误差值,如果是,训练结束,如果否,调整所述第二神经网络模型的模型参数,并将所述第二神经网络模型的模型参数的初始值更新为调整后的模型参数,返回执行所述步骤a2。
41.可选的,所述深度全卷积网络模型包括解码网络和编码网络;
42.所述解码网络包括输入层、多个级联的第一神经网络组和第一卷积层,所述第一神经网络组包括级联的第二卷积层和最大池化层,所述第二卷积层用于对所述待分割医学图像或上一层第一神经网络组的输出图像进行组织器官特征信息的提取,所述最大池化层用于对所述第二卷积层的输出图像进行池化,所述第一卷积层用于对最深层的第一神经网络组的输出图像进行组织器官特征信息的提取;
43.所述编码网络包括多个级联的第二神经网络组、第三卷积层和输出层,所述第二神经网络组包括级联的反卷积层、合并层和第四卷积层,所述反卷积层用于对所述解码网络中的相应的最大池化层进行反向操作,以将组织器官特征信息恢复至池化前的图像中的对应位置,所述合并层用于将所述反卷积层的输出图像与所述解码网络中的相应的所述第二卷积层的输出图像进行线性相加合并,所述第四卷积层用于恢复所述解码网络中的相应的最大池化层对图像进行池化过程中丢失的组织器官特征信息,所述第三卷积层用于对最深层的第四卷积层的输出结果进行逻辑回归。
44.可选的,所述解码网络还包括多个级联的第一残差连接,所述编码网络还包括多个级联的第二残差连接。
45.为达到上述目的,本发明还提供一种电子设备,包括处理器和存储器,所述存储器上存储有计算机程序,所述计算机程序被所述处理器执行时,实现上文所述的医学图像分割方法。
46.为达到上述目的,本发明还提供一种可读存储介质,所述可读存储介质内存储有计算机程序,所述计算机程序被处理器执行时,实现上文所述的医学图像分割方法。
47.与现有技术相比,本发明提供的医学图像分割方法、电子设备和存储介质具有以下优点:本发明通过先获取待分割医学图像;再采用预先训练好的第一神经网络模型对所述待分割医学图像进行分割,以获取第一分割图像;然后再采用预先训练好的第一神经网络模型对所述待分割医学图像进行分割,以获取第一分割图像;再将所述第一分割图像与所述待分割医学图像进行逻辑与操作,以获取感兴趣区域图像;然后再采用预先训练好的第二神经网络模型对所述感兴趣区域图像进行分割,以获取组织器官蒙板图像;最后再将所述组织器官蒙板图像与所述待分割医学图像进行逻辑与操作,以获取最终的组织器官图像。可见,本发明通过采用第一神经网络模型对待分割医学图像进行初步分割,再采用第二神经网络模型在所述第一神经网络模型的分割结果的基础上进行进一步分割,不仅可以大
大提高整体的分割精度,还可以减少人机交互的繁琐操作。此外,本发明提供的医学图像分割方法,通用性强,实现了端到端的算法流程,可以更好地辅助医生提高诊断的准确性。
附图说明
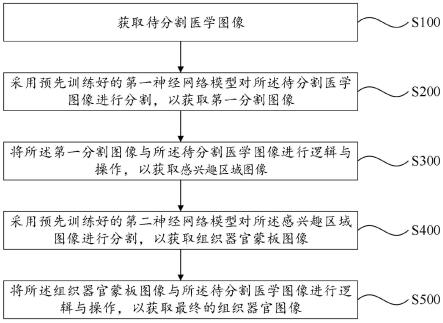
48.图1为本发明一实施方式中的医学图像分割方法的流程图;
49.图2为本发明一实施方式中的待分割医学图像的具体示例;
50.图3为本发明一实施方式中的深度全卷积网络模型的结构示意图;
51.图4为本发明一实施方式中的感兴趣区域图像的具体示例;
52.图5为本发明一实施方式中的最终分割得到的组织器官图像的具体示例;
53.图6为采用金标准分割得到的组织器官图像的具体示例;
54.图7为本发明一实施方式中的电子设备的方框结构示意图;
55.其中,附图标记如下:
56.主动脉血管-100;主动脉瓣膜-200;心室血池-300;
57.输入层-1;输出层-2;第一神经网络组-a、b、c、d;第一卷积层-e1、e2;第二卷积层-a1、a2、b1、b2、c1、c2、d1、d2;最大池化层-a3、b3、c3、d3;第二神经网络组-a、b、c、d;第三卷积层-e1;反卷积层-a1、a2、a3、a4;合并层-a2、b2、c2、d2;第四卷积层-a3、a4、b3、b4、c3、c4、d3、d4;第一残差连接-f1、f2、f3、f4;第二残差连接-f1、f2、f3、f4;
58.处理器-101;通信接口-102;存储器-103;通信总线-104。
具体实施方式
59.以下结合附图1至7和具体实施方式对本发明提出的医学图像分割方法、电子设备和存储介质作进一步详细说明。根据下面说明,本发明的优点和特征将更清楚。需要说明的是,附图采用非常简化的形式且均使用非精准的比例,仅用以方便、明晰地辅助说明本发明实施方式的目的。为了使本发明的目的、特征和优点能够更加明显易懂,请参阅附图。须知,本说明书所附图式所绘示的结构、比例、大小等,均仅用以配合说明书所揭示的内容,以供熟悉此技术的人士了解与阅读,并非用以限定本发明实施的限定条件,任何结构的修饰、比例关系的改变或大小的调整,在与本发明所能产生的功效及所能达成的目的相同或近似的情况下,均应仍落在本发明所揭示的技术内容能涵盖的范围内。
60.需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。在没有更多限制的情况下,由语句“包括一个
……”
限定的要素,并不排除在包括所述要素的过程、方法、物品或者设备中还存在另外的相同要素。
61.本发明的核心思想在于提供一种医学图像分割方法、电子设备和存储介质,不仅可以有效减少人机交互的繁琐操作,同时也可以有效提高图像分割精度。需要说明的是,虽然本发明是以从cta图像中分割出主动脉血管和主动脉瓣膜为例进行说明,但是如本领域技术人员所能理解的,本发明还可以从其它的医学图像中分割出想要分割的组织器官,本
发明对此并不进行限制。
62.需要说明的是,本发明实施方式的电子设备可以是个人计算机、移动终端等,该移动终端可以是手机、平板电脑等具有各种操作系统的硬件设备。
63.为实现上述思想,本发明提供一种医学图像分割方法,请参考图1,其示意性地给出了本发明一实施方式提供的医学图像分割方法的流程图,如图1所示,所述医学图像分割方法包括如下步骤:
64.步骤s100、获取待分割医学图像。
65.在本发明中,所述待分割医学图像可以是包括主动脉血管和主动脉瓣膜的医学图像,也可以是包括其他的组织器官的医学图像,本发明对此并不进行限制。所述待分割医学图像可以是cta(计算机断层血管造影)体数据(三维数据)图像,还可以是其它的医学图像。需要说明的是,所述待分割医学图像的大小可以根据具体情况进行设置,本发明对此并不进行限制,例如所述待分割医学图像的大小可为512
×
512
×
130像素。此外,需要说明的是,所述待分割医学图像可以通过图像获取装置进行采集,例如ct、mri等影像设备,也可以通过互联网搜集得到,还可以通过扫描设备扫描得到。
66.请参考图2,其示意性地给出了本发明一实施方式提供的待分割医学图像的具体示例。如图2所示,所述待分割医学图像为cta图像,所述cta图像中包括心室血池300、主动脉血管100和主动脉瓣膜200等区域,其中主动脉瓣膜200位于主动脉血管100和心室血池300之间,通过采用本发明提供的分割方法可以从所述cta图像中分割出主动脉血管100和主动脉瓣膜200。
67.步骤s200、采用预先训练好的第一神经网络模型对所述待分割医学图像进行分割,以获取第一分割图像。
68.由此,通过采用预先训练好的第一神经网络模型对所述待分割医学图像(例如cta图像)进行初步分割,以获取初步分割结果(例如主动脉血管和主动脉瓣膜的初步分割结果),可以有效减少人机交互的繁琐操作,提高分割精度,为后续获取准确的组织器官图像(例如主动脉血管和主动脉瓣膜图像)奠定基础。
69.为了进一步提高分割精度,在执行步骤s200之前,所述分割方法还包括:
70.对所述待分割医学图像进行预处理,以滤除所述待分割医学图像中的噪声。
71.对应的,步骤s200为:采用预先训练好的第一神经网络模型对预处理后的所述待分割医学图像进行分割。
72.由此,通过对所述待分割医学图像进行预处理,可以有效滤除所述待分割医学图像中的噪声信息,从而可以有效提高所述待分割医学图像的图像质量,为后续获取准确的组织器官图像进一步奠定基础。具体地,可采用高斯滤波器滤除所述待分割医学图像中的噪声信息,此外,还可以采用其他常用的滤波器对所述待分割医学图像进行预处理,本发明对此并不进行限制。
73.优选地,所述第一神经网络模型为深度全卷积网络模型,所述第一神经网络模型包括解码网络和编码网络。所述解码网络包括输入层、多个级联的第一神经网络组和第一卷积层,所述第一神经网络组包括级联的第二卷积层和最大池化层;所述第二卷积层用于对所述待分割医学图像或上一层第一神经网络组的输出图像进行组织器官特征信息的提取,所述最大池化层用于对所述第二卷积层的输出图像进行池化,所述第一卷积层用于对
最深层的第一神经网络组的输出图像进行组织器官特征信息的提取。
74.所述编码网络包括多个级联的第二神经网络组、第三卷积层和输出层,所述第二神经网络组包括级联的反卷积层、合并层和第四卷积层;所述反卷积层用于对所述解码网络中的相应的最大池化层进行反向操作,以将组织器官特征信息恢复至池化前的图像中的对应位置,所述合并层用于将所述反卷积层的输出图像与所述解码网络中的相应的所述第二卷积层的输出图像进行线性相加合并,所述第四卷积层用于恢复所述解码网络中的相应的最大池化层对图像进行池化过程中丢失的组织器官特征信息,所述第三卷积层用于对最深层的第四卷积层的输出结果进行逻辑回归。
75.由此,本发明通过采用深度全卷积网络模型作为第一神经网络模型,可以对所述待分割医学图像的初步分割结果逐步优化,以实现分割精度的逐步提高。
76.为了清楚地理解本实施方式提供的第一神经网络模型的结构,请参考图3,作为示例,其示意性地给出了本发明一实施方式提供的深度全卷积网络模型的结构示意图。如图3所示,所述解码网络包括4个级联的第一神经网络组a、b、c和d,所述编码网络包括4个级联的第二神经网络组a、b、c和d。其中,在第一神经网络组d和第二神经网络组a之间设有第一卷积层e1和e2。
77.如图3所示,第一神经网络组a包括级联的第二卷积层a1、a2和最大池化层a3;第一神经网络组b包括级联的第二卷积层b1、b2和最大池化层b3;第一神经网络组c包括级联的第二卷积层c1、c2和最大池化层c3;第一神经网络组d包括级联的第二卷积层d1、d2和最大池化层d3。其中,第一神经网络组a用于对输入的待分割医学图像进行组织器官特征信息的提取,例如主动脉瓣膜和主动脉血管的纹理特征、几何形状特征、位置特征的提取。具体地,第二卷积层a1和a2用于对待分割医学图像进行卷积处理,以对所述待分割医学图像进行组织器官特征信息的提取,最大池化层a3用于对经过卷积处理后的图像进行池化操作。
78.第一神经网络组b用于对由最大池化层a3池化后的图像进行组织器官特征信息的提取,例如主动脉瓣膜和主动脉血管的纹理特征、几何形状特征、位置特征的提取,该具体过程与第一神经网络组a中的具体过程类似,在此不再赘述。
79.第一神经网络组c用于对由最大池化层b3池化后的图像进行组织器官特征信息的提取,例如主动脉瓣膜和主动脉血管的纹理特征、几何形状特征、位置特征等信息的提取,该具体过程与第一神经网络组a中的具体过程类似,在此不再赘述。
80.第一神经网络组d用于对由最大池化层c3池化后的图像进行组织器官特征信息的提取,例如主动脉瓣膜和主动脉血管的纹理特征、几何形状特征、位置特征等信息的提取,该具体过程与第一神经网络组a中的具体过程类似,在此不再赘述。
81.第一卷积层e1用于对由最大池化层d3池化后的图像进行卷积,以进行组织器官特征信息的提取,第一卷积层e2用于对由第一卷积层e1卷积后的图像继续进行卷积,以进一步进行组织器官特征信息的提取。
82.第二神经网络组a包括级联的反卷积层a1、合并层a2、第四卷积层a3和a4;第二神经网络组b包括级联的反卷积层b1、合并层b2、第四卷积层b3和b4;第二神经网络组c包括级联的反卷积层c1、合并层c2、第四卷积层c3和c4;第二神经网络组d包括级联的反卷积层d1、合并层d2、第四卷积层d3和d4。第二神经网络组d的第四卷积层d4和输出层2之间设置有第三卷积层e1,该第三卷积层e1用于实现图像的逻辑回归,其不属于第二神经网络组。
83.在本实施方式中,第二神经网络组a用于将组织器官特征信息,例如主动脉瓣膜和主动脉血管的纹理特征、几何形状特征、位置特征等恢复至最大池化层d3池化前的图像的对应的位置中。具体地,反卷积层a1用于对最大池化层d3进行反向操作,以将组织器官特征信息恢复至最大池化层d3池化前的图像中的对应位置。合并层a2用于将第一卷积层d2的输出与反卷积层a1的输出进行线性相加合并后作为第四卷积层a3的输入。第四卷积层a3和a4用于恢复图像在最大池化层d3对图像进行池化过程中丢失的组织器官特征信息,例如主动脉瓣膜和主动脉血管的纹理特征、几何形状特征、位置特征等。
84.与第二神经网络组a类似,第二神经网络组b至d也用于恢复图像的组织器官特征信息,最终由第二神经网络组d中的第四卷积层d4输出最终恢复出的图像中的所有组织器官特征信息,例如主动脉瓣膜和主动脉血管的纹理特征、几何形状特征、位置特征,最后经由第三卷积层e1的逻辑回归,从而得到初步图像分割结果,例如主动脉血管和主动脉瓣膜图像的初步分割结果。
85.优选地,如图3所示,所述解码网络还包括多个级联的第一残差连接,所述编码网络还包括多个级联的第二残差连接。由此,通过在所述解码网络中设置多个级联的第一残差连接,在所述编码网络中设置多个级联的第二残差连接,有效缓解了随着网络层数越深,越容易出现梯度消失和梯度爆炸的问题,保证了有效特征的传递,有利于恢复图像,提高了图像分割的准确性。
86.如图3所示,在本实施方式中,所述解码网络包括四个级联的第一残差连接f1、f2、f3和f4,所述编码网络均包括四个级联的第二残差连接f1、f2、f3和f4。其中,在所述解码网络中,通过第一残差连接f1可以将输入层1的输出与第二卷积层a1的输出相加后作为第二卷积层a2的输入;通过第一残差连接f2可以将最大池化层a3的输出与第二卷积层b1的输出相加后作为第二卷积层b2的输入;通过第一残差连接f3可以将最大池化层b3的输出与第二卷积层c1的输出相加后作为第二卷积层c2的输入;通过第一残差连接f4可以将最大池化层c3的输出与第二卷积层d1的输出相加后作为第二卷积层d2的输入。在所述编码网络中,通过第二残差连接f1可以将合并层a2的输出与第四卷积层a4的输出相加后作为反卷积层b1的输入;通过第二残差连接f2可以将合并层b2的输出与第四卷积层b4的输出相加后作为反卷积层c1的输入;通过第二残差连接f3可以将合并层c2的输出与第四卷积层c4的输出相加后作为反卷积层d1的输入;通过第二残差连接f4可以将合并层d2的输出与第四卷积层d4的输出相加后作为第三卷积层e1的输入。
87.需要说明的是,图3所示的深度全卷积神经网络模型中,解码网络包括的第一神经网络组的个数以及编码网络包括的第二神经网络组的个数均为示例,不应理解为对本技术实施方式的限定。所述解码网络包括的第一神经网络组的个数以及编码网络包括的第二神经网络组的个数可以根据具体需要进行设置。需要说明的是,因编码和解码具有一一对应的关系,所以在本技术实施方式提供的深度融合全卷积神经网络模型中,所述解码网络包括的第一神经网络组的个数与编码网络包括的第二神经网络组的个数相等。此外,第一神经网络组包括的第二卷积层的个数以及第二神经网络组包括的第四卷积层的个数不限定为2个,其还可以为3个或3个以上,本发明对其并不进行限制。
88.具体地,所述第一神经网络模型通过以下步骤训练得到:
89.获取第一原始训练样本,所述第一原始训练样本包括第一医学训练图像和与所述
第一医学训练图像对应的第一标签图像,所述第一标签图像为已标注出组织器官的第一医学图像;
90.对所述第一原始训练样本进行扩展,得到扩展后的第一训练样本,所述扩展后的第一训练样本包括扩展后的第一医学训练图像和与所述扩展后的第一医学训练图像对应的第一标签图像;
91.设置第一神经网络模型的模型参数的初始值;以及
92.根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值对预先搭建的第一神经网络模型进行训练,直至满足第一预设训练结束条件。
93.由于第一原始训练样本的数据有限,而深度学习需要在一定数据上进行学习才能具有一定的鲁棒性,为了增加鲁棒性,需要做数据扩增操作,以增加所述深度全卷积网络模型的泛化能力。具体地,可以通过对所述第一原始医学训练图像和对应的第一标签图像分别进行相同的随机刚性变换,具体包括:旋转、缩放、平移、翻转和灰度变换。更具体地,可以对所述第一原始医学训练图像和对应的标签图像分别平移-10到10个像素、旋转-30
°
到30
°
、水平翻转、垂直翻转、缩放0.8到1.2倍、灰度变换等以完成对医学图像的数据扩增。通过上述变换,可以将原先的例如20张图像扩增到2000张,可以用其中的1600张图像进行模型训练,用剩余的400张进行模型测试。
94.优选地,为了提高第一神经网络模型的准确性,在生成扩展后的第一训练样本后,进行第一神经网络模型的训练前,还可以对扩展后的第一训练样本进行预处理,以去除图像中的噪音,提高第一训练样本的图像质量。
95.第一神经网络模型的模型参数包括两类:特征参数和超参数。特征参数是用于学习组织器官特征的参数,例如学习主动脉瓣膜的纹理特征、几何形状特征、位置特征等的参数。特征参数包括权重参数和偏置参数。超参数是在训练时人为设置的参数,只有设置合适的超参数才能从样本中学到特征参数。超参数可以包括学习率、隐藏层个数、卷积核大小、训练迭代次数,每次迭代批次大小。学习率可以看作是步长。
96.举例而言,本发明可以设置学习率为0.001,隐藏层个数分别为16、32、64、128、256,卷积核大小为3
×
3,训练迭代次数为30000次,每次迭代批次大小为1。
97.具体地,所述第一预设训练结束条件为扩展后的第一训练样本中的第一医学训练图像的预测结果与对应的第一标签图像的误差值收敛到第一预设误差值。第一神经网络模型的训练目的是为了由该模型得到的组织器官的分割结果与真实准确的组织器官的分割结果相近,也就是,两者的误差缩小到一定范围,因此,第一预设训练结束条件可以为扩展后的第一训练样本中的第一医学训练图像的预测结果与对应的第一标签图像的误差值收敛到第一预设误差值。此外,第一神经网络模型的训练过程为一个多次循环迭代过程,因此,可以通过设置迭代多少次结束训练,即第一预设训练结束条件还可以为迭代次数达到第一预设迭代次数。
98.进一步地,所述根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值对预先搭建的第一神经网络模型进行训练,包括:
99.根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第一神经网络模型进行训练。
100.由于,模型训练过程实际上是最小化损失函数的过程,而求导数可以快速简单地
实现这个目标,这种求导数的方法就是梯度下降法。由此,采用梯度下降法来训练第一神经网络模型,可以快速简单地实现第一神经网络模型的训练。
101.本发明深度学习中主要利用梯度下降法来训练第一神经网络模型,然后再使用反向传播算法来更新优化第一神经网络模型中的权重参数和偏置参数。具体地,采用梯度下降法判断曲线斜率最大的地方为越快到达最优值的方向,反向传播法是采用概率学的链式求导方法来求偏导数以更新权重,通过不断迭代训练来更新参数,以学习到图像。反向传播算法更新权重参数和偏置参数的方法如下:
102.1、首先进行前向传播,通过不断迭代训练来更新参数,以学习到图像,并且计算所有层(卷积层,反卷积层)的激活值,即图像经过卷积操作后以得到激活图像;
103.2、对输出层(第n
l
层),计算敏感值
[0104][0105]
其中,y为样本真实值,为输出层的预测值,表示输出层参数的偏导数;
[0106]
3、对于l=n
l-1,n
l-2,.....的各层,计算敏感值
[0107][0108]
其中,w
l
表示第l层的权重参数,δ
l+1
表示第l+1层的敏感值,f'(z
l
)表示第l层的偏导数;
[0109]
4、更新每层的权重参数和偏置参数:
[0110][0111][0112]
其中,w
l
和b
l
分别表示l层的权重参数和偏置参数,为学习率,a
l
表示第l层的输出值,δ
l+1
表示l+1层的敏感值。
[0113]
更进一步地,所述根据所述扩展后的第一训练样本和所述第一神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第一神经网络模型进行训练,包括:
[0114]
步骤a1、将扩展后的第一医学训练图像作为第一神经网络模型的输入,根据所述第一神经网络模型的模型参数的初始值,获取所述扩展后的第一医学训练图像的预测结果;
[0115]
步骤b1、根据所述扩展后的第一医学训练图像的预测结果和所述扩展后的第一医学训练图像对应的第一标签图像,计算第一损失函数值;以及
[0116]
步骤c1、判断所述第一损失函数值是否收敛到第一预设误差值,如果是,训练结束,如果否,调整所述第一神经网络模型的模型参数,并将所述第一神经网络模型的模型参数的初始值更新为调整后的模型参数,返回执行所述步骤a1。
[0117]
当第一损失函数值未收敛到第一预设误差值时,表示第一神经网络模型还不准确,需要继续对第一神经网络模型进行训练,如此,则调整模型参数,并将模型参数的初始值更新为调整后的模型参数,返回执行步骤a1,进入下一次迭代过程。
[0118]
第一神经网络模型训练过程中采用的损失函数l(w,b)可以表示为:
[0119][0120]
其中,w和b表示第一神经网络模型的权重参数和偏置参数,m为第一训练样本的数量,m为正整数,xi表示输入的第i个第一训练样本,f
w,b
(xi)表示第i个第一训练样本的预测结果,yi表示第i个第一训练样本的对应的第一标签图像,k是平滑参数,防止分母为零无法计算。
[0121]
步骤s300、将所述第一分割图像与所述待分割医学图像进行逻辑与操作,以获取感兴趣区域图像。
[0122]
由于所获取的第一分割图像为前景(即包括组织器官的区域,例如包括主动脉血管和主动脉瓣膜的区域)为白色(像素值为1),背景为黑色(像素值为0)的二值图像,由此,通过将所述第一分割图像与所述待分割医学图像进行逻辑与操作(将所述第一分割图像中的各个像素点的像素值与所述待分割医学图像(优选为预处理后的待分割医学图像)中的对应的像素点的像素值相乘),从而可以将所述第一分割图像中的前景区域的各个像素点的像素值替换为所述待分割医学图像(优选为预处理后的待分割医学图像)中的对应像素点的像素值,进而可以在待分割医学图像上获取组织器官的roi区域(例如主动脉血管和主动脉瓣膜的roi区域)。请参考图4,其示意性地给出了本发明一实施方式提供的感兴趣区域图像的具体示例。如图4所示,通过将采用第一神经网络模型对cta图像进行初步分割得到的主动脉血管和主动脉瓣膜的初步分割结果与所述cta图像进行逻辑与操作,可以在所述cta图像上获取主动脉血管和主动脉瓣膜的感兴趣区域。
[0123]
步骤s400、采用预先训练好的第二神经网络模型对所述感兴趣区域图像进行分割,以获取组织器官蒙板图像。
[0124]
由此,本发明通过采用预先训练好的第二神经网络模型对所述感兴趣区域图像进行分割,不仅可以准确分割出组织器官蒙板图像(例如主动脉血管和主动脉瓣膜蒙板图像),同时也可以有效减少人机交互的繁琐操作,提高分割精度,为后续获取高质量的组织器官图像(例如主动脉血管和主动脉瓣膜图像)进一步奠定基础。
[0125]
优选地,所述第二神经网络模型为深度全卷积网络模型,所述第二神经网络模型包括解码网络和编码网络。所述解码网络包括输入层、多个级联的第一神经网络组和第一卷积层,所述第一神经网络组包括级联的第二卷积层和最大池化层;所述编码网络包括多个级联的第二神经网络组、第三卷积层和输出层,所述第二神经网络组包括级联的反卷积层、合并层和第四卷积层;所述合并层用于将所述反卷积层的输出与所述解码网络中的相应的所述第二卷积层的输出进行线性相加合并。由此,本发明通过采用深度全卷积网络模型作为第二神经网络模型,可以对感兴趣区域图像的分割结果逐步优化,以实现分割精度的逐步提高。需要说明的是,所述第二神经网络模型的具体结构与所述第一神经网络模型的具体结构类似,关于所述第二神经网络模型的具体结构可以参考上文关于所述第一神经网络模型的描述,故对此不再进行赘述。
[0126]
具体地,所述第二神经网络模型通过以下步骤训练得到:
[0127]
获取第二原始训练样本,所述第二原始训练样本包括第二原始医学训练图像和与
所述第二原始医学训练图像对应的第二标签图像,所述第二原始医学训练图像为包含感兴趣区域的感兴趣区域训练图像,所述第二标签图像为已标注出组织器官的第二医学图像;
[0128]
对所述第二原始训练样本进行扩展,得到扩展后的第二训练样本,所述扩展后的第二训练样本包括扩展后的第二医学训练图像和与所述扩展后的第二医学训练图像对应的第二标签图像;
[0129]
设置第二神经网络模型的模型参数的初始值;以及
[0130]
根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值对预先搭建的第二神经网络模型进行训练,直至满足第二预设训练结束条件。
[0131]
需要说明的是,如本领域技术人员所能理解的,所述第二原始医学训练图像可以为将第一神经网络模型对第一原始医学训练图像进行分割得到的分割结果与第一原始医学训练图像进行逻辑与操作得到,也可以采用其它方式对第一原始医学训练图像进行处理得到,所述第一标签图像和所述第二标签图像可以为同一图像,也可以为不同的图像,本发明对此并不进行限定。此外,需要说明的是,所述第二原始训练样本的扩展方法与所述第一原始训练样本的扩展方法相类似,故对此不再进行赘述。
[0132]
进一步地,所述第二预设训练结束条件为扩展后的第二训练样本中的第二医学训练图像的预测结果与对应的第二标签图像的误差值收敛到第二预设误差值。第二神经网络模型的训练目的是为了由该模型得到的组织器官的分割结果与真实准确的组织器官的分割结果相近,也就是,两者的误差缩小到一定范围,因此,第二预设训练结束条件可以为扩展后的第二训练样本中的第二医学训练图像的预测结果与对应的第二标签图像的误差值收敛到第二预设误差值。此外,第二神经网络模型的训练过程为一个多次循环迭代过程,因此,可以通过设置迭代多少次结束训练,即第二预设训练结束条件还可以为迭代次数达到第二预设迭代次数。
[0133]
进一步地,所述根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值对预先搭建的第二神经网络模型进行训练,包括:
[0134]
更进一步地,所述根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第二神经网络模型进行训练。
[0135]
具体地,利用梯度下降法来训练第二神经网络模型的过程与利用梯度下将法来训练第一神经网络模型的过程相类似,故对此不再进行赘述。
[0136]
所述根据所述扩展后的第二训练样本和所述第二神经网络模型的模型参数的初始值采用随机梯度下降法对预先搭建的第二神经网络模型进行训练,包括:
[0137]
步骤a2、将扩展后的第二医学训练图像作为第二神经网络模型的输入,根据所述第二神经网络模型的模型参数的初始值,获取所述扩展后的第二医学训练图像的预测结果;
[0138]
步骤b2、根据所述扩展后的第二医学训练图像的预测结果和所述扩展后的第二医学训练图像对应的第二标签图像,计算第二损失函数值;以及
[0139]
步骤c2、判断所述第二损失函数值是否收敛到第二预设误差值,如果是,训练结束,如果否,调整所述第二神经网络模型的模型参数,并将所述第二神经网络模型的模型参数的初始值更新为调整后的模型参数,返回执行所述步骤a2。
[0140]
需要说明的是,第二神经网络模型训练过程中采用的损失函数与第一神经网络模
型训练过程中的采用的损失函数相类似,故对此不再进行赘述。
[0141]
步骤s500、将所述组织器官蒙板图像与所述待分割医学图像进行逻辑与操作,以获取最终的组织器官图像。
[0142]
由于所获取的组织器官蒙板图像中的组织器官区域(例如主动脉血管和主动脉瓣膜区域)为白色(像素值为1),非组织器官区域(例如非主动脉血管和非主动脉瓣膜区域)为黑色(像素值为0),由此,通过将所述组织器官蒙板图像与所述待分割医学图像进行逻辑与操作(将所述组织器官蒙板图像中的各个像素点的像素值与所述待分割医学图像(优选为预处理后的待分割医学图像)中的对应像素点的像素值相乘),从而可以将所述组织器官蒙板图像中的组织器官区域(例如主动脉血管和主动脉瓣膜区域)中的各个像素点的像素值替换为所述待分割医学图像(优选为预处理后的待分割医学图像)中的对应像素点的像素值,以获取最终的组织器官图像(例如主动脉血管和主动脉瓣膜图像)。请参考图5和图6,其中图5示意性地给出了本发明一实施方式提供的最终分割得到的组织器官图像的具体示例;图6示意性地给出了采用金标准分割得到的组织器官图像的具体示例。通过将图5和图6进行对比可知,通过采用本发明提供的分割方法对待分割医学图像(例如cta图像)进行分割,可以准确地将想要的组织器官(例如主动脉血管和主动脉瓣膜)从所述待分割医学图像上分割出来,且本发明提供的分割方法得到的分割结果与采用金标准分割得到的分割结果非常接近,可见采用本发明提供的分割方法对待分割医学图像进行分割,不仅可以准确地分割出组织器官图像,同时分割效率和分割精度都得以有效提高。
[0143]
基于同一发明构思,本发明还提供一种电子设备,请参考图7,其示意性地给出了本发明一实施方式提供的电子设备的方框结构示意图。如图7所示,所述电子设备包括处理器101和存储器103,所述存储器103上存储有计算机程序,所述计算机程序被所述处理器101执行时,实现上文所述的医学图像分割方法。
[0144]
如图7所示,所述电子设备还包括通信接口102和通信总线104,其中所述处理器101、所述通信接口102、所述存储器103通过通信总线104完成相互间的通信。所述通信总线104可以是外设部件互连标准(peripheral component interconnect,pci)总线或扩展工业标准结构(extended industry standard architecture,eisa)总线等。该通信总线104可以分为地址总线、数据总线、控制总线等。为便于表示,图中仅用一条粗线表示,但并不表示仅有一根总线或一种类型的总线。所述通信接口102用于上述电子设备与其他设备之间的通信。
[0145]
本发明中所称处理器101可以是中央处理单元(central processing unit,cpu),还可以是其他通用处理器、数字信号处理器(digital signal processor,dsp)、专用集成电路(application specific integrated circuit,asic)、现成可编程门阵列(field-programmable gate array,fpga)或者其他可编程逻辑器件、分立门或者晶体管逻辑器件、分立硬件组件等。通用处理器可以是微处理器或者该处理器也可以是任何常规的处理器等,所述处理器101是所述电子设备的控制中心,利用各种接口和线路连接整个电子设备的各个部分。
[0146]
所述存储器103可用于存储所述计算机程序,所述处理器101通过运行或执行存储在所述存储器103内的计算机程序,以及调用存储在存储器103内的数据,实现所述电子设备的各种功能。
[0147]
所述存储器103可以包括非易失性和/或易失性存储器。非易失性存储器可包括只读存储器(rom)、可编程rom(prom)、电可编程rom(eprom)、电可擦除可编程rom(eeprom)或闪存。易失性存储器可包括随机存取存储器(ram)或者外部高速缓冲存储器。作为说明而非局限,ram以多种形式可得,诸如静态ram(sram)、动态ram(dram)、同步dram(sdram)、双数据率sdram(ddrsdram)、增强型sdram(esdram)、同步链路(synchlink)dram(sldram)、存储器总线(rambus)直接ram(rdram)、直接存储器总线动态ram(drdram)、以及存储器总线动态ram(rdram)等。
[0148]
本发明还提供了一种可读存储介质,所述可读存储介质内存储有计算机程序,所述计算机程序被处理器执行时可以实现上文所述的医学图像分割方法。
[0149]
本发明实施方式的可读存储介质,可以采用一个或多个计算机可读的介质的任意组合。可读介质可以是计算机可读信号介质或者计算机可读存储介质。计算机可读存储介质例如可以是但不限于电、磁、光、电磁、红外线或半导体的系统、装置或器件,或者任意以上的组合。计算机可读存储介质的更具体的例子(非穷举的列表)包括:具有一个或多个导线的电连接、便携式计算机硬盘、硬盘、随机存取存储器(ram)、只读存储器(rom)、可擦式可编程只读存储器(eprom或闪存)、光纤、便携式紧凑磁盘只读存储器(cd-rom)、光存储器件、磁存储器件、或者上述的任意合适的组合。在本文中,计算机可读存储介质可以是任何包含或存储程序的有形介质,该程序可以被指令执行系统、装置或者器件使用或者与其组合使用。
[0150]
计算机可读的信号介质可以包括在基带中或者作为载波一部分传播的数据信号,其中承载了计算机可读的程序代码。这种传播的数据信号可以采用多种形式,包括但不限于电磁信号、光信号或上述的任意合适的组合。计算机可读的信号介质还可以是计算机可读存储介质以外的任何计算机可读介质,该计算机可读介质可以发送、传播或者传输用于由指令执行系统、装置或者器件使用或者与其结合使用的程序。
[0151]
可以以一种或多种程序设计语言或其组合来编写用于执行本发明操作的计算机程序代码,所述程序设计语言包括面向对象的程序设计语言-诸如java、smalltalk、c++,还包括常规的过程式程序设计语言-诸如“c”语言或类似的程序设计语言。程序代码可以完全地在用户计算机上执行、部分地在用户计算机上执行、作为一个独立的软件包执行、部分在用户计算机上部分在远程计算机上执行、或者完全在远程计算机或服务器上执行。在涉及远程计算机的情形中,远程计算机可以通过任意种类的网络——包括局域网(lan)或广域网(wan)连接到用户计算机,或者可以连接到外部计算机(例如利用因特网服务提供商来通过因特网连接)。
[0152]
综上所述,与现有技术相比,本发明提供的医学图像分割方法、电子设备和存储介质具有以下优点:本发明通过先获取待分割医学图像;再采用预先训练好的第一神经网络模型对所述待分割医学图像进行分割,以获取第一分割图像;然后再采用预先训练好的第一神经网络模型对所述待分割医学图像进行分割,以获取第一分割图像;再将所述第一分割图像与所述待分割医学图像进行逻辑与操作,以获取感兴趣区域图像;然后再采用预先训练好的第二神经网络模型对所述感兴趣区域图像进行分割,以获取组织器官蒙板图像;最后再将所述组织器官蒙板图像与所述待分割医学图像进行逻辑与操作,以获取最终的组织器官图像。可见,本发明通过采用第一神经网络模型对待分割医学图像进行初步分割,再
采用第二神经网络模型在所述第一神经网络模型的分割结果的基础上进行进一步分割,不仅可以大大提高整体的分割精度,还可以减少人机交互的繁琐操作。此外,本发明提供的医学图像分割方法,通用性强,实现了端到端的算法流程,可以更好地辅助医生提高诊断的准确性。
[0153]
应当注意的是,在本文的实施方式中所揭露的装置和方法,也可以通过其他的方式实现。以上所描述的装置实施方式仅仅是示意性的,例如,附图中的流程图和框图显示了根据本文的多个实施方式的装置、方法和计算机程序产品的可能实现的体系架构、功能和操作。在这点上,流程图或框图中的每个方框可以代表一个模块、程序或代码的一部分,所述模块、程序段或代码的一部分包含一个或多个用于实现规定的逻辑功能的可执行指令,所述模块、程序段或代码的一部分包含一个或多个用于实现规定的逻辑功能的可执行指令。也应当注意,在有些作为替换的实现方式中,方框中所标注的功能也可以以不同于附图中所标注的顺序发生。例如,两个连续的方框实际上可以基本并行地执行,它们有时也可以按相反的顺序执行,这依所涉及的功能而定。也要注意的是,框图和/或流程图中的每个方框、以及框图和/或流程图中的方框的组合,可以用于执行规定的功能或动作的专用的基于硬件的系统来实现,或者可以用专用硬件与计算机指令的组合来实现。
[0154]
另外,在本文各个实施方式中的各功能模块可以集成在一起形成一个独立的部分,也可以是各个模块单独存在,也可以两个或两个以上模块集成形成一个独立的部分。
[0155]
上述描述仅是对本发明较佳实施方式的描述,并非对本发明范围的任何限定,本发明领域的普通技术人员根据上述揭示内容做的任何变更、修饰,均属于本发明的保护范围。显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若这些修改和变型属于本发明及其等同技术的范围之内,则本发明也意图包括这些改动和变型在内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1