基于MRI影像组学的图像处理方法、装置、设备及存储介质与流程
基于mri影像组学的图像处理方法、装置、设备及存储介质
技术领域
1.本技术涉及图像处理领域,具体而言,涉及一种基于mri影像组学的图像处理方法、装置、设备及存储介质。
背景技术:
2.胶质瘤是最常见的颅内原发神经外胚层肿瘤,起源于大脑或脊髓,由支持神经胶质或前体细胞发展而来,具有发病率高、复发率高、死亡率高,预后差等特点。2016年世界卫生组织(who)对中枢神经系统(cns)脑肿瘤分类进行了巨大的更新,表明胶质瘤的诊断应主要基于分子性能。idh突变作为一种重要的分子生物标志物,引起了众多研究的关注。许多研究表明,idh突变型(idhmut)患者的预后优于野生型(idhwt)患者,且idh突变型胶质瘤对化疗高度敏感。因此,寻找治疗idh突变型胶质瘤的替代策略对临床研究具有重要意义。mri作为一种无创、准确的方法,在临床上常用于胶质瘤的诊断和分期。mri常规序列为t2 flair序列和增强t1加权成像(ce-t1wi)。前者能清楚地显示病变范围和周围水肿情况。ce-t1wi能显示肿瘤坏死,并能将实体瘤与周围浸润部分区分开来。目前已经有多种常规和定量mri方法被纳入到放射组学中来预测idh突变状态,但是目前的方法存在脑胶质瘤idh分类预测的准确度低的缺点。
技术实现要素:
3.本技术实施例的目的在于提供一种基于mri影像组学的图像处理方法、装置、设备及存储介质,用于提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。
4.为此,本技术第一方面一种基于mri影像组学的图像处理方法,所述方法包括:
5.获取针对脑胶质瘤患者扫描生成的第一磁共振成像和第二磁共振成像,所述第一磁共振成像为t2 flair,所述第二磁共振成像为ce-t1wi;
6.基于逐层分割所述第一磁共振成像和所述第二磁共振成像上的脑胶质瘤病变区域,计算所述第一磁共振成像和所述第二磁共振成像的3d影像组学特征;
7.根据所述3d影像组学特征计算得到影像组学标签;
8.确定与脑胶质瘤患者idh高度相关的临床信息;
9.根据所述临床信息、所述影像组学标签构建预测模型;
10.根据所述预测模型对目标图像进行处理,并输出预测结果。
11.本技术第一方面的方法能够有效帮助医生提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。
12.在本技术第一方面中,作为一种可选的实施方式,根据所述3d影像组学特征计算得到影像组学标签,包括:
13.根据五折交叉验证算法对所述3d影像组学特征进行分组,以对所述3d影像组学特征进行降维并得到降维后的特征值数据;
14.根据所述降维后的特征值数据计算得到所述影像组学标签。
15.在申请实施例中,根据降维后的特征值数据能够计算得到影像组学标签。
16.在本技术第一方面中,作为一种可选的实施方式,所述根据五折交叉验证算法对所述3d影像组学特征进行分组,以对所述3d影像组学特征进行降维并得到降维后的特征值数据,包括:
17.对所述3d影像组学特征进行标准化处理;
18.计算标准化处理后的所述3d影像组学特征中每个特征值的方差;
19.筛选出方差大于第一预设阈值的特征值并作为第一筛选集;
20.根据单变量特征选择算法从所述第一筛选集中筛选出p值小于第二预设阈值的特征,并作为第二筛选集;
21.根据回归模型对所述第二筛选集后进行处理并得到所述降维后的特征值数据。
22.在本可选的实施方式中,通过对3d影像组学特征进行标准化处理,进而能够计算标准化处理后的3d影像组学特征中每个特征值的方差,进而能够筛选出方差大于第一预设阈值的特征值并作为第一筛选集,进而能够根据单变量特征选择算法从第一筛选集中筛选出p值小于第二预设阈值的特征,并作为第二筛选集,从而能够根据回归模型对第二筛选集后进行处理并得到降维后的特征值数据。
23.在本技术第一方面中,作为一种可选的实施方式,所述第一预设阈值为0.8,所述第二预设阈值为0.05。
24.在本可选的实施方式中,通过将第二预设阈值设置为0.05,能够从第一筛选集中筛选出p值小于第二预设阈值的特征。
25.在本技术第一方面中,作为一种可选的实施方式,所述降维后的特征值数据包括影像组学特征值和相关系数;
26.以及,根据所述降维后的特征值数据计算得到所述影像组学标签的计算公式为:
[0027][0028]
其中,radscore表示影像组学标签,radfi表示所述影像组学特征值,coefi表示所述相关系数。
[0029]
在本可选的实施方式中,通过上述计算公式能够精确计算影像组学标签。
[0030]
在本技术第一方面中,作为一种可选的实施方式,所述3d影像组学特征包括一阶特征、形状特征、纹理特征和高阶特征。
[0031]
本技术第二方面公开一种基于mri影像组学的图像处理装置,所述装置包括:
[0032]
获取模块,用于获取针对脑胶质瘤患者扫描生成的第一磁共振成像和第二磁共振成像,所述第一磁共振成像为t2 flair,所述第二磁共振成像为ce-t1wi;
[0033]
第一计算模块,用于基于逐层分割所述第一磁共振成像和所述第二磁共振成像上的脑胶质瘤病变区域,计算所述第一磁共振成像和所述第二磁共振成像的3d影像组学特征;
[0034]
第二计算模块,用于根据所述3d影像组学特征计算得到影像组学标签;
[0035]
确定模块,用于确定与脑胶质瘤患者idh高度相关的临床信息;
[0036]
构建模块,用于根据所述临床信息、所述影像组学标签构建预测模型;
[0037]
预测模块,用于根据所述预测模型对目标图像进行处理,并输出预测结果。
[0038]
本技术第一方面的装置能够有效帮助医生提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。
[0039]
在本技术第二方面中,作为一种可选的实施方式,所述第二计算模块,包括:
[0040]
分组子模块,用于根据五折交叉验证算法对所述3d影像组学特征进行分组,以对所述3d影像组学特征进行降维并得到降维后的特征值数据;
[0041]
降维子模块,用于根据所述降维后的特征值数据计算得到所述影像组学标签。
[0042]
本技术第三方面公开一种基于mri影像组学的图像处理设备,所述设备包括:
[0043]
处理器;以及存储器,配置用于存储机器可读指令,所述指令在由所述处理器执行时,使得所述处理器执行本技术第一方面的基于mri影像组学的图像处理方法。
[0044]
本技术第三方面的设备通过执行基于mri影像组学的图像处理方法,进而能够有效帮助医生提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。
[0045]
本技术第四方面公开一种存储介质,所述存储介质存储有计算机程序,所述计算机程序被处理器执行本技术第一方面的基于mri影像组学的图像处理方法。
[0046]
本技术第四方面的存储介质通过执行基于mri影像组学的图像处理方法,进而能够有效帮助医生提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。
附图说明
[0047]
为了更清楚地说明本技术实施例的技术方案,下面将对本技术实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本技术的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
[0048]
图1是本技术实施例公开的一种基于mri影像组学的图像处理方法的流程示意图;
[0049]
图2是本技术实施例公开的一种第一磁共振成像的示意图;
[0050]
图3是本技术实施例公开的一种第二磁共振成像的示意图;
[0051]
图4是本技术实施例公开的一种标记脑胶质瘤病变区域的第一磁共振成像的示意图;
[0052]
图5是本技术实施例公开的一种标记脑胶质瘤病变区域的第二磁共振成像的示意图;
[0053]
图6是本技术实施例公开的第一验证模型的logistic回归模型五折交叉验证结果示意图;
[0054]
图7是本技术实施例公开的第二验证模型的logistic回归模型五折交叉验证结果示意图;
[0055]
图8是本技术实施例公开的第三验证模型的logistic回归模型五折交叉验证结果示意图;
[0056]
图9是本技术实施例公开的一种基于mri影像组学的图像处理装置的结构示意图;
[0057]
图10是本技术实施例公开的一种基于mri影像组学的图像处理设备的结构示意
图。
具体实施方式
[0058]
下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行描述。
[0059]
实施例一
[0060]
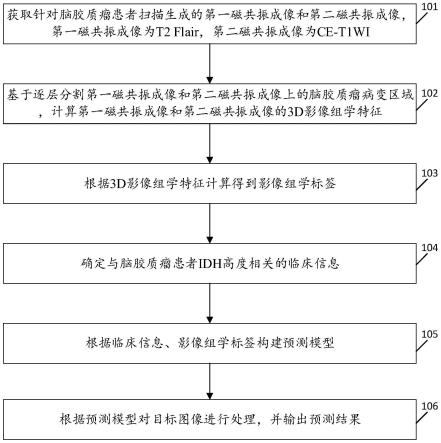
请参阅1,图1是本技术实施例公开的一种基于mri影像组学的图像处理方法的流程示意图。如图1所示,本技术实施例的基于mri影像组学的图像处理方法包括步骤:
[0061]
101、获取针对脑胶质瘤患者扫描生成的第一磁共振成像和第二磁共振成像,第一磁共振成像为t2 flair,第二磁共振成像为ce-t1wi;
[0062]
102、基于逐层分割第一磁共振成像和第二磁共振成像上的脑胶质瘤病变区域,计算第一磁共振成像和第二磁共振成像的3d影像组学特征;
[0063]
103、根据3d影像组学特征计算得到影像组学标签;
[0064]
104、确定与脑胶质瘤患者idh高度相关的临床信息;
[0065]
105、根据临床信息、影像组学标签构建预测模型;
[0066]
106、根据预测模型对目标图像进行处理,并输出预测结果。
[0067]
在本技术实施例中,作为步骤101的一个示例,获取2016年1月1日至2017年12月31日的接受3.0t mri-t2flair和ce t1wi序列扫描的患者的图像数据,即如图2所示的接受3.0t mri-t2flair扫描生成的第一磁共振成像、如图3所示的接受ce t1wi扫描生成的第二磁共振成像。
[0068]
在本技术实施例中,作为步骤102的一个示例,如图4所示,将第一磁共振成像中的h区域作为脑胶质瘤病变区域,另一方面如图5所示,将第二磁共振成像中的g区域作为脑胶质瘤病变区域。
[0069]
在本技术实施例中,临床特征特征分为2类,定性语义特征和定量特征。定性语义特征是医学成像中用来描述病变的特征。而定量特征是通过软件应用数学算法提取出来的描述特征,可以表现出不同程度的复杂性。
[0070]
在本技术实施例中,可将3d影像组学特征分类为一阶特征、形状特征、纹理特征和高阶特征,需要说明的是,关于具体如何将病变直径、形状、边缘、密度、空洞、钙等特征分类为一阶特征、形状特征、纹理特征和高阶特征请参考现有技术,本技术实施不做赘述。
[0071]
在本技术实施例中,作为步骤104的一个示例,通过收集脑胶质瘤患者人口统计学信息、组学病理学信息等资料,采用正太分布检验、t检验、卡方检验等算法,能够确定与脑胶质瘤患者idh高度相关的临床信息。例如图表1所示的临床和组织病理学特征检验表中,可根据统计结果确定与脑胶质瘤患者idh高度相关的临床信息。
[0072]
[0073][0074]
表1
[0075]
在本技术时候示例,根据临床信息、影像组学标签构建的预测模型可以是将临床信息、影像组学标签作为基础神经网络模型的输入,并通过训练该基础神经网络模型而得到。
[0076]
综上,本技术实施例的方法能够有效帮助医生提高脑胶质瘤预后的预测准确度,
以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。尤其是本技术实施例能够根据临床信息、影像组学标签构建预测模型,进而能够输出更加准确的脑胶质瘤idh分类预测结果,这与现有技术通过基于单一临床信息构建预测模型、基于单一影像组学标签构建预测模型而生成的脑胶质瘤idh分类预测结果相比,具有更高的准确性。
[0077]
在本技术实施例中,作为一种可选的实施方式,步骤103:根据3d影像组学特征计算得到影像组学标签,包括子步骤:
[0078]
根据五折交叉验证算法对3d影像组学特征进行分组,以对3d影像组学特征进行降维并得到降维后的特征值数据;
[0079]
根据降维后的特征值数据计算得到影像组学标签。
[0080]
在本可选的实施例中,根据降维后的特征值数据能够计算得到影像组学标签。
[0081]
在本可选实施例中,由于3d影像组学特征中有些特征与脑胶质瘤idh的分类预测关联性不大,因此通过对3d影像组学特征进行降维,能够去除与脑胶质瘤idh的分类预测关联性不大的特征,从而进一步提高脑胶质瘤idh的分类预测的结果。需要说明的是,进行降维而筛选出的3d影像组学特征如表2所示。
[0082]
[0083]
[0084]
[0085]
[0086]
[0087][0088]
表2
[0089]
在本技术实施例,作为一种可选的实施方式,步骤:根据五折交叉验证算法对3d影像组学特征进行分组,以对3d影像组学特征进行降维并得到降维后的特征值数据,包括:
[0090]
对3d影像组学特征进行标准化处理;
[0091]
计算标准化处理后的3d影像组学特征中每个特征值的方差;
[0092]
筛选出方差大于第一预设阈值的特征值并作为第一筛选集;
[0093]
根据单变量特征选择算法从第一筛选集中筛选出p值小于第二预设阈值的特征,并作为第二筛选集;
[0094]
根据回归模型对第二筛选集后进行处理并得到降维后的特征值数据。
[0095]
在本可选的实施方式中,通过对3d影像组学特征进行标准化处理,进而能够计算标准化处理后的3d影像组学特征中每个特征值的方差,进而能够筛选出方差大于第一预设阈值的特征值并作为第一筛选集,进而能够根据单变量特征选择算法从第一筛选集中筛选出p值小于第二预设阈值的特征,并作为第二筛选集,从而能够根据回归模型对第二筛选集后进行处理并得到降维后的特征值数据。
[0096]
需要说明的是,在本可选的实施方式中,通过回归模型即lasso(least absolute shrinkage and selection operator,最小绝对收缩算子),能够将线性模型系数的l1范数作为惩罚项加到损失函数上,使得弱相关特征所对应的系数变为0,实现特征筛选。
[0097]
在本技术实施例中,作为一种可选的实施方式,第一预设阈值为0.8,第二预设阈值为0.05。
[0098]
在本可选的实施方式中,通过将第二预设阈值设置为0.05,能够从第一筛选集中筛选出p值小于第二预设阈值的特征。
[0099]
在本技术第一方面中,作为一种可选的实施方式,降维后的特征值数据包括影像组学特征值和相关系数;
[0100]
以及,根据降维后的特征值数据计算得到影像组学标签的计算公式为:
[0101][0102]
其中,radscore表示影像组学标签,radfi表示影像组学特征值,coefi表示相关系数。
[0103]
在本可选的实施方式中,通过上述计算公式能够精确计算影像组学标签。
[0104]
在本技术第一方面中,作为一种可选的实施方式,本技术实施例的方法还包括:
[0105]
单独根据临床信息构建第一验证模型;
[0106]
单独根据影像组学标签构建第二验证模型;
[0107]
根据临床信息和影像组学标签构建第三验证模型;
[0108]
将测试数据集依次作为第一验证模型、第二验证模型、第三验证模型的输入;
[0109]
根据第一验证模型的输出结果、第二验证模型的输出结果、第三验证模型的输出
结果确定预测模型。
[0110]
在本可选的实施方式中,通过将测试数据集依次作为第一验证模型、第二验证模型、第三验证模型的输入,进而能够根据第一验证模型的输出结果、第二验证模型的输出结果、第三验证模型的输出结果确定预测模型。
[0111]
在本可选的实施例中,作为一个示例,如图6、图7、图8所示,图6、图7、图8分别是第一验证模型的logistic回归模型五折交叉验证结果示意图、第二验证模型的logistic回归模型五折交叉验证结果示意图、第三验证模型的logistic回归模型五折交叉验证结果示意图。根据图6、图7、图8,可知根据临床信息和影像组学标签构建第三验证模型的预测准确度更高。
[0112]
实施例二
[0113]
请参阅9,图9是本技术实施例公开的一种基于mri影像组学的图像处理装置的结构示意图。如图9所示,本技术实施例的基于mri影像组学的图像处理装置包括:
[0114]
获取模块201,用于获取针对脑胶质瘤患者扫描生成的第一磁共振成像和第二磁共振成像,第一磁共振成像为t2 flair,第二磁共振成像为ce-t1wi;
[0115]
第一计算模块202,用于基于逐层分割第一磁共振成像和第二磁共振成像上的脑胶质瘤病变区域,计算第一磁共振成像和第二磁共振成像的3d影像组学特征;
[0116]
第二计算模块203,用于根据3d影像组学特征计算得到影像组学标签;
[0117]
确定模块204,用于确定与脑胶质瘤患者idh高度相关的临床信息;
[0118]
构建模块205,用于根据临床信息、影像组学标签构建预测模型;
[0119]
预测模块206,用于根据预测模型对目标图像进行处理,并输出预测结果。
[0120]
本技术实施例的装置能够有效帮助医生提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。尤其是本技术实施例能够根据临床信息、影像组学标签构建预测模型,进而能够输出更加准确的脑胶质瘤idh分类预测结果,这与现有技术通过基于单一临床信息构建预测模型、基于单一影像组学标签构建预测模型而生成的脑胶质瘤idh分类预测结果相比,具有更高的准确性。
[0121]
在本技术实施例中,作为一种可选的实施方式,第二计算模块203,包括:
[0122]
分组子模块,用于根据五折交叉验证算法对3d影像组学特征进行分组,以对3d影像组学特征进行降维并得到降维后的特征值数据;
[0123]
降维子模块,用于根据降维后的特征值数据计算得到影像组学标签。
[0124]
在本可选实施例中,由于3d影像组学特征中有些特征与脑胶质瘤idh的分类预测关联性不大,因此通过对3d影像组学特征进行降维,能够去除与脑胶质瘤idh的分类预测关联性不大的特征,从而进一步提高脑胶质瘤idh的分类预测的结果。
[0125]
需要说明的是,关于本技术实施例的装置的其他说明请参考本技术实施例一中的详细描述,本技术实施例对此不作赘述。
[0126]
实施例三
[0127]
请参阅10,图10是本技术实施例公开的一种基于mri影像组学的图像处理设备的结构示意图。如图10所示,本技术实施例的基于mri影像组学的图像处理设备包括:
[0128]
处理器301;以及存储器302,配置用于存储机器可读指令,指令在由处理器301执行时,使得处理器301执行本技术实施例的基于mri影像组学的图像处理方法。
[0129]
本技术实施例的设备通过执行基于mri影像组学的图像处理方法,进而能够有效帮助医生提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。尤其是本技术实施例能够根据临床信息、影像组学标签融合后构建综合预测模型,进而能够输出更加准确的脑胶质瘤idh分类预测结果,这与现有技术通过基于单一临床信息构建预测模型、基于单一影像组学标签构建预测模型而生成的脑胶质瘤idh分类预测结果相比,具有更高的准确性。
[0130]
实施例四
[0131]
本技术第四方面公开一种存储介质,存储介质存储有计算机程序,计算机程序被处理器执行本技术第一方面的基于mri影像组学的图像处理方法。
[0132]
本技术第四方面的存储介质通过执行基于mri影像组学的图像处理方法,进而能够有效帮助医生提高脑胶质瘤预后的预测准确度,以辅助医生优化脑胶质瘤治疗策略,改善患者的长期预后结局。尤其是本技术实施例能够根据临床信息、影像组学标签构建预测模型,进而能够输出更加准确的脑胶质瘤idh分类预测结果,这与现有技术通过基于单一临床信息构建预测模型、基于单一影像组学标签构建预测模型而生成的脑胶质瘤idh分类预测结果相比,具有更高的准确性。
[0133]
在本技术所提供的实施例中,应该理解到,所揭露装置和方法,可以通过其它的方式实现。以上所描述的装置实施例仅仅是示意性的,例如,所述单元的划分,仅仅为一种逻辑功能划分,实际实现时可以有另外的划分方式,又例如,多个单元或组件可以结合或者可以集成到另一个系统,或一些特征可以忽略,或不执行。另一点,所显示或讨论的相互之间的耦合或直接耦合或通信连接可以是通过一些通信接口,装置或单元的间接耦合或通信连接,可以是电性,机械或其它的形式。
[0134]
另外,作为分离部件说明的单元可以是或者也可以不是物理上分开的,作为单元显示的部件可以是或者也可以不是物理单元,即可以位于一个地方,或者也可以分布到多个网络单元上。可以根据实际的需要选择其中的部分或者全部单元来实现本实施例方案的目的。
[0135]
再者,在本技术各个实施例中的各功能模块可以集成在一起形成一个独立的部分,也可以是各个模块单独存在,也可以两个或两个以上模块集成形成一个独立的部分。
[0136]
需要说明的是,功能如果以软件功能模块的形式实现并作为独立的产品销售或使用时,可以存储在一个计算机可读取存储介质中。基于这样的理解,本技术的技术方案本质上或者说对现有技术做出贡献的部分或者该技术方案的部分可以以软件产品的形式体现出来,该计算机软件产品存储在一个存储介质中,包括若干指令用以使得一台计算机设备(可以是个人计算机,服务器,或者网络设备等)执行本技术各个实施例所述方法的全部或部分步骤。而前述的存储介质包括:u盘、移动硬盘、只读存储器(read-only memory,rom)随机存取存储器(random access memory,ram)、磁碟或者光盘等各种可以存储程序代码的介质。
[0137]
在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。
[0138]
以上所述仅为本技术的实施例而已,并不用于限制本技术的保护范围,对于本领
域的技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
[0139]
需要说明的是,本技术实施例的方法处了对胶质瘤的mri影像组学的图像处理进而提高脑胶质瘤idh分类预测结果之外,还能够对其他疾病的mri影像组学的图像处理,例如,基于椎间盘源性下腰部的mri影像组学对椎间盘源性下腰部疼痛分级预测。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1