全固体电池以及全固体电池的制造方法与流程
本发明涉及具有橄榄石型正极活性物质的硫化物全固体电池及其制造方法。
背景技术:
当前,从能量密度高这样的观点来看,在各种电池中,锂离子电池得到关注。在其中,将电解液置换为固体电解质的全固体电池特别得到关注。其理由在于,与使用电解液的二次电池不同,全固体电池不使用电解液,所以不会产生过充电所引起的电解液的分解等,并且具有高的循环特性及能量密度。
作为在锂离子电池中使用的正极活性物质,已知橄榄石型正极活性物质。橄榄石型正极活性物质相比于其它正极活性物质具有稳定的构造,具有高的循环特性。因此,近年来正在研究使用了橄榄石型正极活性物质的全固体电池。
专利文献1公开了作为全固体电池的正极活性物质,能够使用作为橄榄石型正极活性物质的LiXPO4(X=Fe、Co,Ni以及Mn)。
另外,在专利文献2中,作为使用了在非晶态状态下作为正极活性物质发挥功能并具有高的离子传导度的正极活性物质的全固体电池,公开了将非晶态的磷酸铁锂用作正极活性物质的全固体电池。
【专利文献1】日本特表2014-534591号公报
【专利文献2】日本特开2011-108533号公报
技术实现要素:
以专利文献1为首,可以说作为全固体电池的正极活性物质能够使用橄榄石型正极活性物质,但实际上,如专利文献2那样,只是制作使用了磷酸铁锂和硫化物固体电解质的全固体电池。即,未报告制造出使用了磷酸铁锂以外的橄榄石型正极活性物质和硫化物固体电解质的全固体电池的例子。
实际上,在使用了磷酸铁锂以外的橄榄石型正极活性物质和硫化物固体电解质的全固体电池中,电池的容量显著变小。认为这是因为在对这样的全固体电池进行了充电的情况下,橄榄石型正极活性物质和硫化物固体电解质化学反应,在橄榄石型正极活性物质和硫化物固体电解质的界面形成电阻层。
本发明的目的在于,提供一种具有LiFePO4以外的橄榄石型正极活性物质和硫化物固体电解质且电池容量提高的全固体电池及其制造方法。
用于解决上述课题的单元如下所述:
1.一种全固体电池,按照正极活性物质层、硫化物固体电解质层以及负极活性物质层的顺序具有正极活性物质层、硫化物固体电解质层以及负极活性物质层,
所述正极活性物质层具有作为第1正极活性物质的LixYyPOz以及作为第2正极活性物质的Lix’Fey’POz’,其中,Y=Ni、Mn和/或Co,0.5≤x≤1.5、0.5≤y≤1.5、2≤z≤7,0.5≤x’≤1.5、0.5≤y’≤1.5、2≤z’≤7,并且
所述第2正极活性物质配置于(a)所述正极活性物质层的所述硫化物固体电解质层侧和/或(b)所述第1正极活性物质的粒子的表面。
2.一种全固体电池的制造方法,是按照正极活性物质层、固体电解质层以及负极活性物质层的顺序具有正极活性物质层、固体电解质层以及负极活性物质层的全固体电池的制造方法,
包括:制造按照所述正极活性物质层、所述固体电解质层以及所述负极活性物质层的顺序具有所述正极活性物质层、所述固体电解质层以及所述负极活性物质层的全固体电池前驱体,然后进行将所述全固体电池前驱体的温度维持为25℃以上且80℃以下、并且将所述全固体电池前驱体放电至2.1V(vs.Li/Li+)以下的充放电循环,
所述正极活性物质层具有作为第1正极活性物质的LixYyPOz以及作为第2正极活性物质的Lix’Fey’POz’,其中,Y=Ni、Mn和/或Co,0.5≤x≤1.5、0.5≤y≤1.5、2≤z≤7,0.5≤x’≤1.5、0.5≤y’≤1.5、2≤z’≤7,并且
所述第2正极活性物质配置于所述正极活性物质层的所述硫化物固体电解质层侧和/或所述第1正极活性物质的粒子的表面。
3.根据所述2记载的全固体电池的制造方法,在所述充放电循环中,使所述全固体电池前驱体放电直至所述正极活性物质层的电位成为1.6V(vs.Li/Li+)以上且2.1V(vs.Li/Li+)以下。
4.根据所述2或者3记载的制造方法,以1.0C以下的充放电速率,进行所述充放电循环。
5.根据所述2~4中的任意一项记载的制造方法,在所述充放电循环中,进行充电直至所述正极活性物质层的电位成为3.8V(vs.Li/Li+)以上且4.4V(vs.Li/Li+)以下。
6.根据所述2~5中的任意一项记载的方法,反复进行所述充放电循环直至所述全固体电池前驱体的放电容量变得比初次的充放电循环中的放电容量大。
7.根据所述2~6中的任意一项记载的制造方法,进行所述充放电循环,直至在放电时的所述正极活性物质层中在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处放电平台消失。
8.根据所述2~7中的任意一项记载的制造方法,进行所述充放电循环,直至在放电时的所述正极活性物质层中在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处产生放电平台。
9.根据所述2~8中的任意一项所述的制造方法,连续地进行所述充放电循环。
10.根据所述9记载的制造方法,从初次的充放电进行所述充放电循环。
11.根据所述2~10中的任意一项记载的制造方法,包括:在至少进行3次所述充放电循环之后,将所述全固体电池前驱体以40~80℃保温40小时以上。
根据本发明,能够提供具有LiFePO4以外的橄榄石型正极活性物质和硫化物固体电解质且电池容量提高的全固体电池及其制造方法。
附图说明
图1是本发明的全固体电池的一个实施方式的示意剖面图。
图2是本发明的全固体电池的一个实施方式中的正极活性物质粒子的示意剖面图。
图3是在正极活性物质层中具有LiFePO4以外的橄榄石型正极活性物质的全固体电池的示意剖面图。
图4是在正极活性物质层中均匀地具有LiFePO4以及除了LiFePO4以外的橄榄石型正极活性物质的全固体电池的示意剖面图。
图5是形成了表面的电阻层的橄榄石型正极活性物质粒子的示意剖面图。
图6是表面的电阻层被破坏的橄榄石型正极活性物质粒子的示意剖面图。
图7A是示出本发明的全固体电池的循环伏安测定的结果的图。
图7B是示出本发明的全固体电池的循环伏安测定的结果的图。
图8是示出在正极活性物质层中均匀地具有LiCoPO4以及LiFePO4的全固体电池的循环伏安测定的结果的图。
图9是示出作为正极活性物质具有LiCoPO4的全固体电池的循环伏安测定的结果的图。
图10A是示出将全固体电池的温度维持为25℃而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图10B是示出将全固体电池的温度维持为42℃而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图10C是示出将全固体电池的温度维持为60℃而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图10D是示出将全固体电池的温度维持为80℃而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图10E是示出将全固体电池的温度维持为100℃而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图11A是示出将充放电速率维持为0.02C而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图11B是示出将充放电速率维持为0.05C而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图11C是示出将充放电速率维持为0.1C而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图11D是示出将充放电速率维持为0.5C而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图11E是示出将充放电速率维持为1.0C而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图12A是示出将正极活性物质的充电上限电位维持为3.8V(vs.Li/Li+)而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图12B是示出将正极活性物质的充电上限电位维持为4.1V(vs.Li/Li+)而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图12C是示出将正极活性物质的充电上限电位维持为4.4V(vs.Li/Li+)而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图12D是示出将正极活性物质的充电上限电位维持为4.7V(vs.Li/Li+)而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图13A是示出将正极活性物质的放电下限电位维持为1.6V(vs.Li/Li+)而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图13B是示出将正极活性物质的放电下限电位维持为2.1V(vs.Li/Li+)而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图13C是示出将正极活性物质的放电下限电位维持为2.3V(vs.Li/Li+)而反复进行了充放电循环的情况下的、电压与电池容量的关系的图表。
图14是示出在充放电循环之后将全固体电池以80℃保存了40小时的情况下的电压与电池容量的关系的图表。
(符号说明)
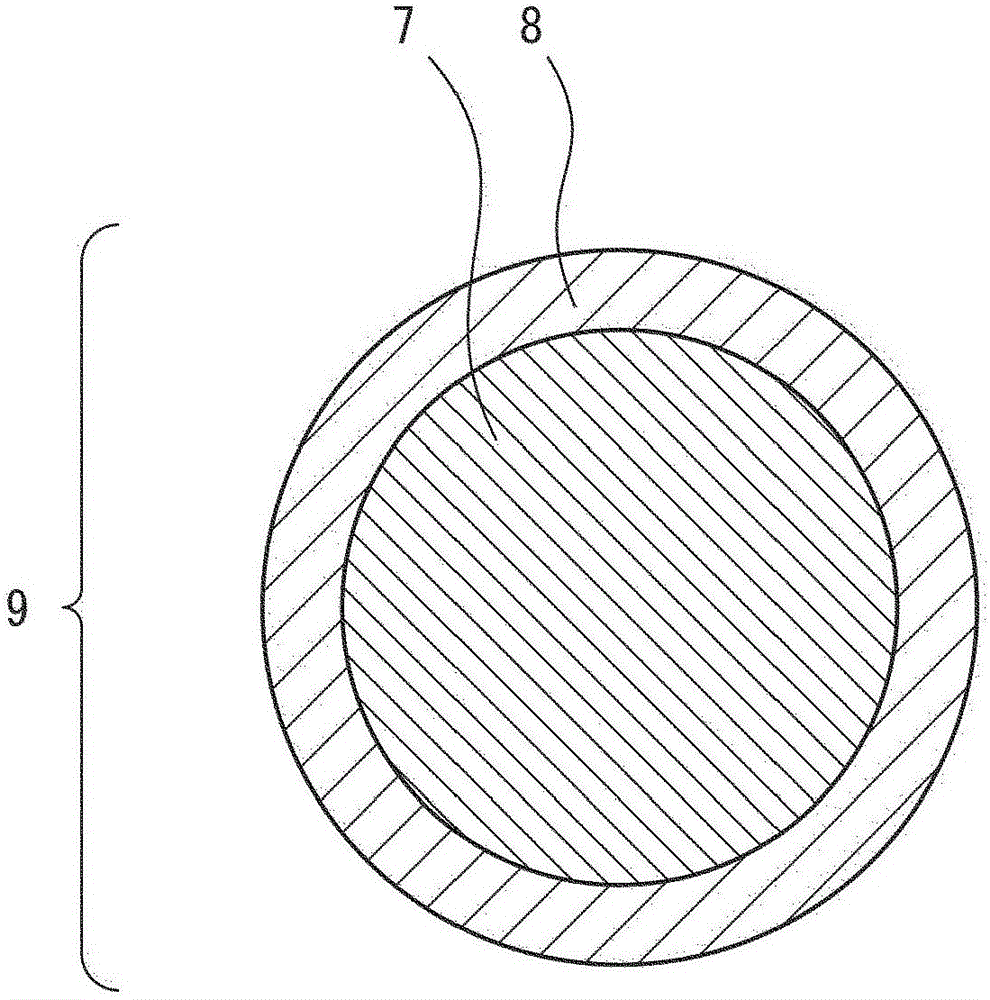
1:正极集电体;2a:具有第1正极活性物质的第1正极活性物质层;2b:具有第2正极活性物质的第2正极活性物质层;2c:均匀地混合了第1正极活性物质以及第2正极活性物质的正极活性物质层;3:硫化物固体电解质层;4:负极活性物质层;5:负极集电体;6:全固体电池;7:LiYPO4;8:LiFePO4;9:正极活性物质粒子;10:正极活性物质的一次粒子;11:磷酸铁锂;12:包覆层;13:碳包覆层;14:电阻层;15:过渡金属含有硫化物区域。
具体实施方式
<<本发明的全固体电池>>
以下,详述本发明的实施方式。此外,本发明不限于以下的实施方式,能够在发明的要旨的范围内实施各种变形。
本发明的全固体电池按照正极活性物质层、硫化物固体电解质层以及负极活性物质层的顺序具有正极活性物质层、硫化物固体电解质层以及负极活性物质层。正极活性物质层具有作为第1正极活性物质的LixYyPOz(Y=Ni、Mn和/或Co,0.5≤x≤1.5、0.5≤y≤1.5、2≤z≤7)以及作为第2正极活性物质的Lix’Fey’POz’(0.5≤x’≤1.5、0.5≤y’≤1.5、2≤z’≤7)。另外,第2正极活性物质配置于(a)所述正极活性物质层的所述硫化物固体电解质层侧和/或(b)所述第1正极活性物质的粒子的表面。
虽然并不通过原理限定,但认为本发明的作用原理如以下所述。
图1是本发明的全固体电池的一个实施方式的示意剖面图。本发明的全固体电池(6)具有正极集电体(1)、正极活性物质层(2a、2b)、硫化物固体电解质层(3)、负极活性物质层(4)以及负极集电体(5)。在图1中,全固体电池具有:具有第1正极活性物质的第1正极活性物质层(2a)和具有第2正极活性物质的第2正极活性物质层(2b)。此外,图1仅为图示本发明的实施方式之一的附图,不是限定本发明的内容的意思。
另外,图2是本发明的全固体电池的另一个实施方式中的、正极活性物质粒子的示意剖面图。在图中,正极活性物质粒子(9)具有第1正极活性物质(7),第1正极活性物质(7)被第2正极活性物质(8)包覆。此外,图2仅为图示本发明的实施方式之一的附图,不是限定本发明的内容的意思。
本发明人发现了如下情况:在作为正极活性物质使用了磷酸铁锂、并且作为固体电解质使用了硫化物固体电解质的全固体电池中,当对电池进行充电时,在磷酸铁锂与硫化物固体电解质之间形成电阻层的同时,在该电阻层的内侧即该电阻层和磷酸铁锂的界面,形成从磷酸铁锂脱离作为其构成要素的Fe而得到的包覆层。该包覆层是Fe少的稳定的磷酸的层,与硫化物固体电解质的反应性小。因此,该包覆层考虑为具有抑制在电池的充放电时磷酸铁锂与硫化物固体电解质反应的、作为保护层的功能。
另外,本发明人发现了如下情况:在磷酸铁锂和硫化物固体电解质的界面形成的电阻层仅通过反复进行一定条件的充放电循环就能够去除,所以通过使用在正极活性物质粒子的表面具有磷酸铁锂的正极活性物质和/或在正极活性物质层的硫化物固体电解质层侧的表面具有磷酸铁锂的正极活性物质层,还能够高效地使用磷酸铁锂以外的橄榄石型正极活性物质例如LiNiPO4、LiMnPO4或者LiCoPO4等。去除电阻层的充放电循环的条件特别优选为在下述的<<本发明的全固体电池的制造方法>>中记载的条件。
图3是使用了LiNiPO4、LiMnPO4或者LiCoPO4等除了磷酸铁锂以外的橄榄石型正极活性物质的全固体电池的示意剖面图。在图中,全固体电池(6)具有正极集电体(1)、具有第1正极活性物质的正极活性物质层(2a)、硫化物固体电解质层(3)、负极活性物质层(4)以及负极集电体(5)。在此,第1正极活性物质包含LiNiPO4、LiMnPO4或者LiCoPO4等。
即使针对这样的全固体电池反复进行一定条件下的充放电循环,电池容量也不会提高。其理由虽然不明确,但考虑在充放电时无法去除电阻层和/或无法形成保护层等的理由。
相对于此,在本发明的全固体电池中,如图1那样,在具有第1正极活性物质的第1正极活性物质层(2a)与硫化物固体电解质层(3)之间,存在具有包含磷酸铁锂的第2正极活性物质的第2正极活性物质层(2b)。在对本发明的全固体电池进行了充电的情况下在第2正极活性物质层(2b)与硫化物固体电解质层(3)之间也形成电阻层,但如果反复进行在例如下述的<<本发明的全固体电池的制造方法>>中记载的条件等一定条件的充放电循环,则容易地去除该电阻层,所以能够得到充分的电池容量。
即,通过使第2正极活性物质介于第1正极活性物质与硫化物固体电解质之间,不会使第1正极活性物质和硫化物固体电解质反应,而能够高效地使用第1正极活性物质。
此外,即使与本发明同样地使用包含第1正极活性物质以及第2正极活性物质的正极活性物质的情况下,在是如图4那样具有均匀地混合了第1正极活性物质以及第2正极活性物质的正极活性物质层(2c)的全固体电池的情况下,也在正极活性物质层和硫化物固体电解质层的界面形成由于第1正极活性物质和硫化物固体电解质反应所致的电阻层,所以即使反复进行一定条件的充放电循环,全固体电池的容量也小。
<全固体电池>
本发明的全固体电池按照正极活性物质层、硫化物固体电解质层以及负极活性物质层的顺序具有正极活性物质层、硫化物固体电解质层以及负极活性物质层。
<正极活性物质层>
1.正极活性物质层
在本发明中,正极活性物质层具有正极活性物质,以及任意地具有固体电解质、导电助剂、粘合剂。
(1)正极活性物质
本发明的全固体电池具有作为第1正极活性物质的LixYyPOz(Y=、Ni、Mn或者Co,0.5≤x≤1.5、0.5≤y≤1.5、2≤z≤7))、以及作为第2正极活性物质的Lix’Fey’POz’(0.5≤x’≤1.5、0.5≤y’≤1.5、2≤z’≤7)。
另外,第1正极活性物质和第2正极活性物质满足下述的(a)和/或(b)的条件:
(a)第2正极活性物质配置于正极活性物质层的硫化物固体电解质层侧。
(b)第2正极活性物质配置于第1正极活性物质粒子的表面。
此外,在(a)的情况下,也可以具有层叠了具有第1正极活性物质的正极活性物质层和具有第2正极活性物质的正极活性物质层的构造。另外,也可以通过浓度梯度,使第2正极活性物质存在于固体电解质层侧。进而,优选在正极活性物质层的硫化物固体电解质层侧不存在第1正极活性物质。这是为了抑制由于第1正极活性物质和硫化物固体电解质反应而在正极活性物质层和硫化物固体电解质层的界面形成电阻层的现象。
另外,在(b)的情况下,正极活性物质层也可以具有硫化物固体电解质。在该情况下,第1正极活性物质优选为整体连续地被第2正极活性物质包覆。这是为了抑制第1正极活性物质和硫化物固体电解质反应而在正极活性物质层和硫化物固体电解质层的界面形成电阻层的现象。
(2)固体电解质
在本发明中,正极活性物质层可以具有固体电解质层。作为固体电解质,只要是用作全固体电池的固体电解质的固体电解质,则不做特别限定。例如,可以举出Li2O-B2O3-P2O5、以及Li2O-Si2O等氧化系非晶质固体电解质、Li2S-SiS2、LiX-Li2S-SiS2、LiX-Li2S-P2S5、LiX-Li2S-P2O5、LiX-Li2S-Li2O-P2S5、及Li2S-P2S5等硫化物固体电解质、以及LiI、Li3N、Li5La3Ta2O12、Li7La3Zr2O12、Li6BaLa2Ta2O12、Li3PO(4-3/2w)Nw(w<1)、及Li3.6Si0.6P0.4O4等结晶质氧化物/氧氮化物。此外,在此“X”是卤素、特别是I和/或Br。
但是,在正极活性物质层中使用硫化物固体电解质的情况下,正极活性物质优选满足上述(b)。
(3)导电助剂
作为导电助剂,除了气相法碳纤维(VGCF)、乙炔黑、灶黑、碳纳米管(CNT)或者碳纳米纤维(CNF)等碳材料以外,还可以举出镍、铝、不锈钢等金属、或者它们的组合。
(4)粘合剂
作为粘合剂,没有特别限定,可以举出聚合体树脂、例如聚偏氟乙烯(PVDF)、聚四氟乙烯(PTFE)、聚酰亚胺(PI)、聚酰胺(PA)、聚酰胺酰亚胺(PAI)、丁二烯橡胶(BR)、丁苯橡胶(SBR)、腈-丁二烯橡胶(NBR)、苯乙烯-乙烯-丁烯-苯乙烯嵌段共聚物(SEBS)、或者羧甲基纤维素(CMC)等、或者它们的组合。
2.硫化物固体电解质层
硫化物固体电解质层具有硫化物固体电解质以及任意地具有粘合剂。作为硫化物固体电解质,能够使用用作全固体电池的固体电解质的硫化物固体电解质。例如,可以举出Li2S-SiS2、LiX-Li2S-SiS2、LiX-Li2S-P2S5、LiX-Li2S-P2S5、LiX-Li2S-Li2O-P2S5、Li2S-P2S5等。此外,在此“X”是卤素、特别是I和/或Br。
另外,作为粘合剂,能够使用与在正极活性物质层中记载的粘合剂同样的粘合剂。
3.负极活性物质层
负极活性物质层具有负极活性物质,以及任意地具有固体电解质、导电助剂、以及粘合剂。
作为在负极活性物质层中使用的负极活性物质,只要能够吸收/释放锂离子等,则不做特别限定。作为负极活性物质的具体例,可以举出金属例如Li、Sn、Si或者In等、Li和Ti、Mg或者Al的合金、或者碳材料例如硬碳、软碳或者石墨等、或者它们的组合等。特别是,从循环特性以及放电特性的观点来看,钛酸锂(LTO)、含锂合金是优选的。
固体电解质、导电助剂以及粘合剂能够使用与在正极活性物质层中记载的例子同样的例子。
<<本发明的全固体电池的制造方法>>
制造全固体电池的本发明的制造方法是按照正极活性物质层、固体电解质层以及负极活性物质层的顺序具有正极活性物质层、固体电解质层以及负极活性物质层的全固体电池的制造方法,包括如下步骤:制造按照正极活性物质层、固体电解质层以及负极活性物质层的顺序具有正极活性物质层、固体电解质层以及负极活性物质层的全固体电池前驱体,然后进行充放电循环,在该充放电循环中,将所述全固体电池前驱体的温度维持为25℃以上且80℃以下,并且将所述全固体电池前驱体放电至2.1V(vs.Li/Li+)以下。另外,正极活性物质层具有作为第1正极活性物质的LixYyPOz(Y=Ni、Mn和/或Co,0.5≤x≤1.5、0.5≤y≤1.5、2≤z≤7)以及作为第2正极活性物质的Lix’Fey’POz’(0.5≤x’≤1.5、0.5≤y’≤1.5、2≤z’≤7),并且第2正极活性物质配置于所述正极活性物质层的所述硫化物固体电解质层侧和/或所述第1正极活性物质的粒子的表面。
虽然不是通过原理限定,但本发明的作用原理认为如以下所述。
在作为橄榄石型正极活性物质使用了磷酸铁锂的情况下,与电阻层的形成同时,在该电阻层的内侧即该电阻层与橄榄石型正极活性物质的界面,形成从磷酸铁锂脱离作为其构成要素的Fe而得到的包覆层。该包覆层是Fe少的稳定的磷酸的层,与硫化物固体电解质的反应性小。因此,该包覆层具有抑制在电池的充放电时磷酸铁锂与硫化物固体电解质反应的、作为保护层的功能。
另外,本发明人发现了如下情况:在作为橄榄石型正极活性物质使用了磷酸铁锂的情况下,通过反复进行一定条件下的充放电循环,能够容易地去除在正极活性物质和硫化物固体电解质的界面形成的电阻层。另外,本发明人发现了如下情况:即使在包含磷酸铁锂以外的橄榄石型正极活性物质的情况下,由于使磷酸铁锂介于硫化物固体电解质与这些橄榄石型正极活性物质之间,从而能够得到具有高的容量的硫化物固体电池。
作为去除该电阻层的机理,如以下那样考虑。首先,如图5那样,当对使用了作为正极活性物质的磷酸铁锂和硫化物固体电解质的全固体电池进行充电时,在正极活性物质的一次粒子(10)的磷酸铁锂(11)和硫化物固体电解质的界面,形成电阻层(14)。另外,同时,在电阻层(14)与磷酸铁锂(11)之间形成包覆层(12)。认为在使用了LiFePO4和Li2PS4的情况下,该反应如下述的反应式所示(关于LiFePO4以外的磷酸铁锂,也认为引起同样的反应):
FePO4+Li3PS4→FeS2(电阻层)+Li4P2O7(包覆层)+Li+e-
认为通过这样的反应形成具有FeS2的电阻层和具有Li4P2O7的包覆层。另外,该反应是在充放电循环的初始的一个循环或者几个循环中的充电时发生。
之后,在初始的循环的放电时,锂离子与构成该电阻层的FeSx反应。在该反应中,考虑2种反应。一种是锂离子插入到FeSx中而生成LixFeSx的反应。该反应是在约2.5V(vs.Li/Li+)附近发生。另一种是FeSx中的Fe和锂置换而生成Li2S的反应(转换反应)。该反应是在约2.1V(vs.Li/Li+)附近发生。认为这些如下述的2个反应式所示:
FeSx+xLi++xe-→LixFeSx
FeSx+2xLi++2xe-→Li2S+Fe
进而,之后,当反复进行充放电循环时,在放电时FeSx中的Fe和锂置换的反应进一步进展。另外,在充电时由于通过该反应生成的Fe的单体或者化合物成为离子而扩散,从而由FeSx构成的电阻层被破坏。认为这些如下述的2个反应式所示:
Fe→Fex++xe-(充电时)
FeSx+2xLi++2xe-→Li2S+Fe(放电时)
由此,存在于磷酸铁锂和硫化物固体电解质的界面的电阻层被部分性地去除,成为断续的电阻层。另外认为,与此同时,在放电时生成的Li2S扩散到正极活性物质的二次粒子内,在二次粒子内部形成锂离子传导路径。另外,关于电阻层被破坏的部分,由于存在包覆层(12),所以即使充电,磷酸铁锂和硫化物固体电解质也不反应,所以不会新形成电阻层。因此,能够使正极活性物质层中包含的磷酸铁锂以及除了磷酸铁锂以外的橄榄石型正极活性物质作为正极活性物质高效地发挥功能。
通过放电至比作为在磷酸铁锂中引起该反应的电位的约2.1V(vs.Li/Li+)更低,从而能够使FeSx中的铁和锂置换的反应高效地进展。因此,通过进行直至正极活性物质层的电位变为约2.1V(vs.Li/Li+)以下为止进行放电的充放电循环,从而能够制作可去除电阻层且具有高的容量、并且循环特性高的硫化物固体电池。
另外,通过在不仅将放电时的正极活性物质层的电位的下限(以下称为“放电下限电位”),进而将充电时的正极活性物质层的电位的上限(以下称为“充电上限电位”)、充放电速率和/或电池的温度控制为一定的条件的同时进行充放电循环,从而能够更高效地制作具有更高的电池容量的硫化物固体电池。
在电池充电时,电位越高,越多地发生形成电阻层的反应。当电阻层变大时,如果不更多地反复之后的充放电循环,则无法去除电阻层。另外,在高的充电上限电位时,其它副反应也进展,完成后的全固体电池的内部电阻变大。因此,期望通过将充电上限电位保持为一定以下来抑制该副反应。
另外,在减小了充放电速率的情况下,变为引起FeSx中的Fe和锂置换的反应的电位的时间变长。由此,能够使通过一次充放电循环发生的该反应的量增加。因此,通过减小充放电速率,能够减少为了去除电阻层而所需的充放电循环数。
另外,在温度过低的情况下,不易产生过渡金属的硫化物中的过渡金属和锂置换的反应。相反,在温度过高的情况下,虽然反应本身更快地进展,但由于其它副反应而正极活性物质劣化。因此,在充放电循环中,期望温度为预定的范围内。
<全固体电池前驱体>
本发明的制造方法是包括在装配按照正极活性物质层、固体电解质层以及负极活性物质层的顺序具有正极活性物质层、固体电解质层以及负极活性物质层的全固体电池前驱体之后,针对全固体电池前驱体通过下述的条件进行充放电循环的全固体电池的制造方法。
装配全固体电池前驱体的方法没有特别限定,可以举出例如将正极活性物质层、固体电解质层以及负极活性物质层按照其顺序层叠来装配全固体电池前驱体的方法。
此外,正极活性物质层、硫化物固体电解质层以及负极活性物质层的制作方法没有特别限定,能够通过对于本领域技术人员而言公知的任意方法制作。作为制作方法,例如能够如下那样地制作正极活性物质层。
首先,使作为正极活性物质的橄榄石型正极活性物质、导电助剂以及粘合剂等分散到分散介质而制作浆料。之后,通过将该浆料涂覆到金属箔上并使其干燥,得到正极活性物质层用的粉末。通过对该粉末进行冲压,能够得到正极活性物质层。此外,粘合剂不是用于制造正极活性物质层的必须的结构。
另外,可以举出通过将正极活性物质层材料混合到分散介质并涂覆到金属箔并使其干燥来制作的方法。进而,例如能够使用静电喷雾装置对金属基盘上喷雾正极活性物质层材料而形成正极活性物质层。
此外,负极活性物质层以及固体电解质层也能够通过同样的方法制作。
另外,正极活性物质层、硫化物固体电解质层以及负极活性物质层能够具有在上述<<本发明的全固体电池>>中记载的结构,并且能够使用材料来制作。
<充放电循环>
本发明的制造方法包括进行充放电循环的步骤,在该充放电循环中,将全固体电池前驱体维持为25℃以上且80℃以下,直至正极活性物质层的电位变为2.1V(vs.Li/Li+)以下为止进行放电。
放电下限电位可以是2.1V(vs.Li/Li+)以下、2.0V(vs.Li/Li+)以下、1.9V(vs.Li/Li+)以下、1.8V(vs.Li/Li+)以下、1.7V(vs.Li/Li+)以下、1.6V(vs.Li/Li+)以下、或者1.5V(vs.Li/Li+)以下。
另外,在本发明的制造方法的充放电循环中,优选为直至正极活性物质层的电位变为1.6V(vs.Li/Li+)以上且2.1V(vs.Li/Li+)以下的放电下限电位为止进行放电。这是因为,在放电下限电位过高的情况下,电阻层不会被充分地破坏,即使反复进行充放电循环,电池容量也不会增加,相反,如果放电下限电位过低,则由于过放电,正极活性物质层中的电池材料反应,从而预想到容量的减少、内部电阻的上升等正极活性物质层的劣化。
进而,该充放电循环优选满足下述的温度、充放电速率、充电上限电位、放电下限电位和/或充放电循环的次数以及时期的条件。
1.温度
在本发明的制造方法的充放电循环中,优选将全固体电池前驱体的温度保持为25~80℃、特别是40℃~80℃。这是为了通过在充放电循环中将全固体电池前驱体保持于一定的范围内而使得用于破坏在充电时在橄榄石型正极活性物质与固体电解质之间形成的电阻层的反应高效地进展。另外,在温度过低的情况下,用于破坏电阻层的反应不充分地进展,需要反复进行非常多次的充放电循环,效率差。相反,在温度过高的情况下,其它副反应进展,正极活性物质会劣化。
温度的范围既可以是25℃以上、30℃以上、35℃以上、40℃以上、41℃以上、42℃以上、45℃以上、或者50℃以上,也可以是80℃以下、75℃以下、70℃以下、65℃以下、60℃以下、或者55℃以下。为了在使得用于破坏电阻层的反应进展的同时减少副反应,更优选为42℃以上且60℃以下。
2.充放电速率
优选在将充放电速率设为1.0C以下来进行本发明的制造方法的充放电循环。在充放电速率过大的情况下,用于破坏电阻层的反应少,所以需要反复进行非常多次的充放电循环。相反,通过减小充放电速率,能够减少为了去除电阻层而所需的充放电循环数。
充放电速率可以是1.0C以下、0.7C以下、0.5C以下、0.1C以下、0.05C以下、或者0.02C以下。
在充放电速率大的情况下,所需的充放电循环数增加。另一方面,如果速率低,则在一个循环中花费时间。因此,从所需的充放电循环数和在一个循环中所需的时间的平衡来看,充放电速率优选为0.1~0.5C。
3.上限电位
在本发明的制造方法的充放电循环中,优选为直至正极活性物质层的电位变为3.8V(vs.Li/Li+)以上且4.4V(vs.Li/Li+)以下的充电上限电位为止进行充电。这是因为,在充电上限电位过高的情况下,副反应进展,正极活性物质劣化。
充电上限电位既可以是3.8V(vs.Li/Li+)以上、4.0V(vs.Li/Li+)以上、或者4.1V(vs.Li/Li+)以上,也可以是4.4V(vs.Li/Li+)以下、4.3V(vs.Li/Li+)以下、或者4.2V(vs.Li/Li+)以下。
4.充放电循环的次数以及时期
在本发明的制造方法中,将该充放电循环优选进行至少3个循环。这是因为,在初始的充电时形成电阻层,之后,通过反复进行几次循环充放电而破坏电阻层。在3个循环以后,既可以反复进行该充放电循环,也可以不进行充放电而在40℃以上且80℃下保温40小时以上。这是因为,通过在40℃以上且80℃以下进行保温,电阻层被进一步破坏。
另外,也可以不连续地进行该充放电循环,也可以在该充放电循环的之间,插入不同的条件的充放电循环。然而,为了高效地制造本发明的全固体电池,优选为连续地进行该充放电循环。另外,从同样的观点来看,优选为从初始充放电时即从最初起进行该充放电循环。
5.充放电循环的结束时期
在本发明的制造方法中,优选为直至放电容量变得比初次的充放电循环中的放电容量大为止反复进行充放电循环。在本发明的制造方法中,原则上,在初始的充放电循环时,电池的放电容量比上次的充放电循环时小。
这认为是基于下述那样的理由。即,在初始的充放电循环中,在作为正极活性物质的磷酸铁锂和硫化物固体电解质的界面形成电阻层,在放电时被抑制磷酸铁锂和锂离子的反应。然而,在本发明的方法中,当进一步反复进行充放电循环时,该电阻层从磷酸铁锂和硫化物固体电解质的界面被去除,所以每当反复进行循环时,在放电时磷酸铁锂和锂离子的反应量增加。另外,关于此,在放电容量变得比初次的充放电循环时的放电容量大时,可以说电阻层被充分地去除了。
另外,优选为直至在放电时的正极活性物质层的电位中在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处放电平台消失为止,进行充放电循环。电阻层中包含的、由来于橄榄石型正极活性物质的过渡金属的硫化物在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)时与锂离子反应。这表示在该电位的范围中存在放电平台的情况下,引起由来于磷酸铁锂的FeSx和锂离子的反应。即,表示在磷酸铁锂和硫化物固体电解质的界面存在电阻层。
另外,优选为直至在放电时的正极活性物质层的电位中在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处产生放电平台为止,进行充放电循环。磷酸铁锂和锂离子的反应电位存在于3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+),所以在该范围内存在放电平台的情况表示电阻层在磷酸铁锂和硫化物固体电解质的界面被充分地去除了。
3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)的放电平台可以在放电容量为至少10mAh/g~60mAh/g、10mAh/g~80mAh/g、10mAh/g~100mAh/g、10mAh/g~120mAh/g、或者10mAh/g~140m Ah/g的范围内存在。另外,优选为在至少10mAh/g~140mAh/g的范围内存在。这是因为,在该放电平台长时,表示磷酸铁锂和锂离子进一步反应。
此外,在本说明书中,放电平台是指,在表示电压和放电容量的关系的曲线中电压的变化相对放电容量的变化少的平坦的部分。更具体而言,是正极活性物质的每单位重量的相对放电容量(Q)的变化率的电压(V)的变化率(dV/dQ)为-0.010(V/(mAh/g))以上且0.000(V/(mAh/g))以下例如为-0.005(V/(mAh/g))以上且0.000(V/(mAh/g))以下的部分。该电位平台可以是例如-0.005(V/(mAh/g))以上且-0.003(V/(mAh/g))以下。
【实施例】
<<实施例1以及比较例1及2>>
通过下述的方法,制作了实施例1以及比较例1及2的全固体电池。针对这些全固体电池,在下述的条件下,进行了循环伏安测定。
<实施例1>
1.全固体电池的制作
(1)正极活性物质层的制作
在将脱水乙醇和二甘醇丁醚以体积比1:2混合而得到的溶剂中溶解甲醇锂、硝酸钴以及磷酸而制作了正极活性物质层成膜用溶液1。将正极活性物质层成膜用溶液1放置于静电喷雾装置,在施加电压15000V、流速50μl/min以及基盘温度300℃的条件下,在铂基盘上喷雾而形成了薄膜。
针对得到的薄膜,以600℃在大气中实施5小时的退火处理,在作为正极集电体的铂基盘上,制作出作为第1正极活性物质的LiCoPO4的层。
接下来,在将脱水乙醇和二甘醇丁醚以体积比1:2混合而得到的溶剂中溶解甲醇锂、硝酸铁以及磷酸而制作了正极活性物质层成膜用溶液2。将正极活性物质层成膜用溶液2放置于静电喷雾装置,在施加电压15000V、流速50μl/min以及基盘温度200℃的条件下,在形成了LiCoPO4的层的铂基盘上喷雾而形成了薄膜。
针对得到的薄膜,以500℃在大气中实施5小时的退火处理,制作了在形成了LiCoPO4的层的铂基盘上具有作为第2正极活性物质的LiFePO4的层的正极活性物质。
(2)固体电解质层的制作
将作为硫化物固体电解质的75Li2S-25P2S5、粘合剂以及作为分散介质的脱水庚烷充分地混合而制作了固体电解质层用浆料。通过将该固体电解质层用浆料在铝箔上涂覆并使其干燥而制作了固体电解质层。
(3)负极活性物质层的制作
在将脱水乙醇和二甘醇丁醚以体积比1:2混合而得到的溶剂中溶解甲醇锂、硝酸钛以及磷酸而制作了负极活性物质层成膜用溶液。将负极活性物质层成膜用溶液放置于静电喷雾装置,在施加电压15000V、流速50μl/min以及基盘温度300℃的条件下,在作为负极集电体的铂基盘上喷雾而形成了薄膜。
(4)电池的装配
将正极集电体、正极活性物质层、固体电解质层、负极活性物质层以及负极集电体按照其顺序层叠,装配出实施例1的全固体电池。
2.循环伏安测定
在实施例1的全固体电池的负极集电体与正极集电体之间,连接循环伏安测定装置,反复进行15次从0V至2.5V(正极活性物质层的电位从1.6V(vs.Li/Li+)至4.1V(vs.Li/Li+))的充放电循环,进行了循环伏安测定。之后,从0V至4.5V(正极活性物质层的电位从1.6V(vs.Li/Li+)至6.1V(vs.Li/Li+)),进行了循环伏安测定。此外,将CV测定中的扫描速度设为2mV/s。
3.结果/考察
图7A以及图7B示出循环伏安测定的结果。图7A示出了将从0V至2.5V(正极活性物质层的电位从1.6V(vs.Li/Li+)至4.1V(vs.Li/Li+))的充放电循环反复进行了15次的循环伏安测定的结果。图7B示出了15个循环后的循环伏安测定的结果。
如图7A那样,针对实施例1的全固体电池进行了从0V至2.5V的充放电循环的结果为,反复进行充放电循环,并且在1.8V(正极活性物质层的电位是3.4V(vs.Li/Li+))处,还原峰值增大,在0.5V~1.4V(正极活性物质层的电位是2.1V(vs.Li/Li+)~3.0V(vs.Li/Li+))附近,还原峰值减少。认为1.8V附近的还原峰值是由来于锂离子插入到LiFePO4中,0.5V~1.4V附近的还原峰值是由来于电阻层和锂离子的反应。
由此,认为通过进行从0V至2.5V(正极活性物质层的电位从1.6V(vs.Li/Li+)至4.1V(vs.Li/Li+))的充放电循环,在LiFePO4的表面形成的电阻层被破坏。
之后,如图7B那样,确认了当在将从0V至2.5V的充放电循环反复进行15次之后从0V至4.5V进行充放电时,在3.5V附近出现氧化峰值,在2.5V附近出现还原峰值。这些峰值分别表示产生了针对LiCoPO4的锂离子的插入脱离反应。
这样,通过在LiCoPO4的表面层叠LiFePO4,并破坏在LiFePO4表面形成的电阻层,从而能够在硫化物全固体电池中使LiCoPO4动作。
<比较例1>
1.全固体电池的制作
在将脱水乙醇和二甘醇丁醚以体积比1:2混合而得到的溶剂中溶解甲醇锂、硝酸铁、硝酸钴以及磷酸而制作了正极活性物质层成膜用溶液3。将正极活性物质层成膜用溶液3放置于静电喷雾装置,在施加电压15000V、流速50μl/min以及基盘温度300℃的条件下,在铂基盘上喷雾而形成了薄膜。此外,溶解的硝酸铁和硝酸钴是1:4的体积比。
针对得到的薄膜,以600℃在大气中实施5小时的退火处理,在作为正极集电体的铂基盘上,制作出混合了LiFePO4以及LiCoPO4的层。
关于其它条件设为与实施例1同样而制作了比较例1的全固体电池。
2.循环伏安测定
在比较例1的全固体电池的负极集电体与正极集电体之间,连接循环伏安测定装置,将从0V至4.5V(正极活性物质层的电位从1.6V(vs.Li/Li+)至6.1V(vs.Li/Li+))的充放电循环反复进行2次,进行了循环伏安测定。此外,将CV测定中的扫描速度设为2mV/s。
3.结果/考察
图8示出循环伏安测定的结果。如图所示,在具有混合了LiFePO4以及LiCoPO4的层的比较例1的全固体电池的情况下,无法确认电池的动作。认为此原因是在LiCoPO4与硫化物固体电解质接触的部分中产生副反应,在正极活性物质层表面形成了电阻层。
<比较例2>
1.全固体电池的制作
在将脱水乙醇和二甘醇丁醚以体积比1:2混合而得到的溶剂中溶解甲醇锂、硝酸钴以及磷酸而制作了正极活性物质层成膜用溶液4。将正极活性物质层成膜用溶液4放置于静电喷雾装置,在施加电压15000V、流速50μl/min以及基盘温度300℃的条件下,在铂基盘上喷雾而形成了薄膜。
针对得到的薄膜,以600℃在大气中实施5小时的退火处理,在作为正极集电体的铂基盘上,制作了仅具有作为正极活性物质的LiCoPO4的正极活性物质层。
关于其它条件设为与实施例1同样而制作了比较例2的全固体电池。
2.循环伏安测定
在比较例2的全固体电池的负极集电体与正极集电体之间,连接循环伏安测定装置,将从0V至4.5V(正极活性物质层的电位从1.6V(vs.Li/Li+)至6.1V(vs.Li/Li+))的充放电循环反复进行4次,进行了循环伏安测定。此外,将CV测定中的扫描速度设为2mV/s。
3.结果/考察
图9示出循环伏安测定的结果。如图所示,在具有仅具有作为正极活性物质的LiCoPO4的正极活性物质层的比较例2的全固体电池的情况下,即使反复进行一定的充放电循环,也无法确认电池的动作。由此考虑虽然在作为正极活性物质的LiCoPO4与硫化物固体电解质接触的部分产生副反应而在正极活性物质层表面形成了电阻层,但在之后的充放电循环中无法去除电阻层、或者未形成包覆层等的理由。
<<参考例1~17>>
为了研究能够最佳地去除在磷酸铁锂与硫化物固体电解质之间形成的电阻层的条件,如下述那样制作全固体电池,进而在一定的条件下,反复进行了充放电循环。
<全固体电池的制作>
1.正极活性物质层用粉末的制作
对具有作为正极活性物质的碳涂层的LiFePO4、作为导电助剂的气相法碳纤维(VGCF)、作为硫化物固体电解质的Li3PS4-LiI-LiBr、作为分散介质的丁酸丁酯以及作为粘合剂的聚偏氟乙烯(PVDF)进行称量,并充分地混合而制作了正极活性物质层用浆料。将该正极活性物质层用浆料涂覆到铝箔上并使其干燥而得到了正极活性物质层用粉末。
2.负极活性物质层用粉末的制作
对作为负极活性物质的Li4Ti5O12(LTO)、作为导电助剂的VGCF、作为硫化物固体电解质的Li3PS4-LiI-LiBr、作为分散介质的丁酸丁酯以及作为粘合剂的PVDF进行称量,并充分地混合而制作了负极活性物质层用浆料。将该负极活性物质层用浆料涂覆到铝箔上并使其干燥而得到了负极活性物质层用粉末。
3.固体电解质层的制作
将硫化物固体电解质、粘合剂以及作为分散介质的脱水庚烷充分地混合而制作了固体电解质层用浆料。通过将该固体电解质层用浆料涂覆到铝箔上并使其干燥而得到了固体电解质层。
4.电池的装配
冲压固体电解质层,在其上设置称量出预定量的正极活性物质层用粉末,进行冲压而形成了正极活性物质层。将负极活性物质层用粉末称量预定量,进行冲压而形成了负极活性物质层。在正极活性物质层的固体电解质层上层叠负极活性物质层,用夹具约束而装配出全固体电池。
<充放电循环>
针对通过上述方法制作的全固体电池,关于放电下限电位、充电上限电位、充放电速率以及温度,以下述的表1的条件,反复进行了充放电循环。然后,测定了充放电循环中的电池电压和充电容量以及放电容量的关系。以下,将放电容量记载为电池容量。
【表1】
1.表的说明
如表1所示,参考例1~3是将温度、充放电速率以及充电上限电位固定并仅使放电下限电位变化而反复进行了充放电循环的情况。另外,参考例4~7是将温度、充放电速率以及放电下限电位固定并仅使充电上限电位变化而反复进行了充放电循环的情况。另外,参考例8~12是将温度、充电上限电位以及放电下限电位固定并仅使充放电速率变化而反复进行了充放电循环的情况。另外,参考例13~17是将充放电速率、充电上限电位以及放电下限电位固定并仅使温度变化而反复进行了充放电循环的情况。
另外,在表1中,“效果”是指,通过反复进行充放电循环而放电容量是否增加的判断。在“效果”中,“○”是能够增加放电容量的情况,“×”是无法增加放电容量的情况。另外,“△”是虽然通过充放电循环而放电容量增加但副反应的量过多的情况(参考例7)、或者虽然通过反复进行充放电循环而放电容量增加但如果不进行非常多次的循环则放电容量不充分地增加的情况(参考例13)。
另外,在表1中,“图”是表示通过各条件反复进行了充放电循环的情况下的电池电压和充电容量以及电池容量的关系的图。在图10A~图13C中,电压记载了与将LTO用作负极活性物质的情况下的LTO和锂离子反应的电位相对的电位(V(vs.LTO))。相对于此,在本说明书中,希望理解为记载为相对金属锂的析出电位的电位(V(vs.Li/Li+))。关于LTO和锂离子反应的电位(V(vs.LTO)),通过加上1.6V而能够换算为相对金属锂的析出电位的电位(V(vs.Li/Li+))。在图10A~图13C中,在与LTO和锂离子反应的电位相对的电位(V(vs.LTO))下,加上括号记载了相对金属锂的析出电位的电位(V(vs.Li/Li+))。此外,在图10A~图13C中,电池容量是正极活性物质的每单位重量的容量。
2.结果
(1)关于放电下限电位(参考例1~3)
关于参考例1~3,一边将放电下限电位分别维持为1.6V(vs.Li/Li+)、2.1V(vs.Li/Li+)以及2.3V(vs.Li/Li+),一边反复进行了充放电循环。其结果,关于参考例1以及2,虽然在最初的几次循环中电池容量减少,但之后通过进而反复进行充放电直至20个循环,能够得到大的电池容量的全固体电池。相对于此,在参考例3中,即使反复进行充放电循环,电池容量也不增加,无法得到大的电池容量的全固体电池。
在图13A以及B中,在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处充分地存在反应平台。相对于此,在图13C中,虽然在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处看到反应平台,但在反应平台的途中放电结束。认为此现象表示在放电至比作为电阻层的硫化铁和锂离子的反应电位即2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)低的电压的参考例1以及2中,电阻层被充分地破坏,相对于此,在仅放电至2.3V的参考例3中,电阻层未被充分地破坏。
(2)关于充电上限电位(参考例4~7)
关于参考例4~7,针对制作出的全固体电池,将充电上限电位分别设为3.8V(vs.Li/Li+)、4.1V(vs.Li/Li+)、4.4V(vs.Li/Li+)以及4.7V(vs.Li/Li+)而反复进行了充放电循环。其结果,在参考例4~6即将充电上限电位设为3.8~4.4V(vs.Li/Li+)而进行了充放电的情况下,得到了具有160~175mAh/g这样的接近LiFePO4的理论容量的电池容量的全固体电池。相对于此,如参考例7那样,在以4.7V(vs.Li/Li+)反复进行了充放电循环的情况下,得到200mAh/g这样的比LiFePO4的理论容量大的电池容量。
如图12A~12C那样,在将充电上限电位设为3.8~4.4V(vs.Li/Li+)而进行了充放电的参考例4~6的情况下,在最初的几次循环中电池容量减少,并且,在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)附近产生了电位平台。之后,通过反复进行充放电循环,2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)附近的电位平台消失,在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处产生电位平台,电池容量增加。比较图12A~12C,随着充电上限电位变高,直至在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处产生电位平台所需的充放电循环数增加。认为这是因为上限电位越高,越有意地引起副反应。
如图12D那样,在将充电上限电位设为4.7V(vs.Li/Li+)而进行了充放电的参考例7的情况下,与参考例4~6同样地,在最初的几次循环中电池容量减少,之后反复进行充放电循环,从而电池容量增加。然而,在20次循环之后,成为了比LiFePO4的理论容量大的电池容量。另外,3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)的电位平台短。这表示在参考例7中发生了大量的副反应。
(3)关于充放电速率(参考例8~12)
关于参考例8~12,针对制作出的全固体电池,一边将充放电速率分别维持为0.02C、0.05C、0.1C、0.5C.以及1.0C,一边反复进行了充放电循环。其结果,不论在哪一个情况下,都得到了大的电池容量。特别是,在充放电速率是0.5C以下的情况、即参考例8~11的情况下,得到了具有160~175mAh/g这样的、接近LiFePO4的理论容量的电池容量的全固体电池。在将充放电速率设为1.0C而进行的情况、即参考例12的情况下,相比于其它情况,需要更多的充放电循环。然而,能够得到具有约145mAh/g这样的大的电池容量的全固体电池。
如图11B~D那样,在将充放电速率设为0.05C、0.1C以及0.5C而反复进行了充放电循环的参考例9~11的情况下,在最初的几次循环中的放电时,在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处产生电位平台,之后反复进行循环,从而2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)附近的电位平台消失,在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处产生了电位平台。
认为这是因为,在参考例9~11中,在初始的充电时形成的硫化铁的电阻层在最初的几次循环中与锂离子反应而被破坏,通过之后的充放电循环,电阻层从正极活性物质和硫化物固体电解质的界面剥离,从而正极活性物质与锂离子能够充分地反应。
另外,如图11E那样,在将充放电速率设为1.0C而反复进行了充放电循环的参考例12的情况下,在初始的几次循环中在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处产生了电位平台。但是,即使将充放电循环反复很多次,2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)的电位平台也不会消失,电池容量持续减少直至将充放电反复进行14次循环。当进一步进行充放电时,电池容量逐渐上升,2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)附近的电位平台消失,在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处开始产生电位平台。
最终地,在将充放电循环反复进行了81次循环时,电池容量得到了稳定。认为这是因为,充放电速率过大,所以放电所需的时间短,一次循环中的电阻层和锂离子的反应少,所以相比于充放电速率小的情况,经过更多的充放电循环而电阻层被破坏。
相反,如图11A那样,在将充放电速率设为0.02C而反复进行了充放电循环的参考例8的情况下,在最初的放电时在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)附近产生了电位平台。但是,之后,在第2次循环的放电时,2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)附近的电位平台消失,在第3次循环中,在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处产生了电位平台。认为这是因为,由于充放电速率小,所以放电所需的时间长,一次循环中的电阻层和锂离子的反应更多。
(4)关于温度(参考例13~17)
关于参考例14~16,一边将全固体电池的温度分别维持为42℃、60℃以及80℃,一边反复进行了充放电循环。其结果,虽然在最初的3、4次循环中电池容量减少,但之后通过进而反复进行充放电直至20次循环,能够得到大的电池容量的全固体电池。
特别是,关于参考例14,能够实现约165mAh/g这样的接近LiFePO4的理论容量的电池容量,关于参考例15,能够实现175mAh/g这样的接近LiFePO4的理论容量的电池容量。另外,关于参考例16,最终的电池容量约为110mAh/g,虽然比LiFePO4的理论容量小,但能够实现大的电池容量。
如图10B以及图10C那样,在将全固体电池的温度分别维持为42℃以及60℃而反复进行了充放电循环的参考例14以及15的情况下,虽然在最初的3、4次循环中电池容量逐渐减少,但之后通过反复进行充放电循环,电池容量逐渐地增加,在20次循环之后,电池容量约为165~175mAh/g,得到了稳定。
如图10B以及图10C那样,在参考例14以及15中,在最初的3、4次循环中的放电时,在作为硫化铁和锂离子的反应电位的2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处存在电位平台。之后每当反复进行循环时该电位平台逐渐减少,在20次循环之后,在作为LiFePO4的反应电位的3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处形成了电位平台。
认为这是因为,在参考例14以及15中,在初始的充电时形成的硫化铁的电阻层在最初的3或者4次循环中与锂离子反应而被破坏,通过之后的充放电循环,电阻层从正极活性物质和硫化物固体电解质的界面剥离,从而正极活性物质与锂离子能够充分地反应。
另外,在观察图10D时,如参考例16那样,在将全固体电池的温度维持为80℃而反复进行了充放电循环的情况下,与将全固体电池的温度维持为42℃以及60℃而反复进行了充放电循环的情况同样地,在最初的3或者4次循环中,电池容量逐渐地减少,之后通过反复进行充放电循环,电池容量增加并得到了稳定。然而,在温度是80℃的情况下,虽然通过充放电循环的反复而电池容量增加,但最终的电池容量约为110mAh/g,是比以42℃、60℃进行的情况小的值。这认为是,电池的温度高,所以在反复进行充放电循环的过程中,正极活性物质等劣化,电池容量减少。
另外,可知,如图10D所示,在将温度设为80℃的情况下,在2.6V(vs.Li/Li+)~3.4V(vs.Li/Li+)处放电曲线平缓地降低(容量降低),这被推测为产生了副反应。
另一方面,在一边将全固体电池的温度维持为25℃一边反复进行了充放电循环的参考例13中,最终电池容量在140mAh/g下得到了稳定。
如图10A那样,在参考例13的情况下,即使反复进行充放电,在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处也几乎不产生电位平台,每当反复进行充放电循环时,电池容量减少。然而,在14次循环以后,电池容量逐渐开始上升。然后,在66次循环之后,电池的容量增加至约140mAh/g。
这认为是,全固体电池的温度过低,所以在电池充电时在正极活性物质和硫化物固体电解质的界面形成的电阻层几乎不与锂离子反应,在电阻层被破坏之前,需要很多次充放电循环。
在将全固体电池的温度维持为100℃的参考例17中,如图10E那样,在最初的几次循环中在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处产生了电位平台。另外,如果将充放电反复进行4~6次循环,则电池容量增加至约200。然而,即使反复进行充放电,在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处也不产生电位平台,电池容量逐渐减少,最终的电池容量大幅低于LiFePO4的理论容量,降低至约25mAh/g。
这样,在将温度维持为100℃而反复进行了充放电循环的情况下,电池容量一下子增加,这表示在放电时电阻层与锂离子反应,电阻层被破坏一部分。然而,认为温度过高,所以在反复进行充放电循环的过程中,正极活性物质等劣化,电池容量减少。
另外,可知,如图10E所示,在将温度设为100℃的情况下,在2.6V(vs.Li/Li+)~3.4V(vs.Li/Li+)处放电曲线平缓地降低(容量降低),这被推测为产生了副反应。
<<参考例18>>
<电池的装配以及充放电>
与上述<<充放电循环的条件的验证>>的<全固体电池的制作>同样地,装配出全固体电池。针对该全固体电池,将放电下限电位设为2.1V(vs.Li/Li+),将充电上限电压设为4.1V(vs.Li/Li+),将充放电速率设为0.1C,将电池的温度设为60℃,将充放电进行了3次循环。之后,将该全固体电池以80℃保存40小时而制作出了全固体电池。
针对该全固体电池,将放电下限电位设为2.1V(vs.Li/Li+),将充电上限电压设为4.1V(vs.Li/Li+),将充放电速率设为0.1C,将电池的温度设为60℃而进行充放电,测定了其电池容量。
<结果以及考察>
图14是示出该全固体电池的各充放电循环中的电池电压和充电容量以及电池容量的关系的图。
如图所示,在参考例18中,直至最初的3次循环,在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处存在电位平台。然而,之后,在以80℃保存了40小时之后的充放电循环中,在2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)处不存在电位平台,在3.3V(vs.Li/Li+)~3.5V(vs.Li/Li+)处产生了电位平台。另外,电池容量也增加至约160mAh/g。
这样,通过以80℃保存40小时,2.1V(vs.Li/Li+)~2.5V(vs.Li/Li+)的电位平台消失,电池容量增加,认为其理由是,通过初始的3次循环而被破坏的电阻层通过在高温下长时间保存电池而被进一步破坏。
- 还没有人留言评论。精彩留言会获得点赞!