有机光电转换元件、光学面阵传感器、成像器件和成像装置的制作方法
本发明涉及有机光电转换元件、光学面阵传感器、成像器件(imagingdevice)和成像装置。
背景技术:
二维光接收器件广泛地用作成像器件。这种成像器件包括由半导体中二维排列的光电转换部限定的像素,并且通过光电转换在像素中产生的信号作为电荷被传输并且由ccd电路或cmos电路读出。
已知光电二极管,其包括含有有机化合物的光电转换部。
ptl1公开了高灵敏、快速响应的有机光电转换元件,其具有高的光电流与暗电流的s/n比。该有机光电转换元件包括空穴阻挡层,该空穴阻挡层含有富勒烯衍生物和具有5.5ev以上的电离电位的有机化合物。
在ptl1中公开的有机光电转换元件中,由光电转换层产生的空穴未高效率地到达空穴收集电极。因此,该有机光电转换元件有改善的余地。
引用列表
专利文献
ptl1:日本专利公开no.2013-236008
技术实现要素:
本发明提供其中通过光电转换产生的空穴能够高效率地移动至阴极的有机光电转换元件。
根据本发明的一方面,提供有机光电转换元件,其包括阳极、阴极和光电转换部。有机光电转换部包括第一有机化合物层。该有机光电转换元件在该阴极和该光电转换部之间也包括第二有机化合物层。该第二有机化合物层含有具有5.1ev以下的电离电位和2.5ev以上的带隙的有机化合物。
由以下参照附图对例示实施方式的说明,本发明的进一步的特征将变得清楚。
附图说明
图1为根据本发明的实施方式的有机光电转换元件的截面示意图。
图2为表示根据本发明的实施方式的有机光电转换元件的电极之间的能量的图。
具体实施方式
本发明提供有机光电转换元件,其包括阳极、阴极和该阳极与该阴极之间的光电转换部。该光电转换部包括第一有机化合物层,且第二有机化合物层设置在该阴极与该光电转换部之间。在该第二有机化合物层中含有的有机化合物具有5.1ev以下的电离电位和2.5ev以上的带隙。
由于该有机化合物层具有5.1ev以下的电离电位,因此能够高效率地将空穴从光电转换部传输至阴极。而且,由于第二有机化合物层的有机化合物具有2.5ev以上的带隙,因此防止电子从阴极流入光电转换部。
[实施方式]
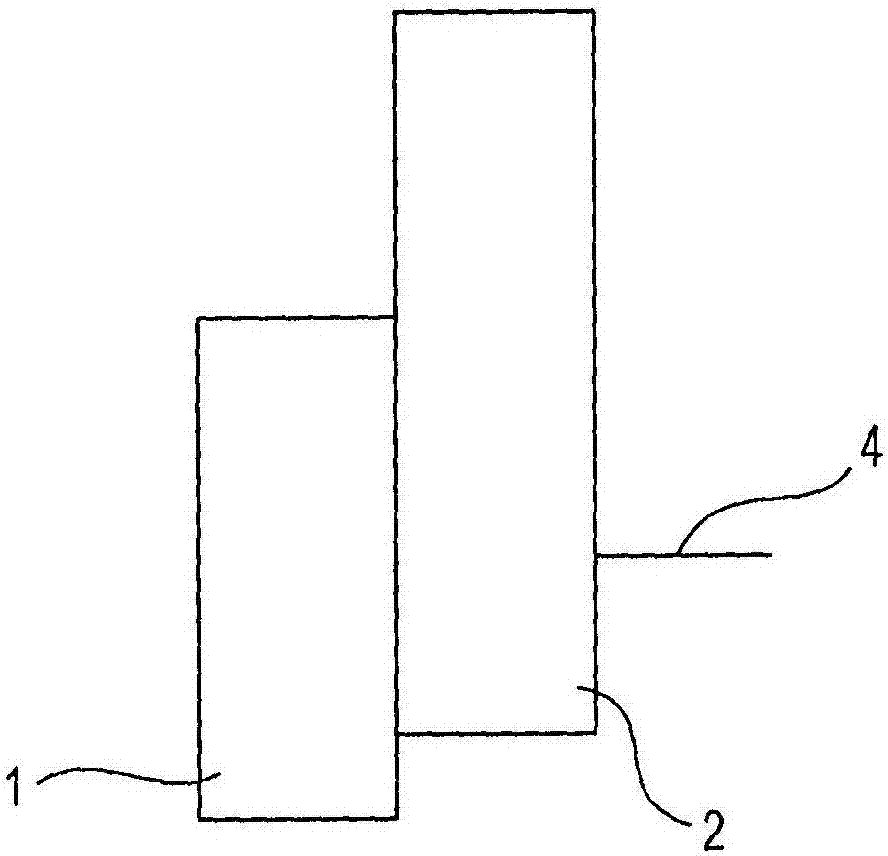
图1为根据本发明的实施方式的有机光电转换元件的截面示意图。该有机光电转换元件在阴极4与阳极5之间包括第一有机化合物层1。第一有机化合物层1用作将光转换为电荷的光电转换部。由于第一有机化合物层意在将光转换为电荷,因此其可被称为光电转换层。
该有机光电转换元件还包括第一有机化合物层与阴极之间的第二有机化合物层2和第一有机化合物层与阳极之间的第三有机化合物层3。
将阳极5连接至读出电路6。读出电路6读取根据由有机转换部产生的电荷的信息并且将该信息传送至例如设置在下游侧的信号处理部(未示出)。读出电路6可连接至阴极。
有机光电转换元件也包括阴极上方的无机保护层7。无机保护层由例如氧化硅、氮化硅、氧化铝等制成。保护层可通过气相沉积、溅射、ald(原子层沉积)等形成。
在无机保护层上设置滤色器8。滤色器可以透射可见光的红光。如果配置多个有机光电转换元件,则可设置多个滤色器,为每个有机光电转换元件设置一个。或者,可由多个有机光电转换元件分享单一的滤色器。可将滤色器例如以bayer阵列排列。
在滤色器上设置微透镜9。微透镜将入射光聚焦在有机光电转换元件上。如果配置多个有机光电转换元件,则可设置多个微透镜,为每个有机光电转换元件设置一个。或者,可由多个有机光电转换元件分享单一的微透镜。
对于有机光电转换元件中的光电转换,优选在阴极与阳极之间施加电压。该电压优选在0.5v至15v的范围内。
图2为根据本发明的实施方式的有机光电转换元件的能量图。图2只示出阴极4、第一有机化合物层1和第二有机化合物层2,省略了其他部件或构件。图2中,由附图标记4表示的线表示阴极的功函数的能级。对于由附图标记1和2表示的矩形,竖直方向上的长度表示对应的有机化合物层中含有的有机化合物的带隙;矩形的底边的位置表示有机化合物的电离电位;矩形的顶边的位置表示电子亲和势。
如果任意有机化合物层含有多种有机化合物,则示出以最高比例含有的有机化合物的能量。
图2中,位置越低,则能量越高。而且,矩形的竖直方向上的长度越大,则带隙越宽。
优选地,第二有机化合物层的有机化合物具有比第一有机化合物层的有机化合物低的电离电位。在这种状况下,空穴能够高效率地从第一有机化合物层移动至阴极。
更具体地,优选第二有机化合物层中的有机化合物的电离电位比第一有机化合物层中的有机化合物的电离电位低0.5ev以上。而且,优选第二有机化合物层中的有机化合物的电离电位高于阴极的功函数。
因此,优选第二有机化合物层中的有机化合物的电离电位高于阴极的功函数并且低于第一有机化合物层中的有机化合物的电离电位。
优选地,第二有机化合物层中的有机化合物具有比第一有机化合物层中的有机化合物低的电子亲和势。在这种状况下,能够防止电子从阴极流入第一有机化合物层。更具体地,优选第二有机化合物层中的有机化合物的电子亲和势比第一有机化合物层中的有机化合物的电子亲和势低0.5ev以上。而且,优选第二有机化合物层中的有机化合物的电子亲和势比阴极的功函数低1.0ev以上。
优选地,第二有机化合物层中的有机化合物耐水。这是因为,将第二有机化合物层设置得比第一有机化合物层更接近外部,因此更易于受到从外部进入的湿气的影响。更具体地,优选第二有机化合物层中的有机化合物不易溶于水或不易与水反应。
第二有机化合物层中的有机化合物比ptl1中公开的空穴阻挡层中含有的有机化合物更耐水。
能够根据下述程序对有机化合物的耐水性进行估测。在气相沉积装置的真空室中5×10-3pa下使用电阻加热通过真空沉积在硅基板上将有机化合物层形成至50nm以上的厚度。将水滴到有机化合物层上并且使其静置10分钟。
然后,在滴水后10分钟测定有机化合物层的厚度。于是通过比较滴水前后的厚度,能够估测耐水性。能够使用例如由kla-tencor制造的仪器p-16测定此时的厚度的减少率。使用液滴痕迹的两端处两点的测定值的平均来计算厚度的减少率。
耐水性有机化合物层的厚度的减少率优选在0%-50%的范围内,更优选在0%-30%的范围内,例如在0%-10%的范围内。
或者,可代替测定厚度的减少率而测定水滴与有机化合物层的接触角来估测耐水性。能够采用已知方法测定接触角。例如,可使用例如接触角计dropmaster700和分析软件程序famas(均由kyowainterfacescience制造)来测定接触角。
与耐水性有机化合物层的接触角优选在50°-120°的范围内,例如在70°-100°的范围内。
有机化合物层的高耐水性暗示有机化合物层中的有机化合物耐水。即使将水滴到其上,耐水性有机化合物层也不太可能在有机化合物层的表面轮廓上发生改变。因此,水滴的接触角大或者厚度的减少率低。
优选地,第二有机化合物层含有选自由亚咪唑基(imidazolidene)衍生物、亚苯并咪唑基(benzoimidazolidene)衍生物和亚吖啶基(acridinylidene)衍生物组成的组中的至少一种。
第二有机化合物层可与阴极接触。
能够根据下述程序来测定电离电位。
在真空室中5×10-3pa下使用电阻加热通过真空沉积在al/nd基板上形成有机化合物层。优选地,将该层沉积至约150nm-200nm的范围内的厚度。然后,使用大气光电子能谱仪例如由rikenkeiki制造的ac-2测定得到的层的电离电位。
能够根据下述程序测定带隙。
在真空室中5×10-3pa下使用电阻加热通过真空沉积在al/nd基板上形成有机化合物层。优选地,将该层沉积至约150nm-200nm的范围内的厚度。为了测定带隙,使用紫外-可见分光光度计等测定吸收光谱。由吸收光谱的吸收边缘确定带隙。紫外-可见分光光度计可以是例如由jascocorporation制造的v-560。
[有机光电转换元件的结构]
根据本发明实施方式的有机光电转换元件的第一有机化合物层意在接收光并且根据光量来产生电荷。由于其功能,第一有机化合物层可被称为光电转换层。第一有机化合物层可含有多种有机化合物。
当第一有机化合物层含有多种有机化合物时,多种有机化合物的混合物可形成单一层,或者多种有机化合物可形成包括多个层的多层组成。
如果多种有机化合物形成多层复合物,则优选在从阳极至阴极的方向上形成复合层。
优选地,第一有机化合物层含有p型有机半导体或n型有机半导体。更优选地,第一有机化合物层至少部分地具有含有p型有机化合物和n型有机化合物的混合物的本体异质层(混合层)。
第一有机化合物层的本体异质层能够增加光电转换元件的光电转换效率(灵敏度)。本体异质层以最佳比例含有有机化合物时,使第一有机化合物层中的电子和空穴的迁移率增加,因此能够使有机光电转换元件的光学响应速度增加。
优选地,第一有机化合物层含有富勒烯或富勒烯衍生物作为n型有机半导体。第一有机化合物层中的富勒烯或富勒烯衍生物的分子链限定了电子的路径并因此增加电子传输性,从而增加有机光电转换元件的光学响应速度。富勒烯或富勒烯衍生物含量优选在40体积%-85体积%的范围内,相对于光电转换层或第一有机化合物层中的材料的总体积。
例示性富勒烯或富勒烯衍生物包括富勒烯c60、富勒烯c70、富勒烯c76、富勒烯c78、富勒烯c80、富勒烯c82、富勒烯c84、富勒烯c90、富勒烯c96、富勒烯c240、富勒烯540、混合富勒烯和富勒烯纳米管。
富勒烯衍生物为具有取代基的富勒烯。取代基可以是烷基、芳基、杂环基等。
第一有机化合物层中可含有的p型有机半导体能够用作有机半导体给体,并且典型地为空穴传输、给电子有机化合物。更具体地,p型有机半导体是一种比另一种电离电位低的两种有机化合物中的一种。
能够在第一有机化合物层中使用的p型有机半导体的实例包括三芳基胺化合物、吡喃化合物、喹吖啶酮化合物、联苯胺化合物、吡唑啉化合物、苯乙烯基胺化合物、腙化合物、三苯基甲烷化合物、咔唑化合物、聚硅烷化合物、噻吩化合物、酞菁化合物、菁化合物、部花青化合物、oxonol化合物、多胺化合物、吲哚化合物、吡咯化合物、吡唑化合物、聚亚芳基化合物、稠合芳烃(萘衍生物、蒽衍生物、菲衍生物、并四苯衍生物、芘衍生物、苝衍生物、荧蒽衍生物)、和具有含氮杂环化合物作为配体的金属络合物。这些中,优选为三芳基胺化合物、吡喃化合物、喹吖啶酮化合物、吡咯化合物、酞菁化合物、部花青化合物和稠合芳烃。
荧蒽衍生物是在其化学结构中具有荧蒽骨架的化合物。类似地,萘衍生物、蒽衍生物、菲衍生物、并四苯衍生物、芘衍生物和苝衍生物是各自在其化学结构中具有对应的化合物骨架的化合物。
优选地,第一有机化合物层不发光。更具体地,“不发光”意味着该层在可见波长区域(400nm-730nm)中具有1%以下、优选0.5%以下、例如0.1%以下的发光量子效率。如果光电转换部的发光量子效率超过1%,则将有机光电转换元件应用于传感器或成像器件时对感测性能或成像性能产生不利影响。
根据本发明实施方式的有机光电转换元件可进一步包括在阳极与第一有机化合物层之间的第三有机化合物层。第三有机化合物层意在防止空穴从阳极进入第一有机化合物层并且优选具有高电离电位。
根据实施方式的有机化合物层可包括基板。基板可以是硅基板、玻璃基板、柔性基板等。
有机光电转换元件的阴极是收集光电转换部中产生的电荷的空穴的电极。阴极可由导电性透明材料制成。在将阴极设置在有机光电转换元件的光进入侧附近的结构中,优选阴极是光学透明的。阴极可被称为空穴收集电极或负电极。
阴极材料的实例包括金属、金属氧化物、金属氮化物、金属硼化物、有机导电性化合物及其混合物。更具体地,阴极材料包括金属单质,例如金、铂、银、铜、镍、钯、钴、硒、钒、钨、铝、钛和锰;这些金属单质的混合物或合金;锑掺杂或氟掺杂的氧化锡(ato、fto);导电性金属氧化物,例如氧化锡、氧化锌、氧化铟、氧化铟锡(ito)和氧化铟锌(izo);无机导电性化合物,例如碘化铜和硫化铜;有机导电性材料,例如聚苯胺、聚噻吩和聚吡咯;和包括有机导电性材料层和ito或氮化钛层的复合物。
有机光电转换元件的阳极是收集光电转换部中产生的电荷的电子的电极。在将阳极设置在有机光电转换元件的光进入侧的结构中,优选阳极是光学透明的。阳极可被称为电子收集电极或正电极。
阴极材料的实例包括金属、金属氧化物、金属氮化物、金属硼化物、有机导电性化合物及其混合物。更具体地,阴极材料包括金属单质,例如金、铂、银、铜、镍、钯、钴、硒、钒、钨、铝、钛和锰;这些金属单质的混合物或合金;锑掺杂或氟掺杂的氧化锡(ato、fto);导电性金属氧化物,例如氧化锡、氧化锌、氧化铟、al掺杂的氧化锌(azo)、氧化铟锡(ito)、氧化铟锌(izo)和tio2;无机导电性化合物,例如碘化铜和硫化铜;有机导电性材料,例如聚苯胺、聚噻吩和聚吡咯;和包括有机导电性材料层和ito或氮化钛层的复合物。
与读出电路连接的阳极和阴极中的一者可被称为像素电极。
如果将包括绝缘层的电容器元件设置在阳极与阴极之间,则阳极和阴极可被分别称为像素电极和对电极。
如果任一电极由ito制成,则ito电极能够采用电子束法、溅射、电阻加热气相沉积、化学反应法(例如,溶胶-凝胶法)、用氧化铟锡分散体的涂布等形成。可对得到的ito电极进行uv-臭氧处理、等离子体处理等。如果任一电极由tin制成,则tin电极能够通过反应性溅射或任何其他方法形成,并且可对得到的tin电极进行退火、uv-臭氧处理、等离子处理等。
根据本发明的实施方式的光电转换元件的有机化合物层可含有由通式(1)-(6)的任一个表示的有机化合物:
[化1]
式(1)中,r1-r4各自表示选自由取代或未取代的苯基、取代或未取代的苄基、取代或未取代的联苯基、取代或未取代的萘基、取代或未取代的菲基、取代或未取代的芴基、取代或未取代的苯并[9,10]菲基、取代或未取代的二苯并呋喃基和取代或未取代的二苯并噻吩基组成的组中的基团。
r5-r12各自表示氢原子或者选自由具有1-4的范围内的碳数的烷基和取代或未取代的芳基组成的组中的基团。
芳基可具有碳数在1-4的范围内的烷基作为取代基。
[化2]
式(2)中,r1-r4各自表示选自由取代或未取代的苯基、取代或未取代的联苯基、取代或未取代的萘基、取代或未取代的菲基、取代或未取代的芴基、取代或未取代的苯并[9,10]菲基、取代或未取代的二苯并呋喃基和取代或未取代的二苯并噻吩基组成的组中的基团。
[化3]
式(3)中,x1和x2各自表示芳基。该芳基可具有卤素原子或烷基。r1-r16各自表示氢原子或选自由卤素原子、烷基和芳基组成的组中的取代基。
[化4]
式(4)中,r1-r28各自表示氢原子或者选自由卤素原子、具有1-8的范围内的碳数的烷基和取代或未取代的芳基组成的组中的取代基。
[化5]
式(5)中,ar1-ar4各自表示取代或未取代的稠环。
r1-r8各自表示氢原子或者选自由卤素原子、具有1-8的范围内的碳数的烷基和取代或未取代的芳基组成的组中的取代基。
[化6]
通式(6)中,ar1-ar4各自表示取代或未取代的杂单环基团。
r1-r8各自表示氢原子或者选自由卤素原子、具有1-8的范围内的碳数的烷基和取代或未取代的芳基组成的组中的取代基。
通式(1)-(6)中的卤素原子包括氟、氯、溴和碘。优选氟。
优选地,上述通式中的烷基具有1-8的范围内的碳数。具有1-8的范围内的碳数的烷基的实例包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基和正辛基。
芳基的实例包括苯基、萘基、菲基、
稠环的实例包括萘基、茚基、菲基、蒽基、芘基、芴基、喹啉基、异喹啉基、氮杂菲基、菲咯啉基(phenanthronyl)、苯并噻吩基、二苯并噻吩基、苯并呋喃基和二苯并呋喃基。
这些稠环中,萘基、茚基、菲基、蒽基、芘基和芴基为全部由氢和碳组成的烃。
另一方面,喹啉基、异喹啉基、氮杂菲基、菲咯啉基(phenanthronyl)、苯并噻吩基、二苯并噻吩基、苯并呋喃基和二苯并呋喃基为均含有杂原子的稠环。优选地,稠环各自全部由氢和碳组成。
每个杂单环基团可以是包括碳和氮原子的6元芳环或者包括碳原子、和氮、硫和氧原子中的任意原子的5元环。更具体地,杂单环基团的实例包括吡啶基、吡嗪基(pyrazyl)、嘧啶基、pyrididazoyl、三嗪基(triazyl)、吡咯、呋喃基、噻吩基、咪唑、吡唑、噁唑、噻唑、咪唑啉和噻嗪。
如果通式(1)-(6)的上述基团具有取代基,则该取代基选自由卤素原子、烷基和芳基组成的组。这种情况下,卤素原子优选为氟。烷基优选具有1-8的范围内的碳数。芳基优选为苯基、萘基、菲基、
以下示出由通式(1)表示的有机化合物的实例。
[化7]
[化8]
以下示出由通式(2)表示的有机化合物的实例。
[化9]
以下示出由通式(3)表示的有机化合物的实例。
[化10]
[化11]
[化12]
以下示出由通式(4)表示的有机化合物的实例。
[化13]
[化14]
[化15]
[化16]
[化17]
以下示出由通式(5)表示的有机化合物的实例。
[化18]
[化19]
[化20]
以下示出由通式(6)表示的有机化合物的实例。
[化21]
[化22]
[化23]
[化24]
[通式(1)-(6)的有机化合物的合成方法]
在“journalofamericanchemicalsociety,1964,86(12),第2518-2519页”中由davidm.lemal公开了通式(1)的有机化合物的合成方法。通过适当地替换公开的方法中使用的试剂,能够合成各种由通式(1)表示的有机化合物。
在“organicsyntheses,coll.第5卷,第115页(1973)和第47卷,第14页(1967)”中由h.w.wanzlick公开了通式(2)的有机化合物的合成方法。通过适当地替换公开的方法中使用的试剂,能够合成各种由通式(2)表示的有机化合物。
[通式(3)的有机化合物的合成方法]
通式(3)的有机化合物可通过例如下述方法合成。
[化25]
通过适当地替换与r1-r4、x1和x2对应的试剂,能够合成各种由通式(3)表示的有机化合物。例如,通过下述方案合成了通式(3)的例示化合物a-1。
[化26]
(1)化合物b-13的合成
首先,在200ml三颈烧瓶中装入下述试剂:
化合物b-11:1.50g(7.68mmol)
化合物b-12:2.41g(15.36mmol)
叔丁醇钠:1.47g(15.36mmol)
然后,在添加100ml的氯苯后,在氮气氛中室温下搅拌的同时将155mg的三叔丁基膦添加到该混合物中。随后,添加86mg的醋酸钯。加热到131℃后,在该温度(131℃)下将该反应液搅拌5小时以反应。反应完成后,添加100ml的水,并且用氯仿萃取有机相。然后,用无水硫酸钠干燥有机相,随后在减压下浓缩以得到粗产物。通过硅胶柱(甲苯+乙酸乙酯混合洗脱剂)将粗产物纯化以得到1.31g(收率63%)的白色固体的化合物b-13。
(2)例示化合物a-1的合成
在50ml三颈烧瓶中装入30ml的丙酮。用氩气对丙酮进行冒泡15分钟。然后,将下述试剂添加到烧瓶中:
化合物b-13:271mg(1.0mmol)
锌粉末:1.30g(20.0mmol)
随后,将反应液加热到50℃,然后在该温度(50℃)下搅拌30分钟。在用冰冷却反应液的同时历时30分钟的时间添加12.0ml的浓盐酸。然后,在室温下将反应液搅拌20小时以反应。反应完成后,添加30ml的水,并且通过过滤将得到的黄色固体沉淀物分离出。用水对分离的固体进行冲洗。于是,得到了177mg(收率:69%)的黄色固体的例示化合物a-1。
[通式(4)的有机化合物的合成方法]
通式(4)的有机化合物可通过例如下述方案合成。
[化27]
通过适当地替换与r1和r2对应的试剂,能够合成各种由通式(4)表示的有机化合物。例如,通过下述方案合成了通式(4)的例示化合物a1。
(1)化合物e3的合成
[化28]
将下述化合物和溶剂添加到100ml回收烧瓶中:
e1:2.36g(10.0mmol)
e2:2.33g(21.0mmol)
醋酸钯:67mg(0.3mmol)
三叔丁基膦:0.17ml(0.7mol)
叔丁醇钠:2.31g(24.0mmol)
甲苯:50ml
在搅拌下将得到的溶液加热回流历时8小时。反应完成后,添加水以分离。通过硅胶柱色谱(洗脱剂:庚烷/氯仿=3/1)对反应产物进行纯化以得到2.34g(收率:79%)的化合物e3。
(2)化合物e4的合成
[化29]
将下述化合物和溶剂添加到100ml回收烧瓶中:
化合物e3:1.48g(5.00mmol)
原甲酸三乙酯:25ml
向得到的溶液中添加0.5ml的12n盐酸,并且将混合物搅拌5分钟。然后,添加0.05ml的甲酸,并且在搅拌下将混合物在80℃下加热4小时。反应完成后,在减压下将原甲酸三乙酯除去。然后,将得到的产物溶解于氯仿中并且通过硅胶柱色谱(洗脱剂:氯仿/甲醇=20/1)纯化以得到1.20g(收率:70%)的化合物e4。
(3)例示化合物a1的合成
[化30]
在氮气流中,将下述化合物和溶剂添加到100ml回收烧瓶中:
e4:342mg(1.00mmol)
脱水thf:20ml
向得到的溶液中添加48mg(2.00mmol)的氢化钠,并且将混合物搅拌2分钟。然后,添加1mg(0.01mmol)的tbuok,并且在搅拌下将混合物在80℃下加热10小时。反应完成后,添加20ml的脱水甲苯并且通过才利特(celite)过滤样品。将滤液浓缩以得到粉末。通过在脱水己烷中分散来对粉末进行清洗并且过滤以得到160mg(收率:52%)的黄色粉末的例示化合物a1。
使用由bruker制造的autoflexlrf对得到的化合物进行基质辅助激光解吸/电离飞行时间质谱(maldi-tof-ms)。
测定值:m/z=612.38;计算值:612.19
使用ag/ag+参比电极、pt对电极和玻璃碳工作电极,在四丁基高氯酸铵在n,n-二甲基甲酰胺中的0.1m溶液中进行cv测定。电位扫描速率为0.5v/s。
对于该测定,使用了由als制造的电化学分析仪model660c。氧化电位为-0.85v。
[通式(5)的有机化合物的合成方法]
通式(5)的有机化合物可通过例如下述方法合成。
[化31]
通过适当地替换与r1和r2对应的试剂,能够合成各种由通式(5)表示的有机化合物。
例如,通过下述方案合成了通式(5)的例示化合物a2。
(1)化合物e3的合成
[化32]
将下述化合物和溶剂添加到100ml回收烧瓶中:
e11:1.36g(10.0mmol)
e15:4.35g(21.0mmol)
三(二亚苄基丙酮)二钯(0):274mg(0.3mmol)
2-二环己基膦基-2',4',6'-三异丙基联苯:333mg(0.7mmol)
叔丁醇钠:2.31g(24.0mmol)
甲苯:50ml
在搅拌下将得到的溶液加热回流8小时。反应完成后,通过才利特过滤反应混合物,然后通过添加水进行分离。通过硅胶柱色谱(洗脱剂:庚烷/氯仿=3/1至2/1)将分离的反应产物纯化以得到2.53g(收率:65%)的化合物e3。
(2)化合物e4的合成
[化33]
将下述化合物和溶剂添加到100ml回收烧瓶中:
e27:1.94g(5.00mmol)
原甲酸三乙酯:50ml
向得到的溶液中添加0.8ml的12n盐酸,并且将混合物搅拌5分钟。然后,添加0.05ml的甲酸,并且在搅拌下将混合物在80℃下加热4小时。反应完成后,将20ml的二乙醚添加到冷却的反应混合物中。通过过滤收集沉淀的晶体。用二乙醚清洗后,在减压下120℃下将晶体干燥以得到1.73g(收率:80%)的化合物e28。
(3)例示化合物a2的合成
[化34]
在氮气流中,将下述化合物和溶剂添加到100ml回收烧瓶中:
e4:435mg(1.00mmol)
脱水dmf:5ml
用氮气对得到的溶液进行脱气后,添加96mg(4.00mmol)的氢化钠,并且将混合物搅拌2分钟。然后,添加44mg(0.4mmol)的tbuok,并且在搅拌下将混合物在30℃下加热24小时。反应完成后,在搅拌下将用氮气进行了脱气的10ml的水逐渐添加到样品中以使反应产物沉淀,然后使用注射器将溶剂除去。在将添加用氮气进行了脱气的10ml的水、然后使用注射器除去溶剂的操作进行两次后,添加10ml的经脱气的己烷,清洗样品并且用超声波分散。然后,通过膜滤器进行过滤来收集反应产物,并且用己烷清洗以得到267mg(收率:67%)的黄色粉末的例示化合物a2。
使用由bruker制造的autoflexlrf对得到的化合物进行基质辅助激光解吸/电离飞行时间质谱(maldi-tof-ms)。
测定值:m/z=796.33;计算值:796.36
使用ag/ag+参比电极、pt对电极和玻璃碳工作电极,在四丁基高氯酸铵在n,n-二甲基甲酰胺中的0.1m溶液中进行cv测定。电位扫描速率为0.5v/s。
对于该测定,使用了由als制造的电化学分析仪model660c。氧化电位为-0.98v。
[通式(6)的有机化合物的合成方法]
[化35]
通过适当地替换与r1和r2对应的试剂,能够合成各种由通式(6)表示的有机化合物。例如,通过下述方案合成了通式(6)的例示化合物a2。
(1)化合物e3的合成
[化36]
将下述化合物和溶剂添加到100ml回收烧瓶中:
e1:1.36g(10.0mmol)
e2:3.30g(21.0mmol)
三(二亚苄基丙酮)二钯(0):274mg(0.3mmol)
2-二环己基膦基-2',4',6'-三异丙基联苯:333mg(0.7mmol)
叔丁醇钠:2.31g(24.0mmol)
甲苯:50ml
在搅拌下将得到的溶液加热回流8小时。反应完成后,通过才利特过滤反应混合物,然后通过添加水来进行分离。通过硅胶柱色谱(洗脱剂:庚烷/氯仿=3/1至2/1)将分离的反应产物纯化以得到1.77g(收率:61%)的化合物e3。
(2)化合物e4的合成
[化37]
将下述化合物和溶剂添加到100ml回收烧瓶中:
e27:1.45g(5.00mmol)
原甲酸三乙酯:50ml
向得到的溶液中添加0.8ml的12n盐酸,并且将混合物搅拌5分钟。然后,添加0.05ml的甲酸,并且在搅拌下将混合物在80℃下加热4小时。反应完成后,将20ml的二乙醚添加到冷却的反应混合物中。通过过滤收集沉淀的晶体。用二乙醚清洗后,在减压下120℃下将晶体干燥以得到1.51g(收率:90%)的化合物e4。
(3)例示化合物a2的合成
[化38]
在氮气流中,将下述化合物和溶剂添加到100ml回收烧瓶中:
e4:336mg(1.00mmol)
脱水dmf:5ml
用氮气对得到的溶液脱气后,添加96mg(4.00mmol)的氢化钠,并且将混合物搅拌2分钟。然后,添加了44mg(0.4mmol)的tbuok,并且在搅拌下将混合物在30℃下加热24小时。反应完成后,在搅拌下将用氮气进行了脱气的10ml的水逐渐添加到样品中以使反应产物沉淀,然后使用注射器将溶剂除去。在将添加用氮气进行了脱气的10ml的水、然后使用注射器除去溶剂的操作进行两次后,添加10ml的经脱气的己烷,清洗样品并且用超声波分散。然后,通过膜滤器进行过滤来收集反应产物,并且用己烷清洗以得到210mg(收率:77%)的黄色粉末的例示化合物a2。
使用由bruker制造的autoflexlrf对得到的化合物进行基质辅助激光解吸/电离飞行时间质谱(maldi-tof-ms)。
测定值:m/z=600.29;计算值:600.27
使用ag/ag+参比电极、pt对电极和玻璃碳工作电极,在四丁基高氯酸铵在n,n-二甲基甲酰胺中的0.1m溶液中进行cv测定。电位扫描速率为0.5v/s。
对于该测定,使用了由als制造的电化学分析仪model660c。氧化电位为-0.74v。
[包括有机光电转换元件的成像器件]
通过替换第一有机化合物层中使用的有机化合物,能够制备用于具有不同颜色的光的另一有机光电转换元件。用于具有不同颜色的光的有机光电转换元件意味着该元件将与由其他光电转换元件光电转换的光不同的波长范围中的光转换。
本发明实施方式的有机光电转换元件可用于光学面阵传感器。该光学面阵传感器包括多个有机光电转换元件,该有机光电转换元件以由行和列限定的二维阵列配置。在该结构中,有机光电转换元件各自产生电荷并且独立地输出电荷,因此光学面阵传感器提供表示在特定的受光区域中光强度的分布的信息。
光学面阵传感器的多个有机光电转换元件的每一个可设置有能够将具有不同颜色的光转换为电能的附加的光学光电转换元件。将该附加的有机光电转换元件设置在另一有机光电转换元件上。该附加的有机光电转换元件对具有与由另一有机光电转换元件转换的光不同的波长的光进行光电转换。
本发明实施方式的有机光电转换元件可用于成像器件。该成像器件包括多个像素和信号处理部。将该多个像素以包括多个行和多个列的矩阵方式配置。该结构中的每个像素输出信号以提供图像信号。
在该成像器件中,每个像素包括至少一个有机光电转换元件。
该像素可包括与有机光电转换元件连接的读出电路。该读出电路包括晶体管,该晶体管输出例如根据有机光电转换元件中产生的电荷的信号。
该像素可进一步包括能够光电转换具有与由另一有机光电转换元件转换的光不同颜色的光的附加的有机光电转换元件。将该附加的有机光电转换元件设置在另一有机光电转换元件上。该附加的有机光电转换元件光电转换具有与由另一有机光电转换元件转换的光不同的波长的光。将这两种有机光电转换元件组合时,成像器件不需要滤色器。
该像素可包括多个有机光电转换元件。这样的结构使得能够在成像表面上进行相位差自动聚焦。多个像素中的两个以上可共用读出电路。
该成像器件可包括波长选择部。该波长选择部可以是滤色器。将该滤色器设置在光进入侧的附近。对于用于特定颜色的有机光电转换元件,优选滤色器透射具有特定颜色的光。特定颜色是指特定波长范围内的光。成像器件中,可设置多个滤色器,为每个像素设置一个,或者可由多个像素共用单一的滤色器。
或者,该波长选择部可以是将具有特定波长的光分离出的棱镜。
该成像器件可包括微透镜。将该微透镜设置在光进入侧的附近并且适于收集入射到光电转换部的光。可设置多个微透镜,为每个像素设置一个,或者可由多个像素共用单一的微透镜。
将本发明实施方式的有机光电转换元件用于成像器件时,可将滤光器设置在成像器件的光进入侧的附近。该滤光器可以是低通滤波器、能够将波长低于或等于紫外线的波长的光除去的uv截止滤波器或者能够除去红外线的ir截止滤波器。由于该滤光器减少扰音,因此该成像器件能够形成高质量图像。
本发明实施方式的有机光电转换元件可用于成像装置。该成像装置包括具有多个透镜的成像光学系统和能够接收已通过该成像光学系统的光的成像器件。或者,该成像装置包括能够与成像光学系统连接的联接部、和成像器件。
更具体地,该成像装置可以是数码相机(digitalcamera)或数字静态照相机(digitalstillcamera)。
该成像装置可进一步包括适于接收来自外部的信号的接收器。将接收器接收的信号用于至少控制成像装置的成像范围、成像起点和成像终点。该成像装置可进一步包括适于将得到的图像传送到外部的传送器。以有线方式或无线方式进行该传送。对于无线传送,可使用已知的通信系统例如wi-fi或bluetooth(注册商标)。
接收器和传送器的存在能够使该成像装置用作网络照相机。
[有机化合物的电离电位的测定]
根据下述程序测定由通式(1)表示的例示化合物a1的电离电位。
在真空室中5×10-3pa下使用电阻加热通过真空沉积在al/nd基板上形成有机化合物的层。将该有机化合物层形成至150nm-200nm的厚度。使用大气光电子能谱仪(由rikenkeiki制造的ac-2)测定得到的层的电离电位。
[有机化合物的带隙的测定]
根据下述程序测定由通式(1)表示的例示化合物a1的带隙。
在真空室中5×10-3pa下使用电阻加热通过真空沉积在al/nd基板上形成有机化合物的层。将该有机化合物层形成至150nm-200nm的厚度。
使用紫外-可见分光光度计(由jascocorporation制造的v-560)测定该有机化合物层的吸收光谱。由该吸收光谱的吸收边缘确定带隙。
[耐水性的测定]
通过气相沉积在硅基板上由例示化合物a3形成50nm厚的有机化合物层。
将水滴到得到的有机化合物层上并且使其静置10分钟。但是,有机化合物层的厚度没有减少。这表明厚度的减少率为1%以下。确认例示化合物a3具有高耐水性。
根据本发明,提供通过光电转换产生的空穴能够高效率地移动到阴极的有机光电转换元件。
尽管已参照例示实施方式对本发明进行了说明,但应理解本发明并不限于所公开的例示实施方式。下述权利要求的范围应给予最为宽泛的解释以包括所有这样的变形以及等同的结构和功能。
本申请要求于2015年6月5日提交的日本专利申请no.2015-115237的权益,由此通过引用将其全部内容并入本文。
- 还没有人留言评论。精彩留言会获得点赞!