固态电解质及其制备方法和应用与流程
本发明属于电池领域,具体而言,本发明涉及固态电解质及其制备方法和应用。
背景技术:
电动车辆需要电池可以在低至-30℃的寒冷温度或大于45℃的高温温度范围且在不到30分钟内充电,对现有电动车辆的电池来说是个较大的挑战。现有商业锂离子电池主要采用具有有机溶剂的液体电解质,但液体电解质中的有机溶剂会在低温下变粘,并在高温下挥发。粘度的增加降低了液体电解质的离子电导率,并降低了安全充电速率。此外,有机溶剂的挥发性和易燃性妨碍了电池的安全性,并可导致火灾或爆炸。目前有用有机溶剂和固体离子导体如聚合物或无机晶体和玻璃代替它们的商业化方案以降低电池的着火风险。第一代固体锂电解质包括聚环氧乙烷和聚偏氟乙烯聚合物的锂盐溶液,或硫化物、氧化物和磷酸盐基的单离子无机导体,例如lps、llzo和latp族。虽然使用这些固体导体可以提高电池安全性,但它们的性能劣于具有液体电解质的电池。通常,具有固体电解质的电池仅在40℃左右的高温下性能优异。此外,它们的能量密度和充电速率显著低于具有液体电解质的电池。
同时,在现有固态电解质的制备过程中,难以加工成具有大表面积(>15cm×15cm)和高密度(>90%)的厚度<25μm的薄膜,且所得的薄膜拉伸强度不足,无法经受电池组装。现有固态电解质的处理限于在惰性气氛且温度>1000℃的高温条件下进行烧结处理。另外,低电阻界面即通常被称为固体电解质界面(sei)在具有液体电解质的电池中是不可缺少的,而在含固态电解质的电池中,涂覆和保护电极活性材料免于与固态电解质反应的研究仍然是初期的,并且对于商业化来说还不够成熟。
因此,现有固态电解质有待进一步改进。
技术实现要素:
本发明旨在至少在一定程度上解决相关技术中的技术问题之一。为此,本发明的一个目的在于提出一种固态电解质及其制备方法和应用。该固态电解质质地柔软、密度低、易于挤压,不与空气或水反应,且室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,氧化稳定性和热稳定性好,同时与电极活性材料的反应性低。
在本发明的一个方面,本发明提出了一种固态电解质,根据本发明的实施例,所述固态电解质的通式为li3mx6,其中,x选自cl-、br-、i-、f-、bf4-、pf6-、bob-、三氟甲基磺酰亚胺阴离子和双氟甲基磺酰亚胺阴离子中的至少之一,m选自sc3+、y3+、la3+、mo3+、b3+、al3+、ga3+、in3+和fe3+中的至少之一。
根据本发明实施例的固态电解质,其不含硫、氧或磷酸盐配体,并具有高的锂传导性。同时质地柔软、密度低、易于挤压,且不与空气或水反应。室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,氧化稳定性和热稳定性好,同时与电极活性材料的反应性低。
另外,根据本发明上述实施例的固态电解质还可以具有如下附加的技术特征:
在本发明的一些实施例中,所述x选自cl-、br-、i-和f-中的至少之一,m选自y3+、mo3+、al3+和fe3+中的至少之一。
在本发明再一个方面,本发明提出了一种制备固态电解质的方法,根据本发明的实施例,该方法包括:
按照化学计量比将lix与mx3混合研磨;
将所述混合研磨后所得的混合物在惰性气氛下进行烧结,冷却后得到固态电解质li3mx6,其中,所述lix与所述mx3中的x选自cl-、br-、i-、f-、bf4-、pf6-、bob-、三氟甲基磺酰亚胺阴离子和双氟甲基磺酰亚胺阴离子中的至少之一,所述mx3中的m选自sc3+、y3+、la3+、mo3+、b3+、al3+、ga3+、in3+和fe3+中的至少之一。
根据本发明实施例的制备固态电解质的方法,通过按照化学计量比将lix与mx3混合研磨,有利于提高lix与mx3的接触面积,同时能使得少量lix与mx3发生固相反应生成li3mx6;混合研磨后的混合物在惰性气氛下烧结后,能使得原料lix与mx3进行高温固态反应并且反应充分,按照化学计量比生成相应量的li3mx6,冷却后得到固态电解质li3mx6。发明人经过大量实验意外发现,该方法通过采用简单的研磨和烧结相结合的工艺,既便于实现工业化生产,又能制备得到柔软、密度低、易于挤压、纯度高、室温下离子电导率达1.2ms/cm、电子电导率低至10-9s/cm、氧化稳定性和热稳定性好且与电极活性材料的反应性低的固态电解质。
另外,根据本发明上述实施例的制备固态电解质的方法还可以具有如下附加的技术特征:
在本发明的一些实施例中,所述混合研磨的时间为1-2h。
在本发明的一些实施例中,所述烧结的温度不大于800℃,时间为10-60h。
在本发明的一些实施例中,所述烧结的温度为550-800℃,时间为10-60h。
在本发明的一些实施例中,所述烧结为以5℃/min的速度从200℃升温至750℃,烧结10-60h。
在本发明的一些实施例中,所述冷却为以5℃/min的速度冷却至200℃。
在本发明的一些实施例中,所述lix和所述mx3的纯度分别独立的不小于95%。
在本发明的又一个方面,本发明提出了一种固态电池,根据本发明的实施例,该固态电池具有上述固态电解质。因该固态电解质柔软、易于挤压,使得固态电解质可根据电池的要求灵活变换具体形态,显著提高了该固态电解质的适用性;同时因该固态电解质纯度高,室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,与电极活性材料的反应性低,使得该电池具有较好的充放电性能;进一步的,因该固态电解质的氧化稳定性和热稳定性好,有利于提高固态电池对环境的适应性,避免因温度过高导致固态电池爆炸等事故的发生,同时可避免因氧化性环境导致的电池性能损坏问题。
在本发明的又一个方面,本发明提出了一种车辆,根据本发明的实施例,该车辆具有上述固态电池。该固态电池具有较好的充放电性能,同时对环境的适应性强,使得车辆能在具有较高里程数的同时对环境的适应性提高。
本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:
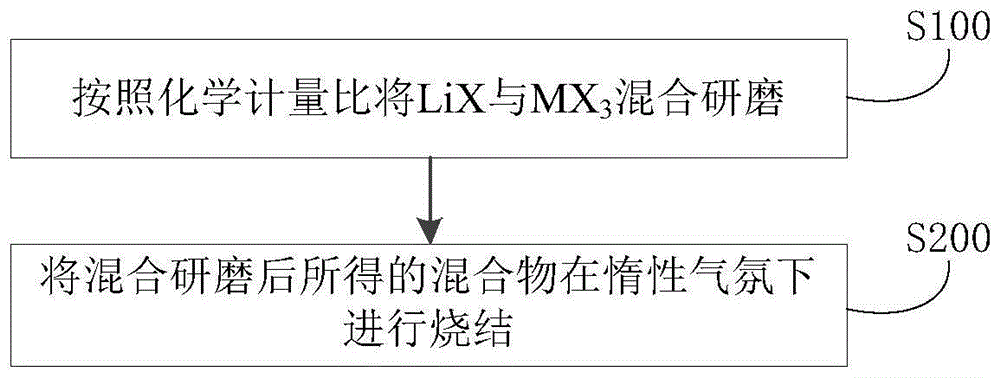
图1是根据本发明一个实施例的制备固态电解质的方法流程示意图;
图2是实施例1和对比例1所得的固态电解质li3ybr6与ybr3的xrd图谱;
图3是实施例1和对比例1所得的固态电解质li3ybr6与[6-319]libr/libr、[49-959]libr/libr的xrd图谱;
图4(a)是与含对比例1所得的li3mbr6的阴极循环之后的铟阳极中br的x射线能谱分析信号图;
图4(b)是与含对比例1所得的li3mbr6的阴极循环之后的铟阳极中y的x射线能谱分析信号图;
图4(c)是与含对比例1所得的li3mbr6的阴极循环之后的铟阳极中in的x射线能谱分析信号图;
图5是在li/li电池电镀/剥离循环中通过对比例1所得的li3ybr6剥离所得的电压-时间、电流-时间曲线图;
图6是在li/li电池电镀/剥离循环中通过对比例1所得的li3ybr6剥离的cv循环曲线图;
图7是含对比例1所得的固态电解质li3ybr6的li/nmc811电池的第一循环曲线图;
图8是含对比例1所得的固态电解质li3ybr6的in/nmc811电池循环曲线图;
图9(a)是实施例1所得固态电解质li3ybr6的阻抗谱图;
图9(b)是图9(a)的局部放大图;
图10是实施例1所得固态电解质li3ybr6的电子电导率测试中电流-时间关系图;
图11是实施例1所得固态电解质li3ybr6的差分扫描量热法热稳定性曲线图;
图12是实施例1和对比例4、对比例5所得固态电解质li3ybr6的氧化稳定性曲线图。
具体实施方式
下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
在本发明的一个方面,本发明提出了一种固态电解质,根据本发明的实施例,该固态电解质的通式为li3mx6,其中,x可以选自cl-、br-、i-、f-、bf4-、pf6-、bob-、三氟甲基磺酰亚胺阴离子和双氟甲基磺酰亚胺阴离子中的至少之一,优选cl-、br-、i-和f-中的至少之一,m可以选自sc3+、y3+、la3+、mo3+、b3+、al3+、ga3+、in3+和fe3+中的至少之一,优选y3+、mo3+、al3+和fe3+中的至少之一。发明人发现,现有固态电解质的性能包括能量密度和充电速率大多劣于液态电解质,且热稳定性差,同时工业化的固态电解质的表面积均较小,密度较低,厚度较大,拉伸强度不够,且较难经受得起电池组装而不破损。发明人经过大量实验后提出了通式为li3mx6的上述固态电解质,其不含硫、氧或磷酸盐配体,且经大量实验发现其具有高的锂传导性,同时质地柔软、密度低、易于挤压,且不与空气或水反应,室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,氧化稳定性和热稳定性好,同时与电极活性材料的反应性低。
在本发明的再一个方面,本发明提出了一种制备上述固态电解质的方法,根据本发明的实施例,参考图1,该方法包括:
s100:按照化学计量比将lix与mx3混合研磨
该步骤中,按照化学计量比将lix与mx3混合研磨。发明人发现,通过按照化学计量比将lix与mx3混合研磨,有利于提高lix与mx3的接触面积,提高反应程度,同时能使得少量lix与mx3反应生成li3mx6。
根据本发明的一个实施例,x可以选自cl-、br-、i-、f-、bf4-、pf6-、bob-、三氟甲基磺酰亚胺阴离子和双氟甲基磺酰亚胺阴离子中的至少之一,m可以选自sc3+、y3+、la3+、mo3+、b3+、al3+、ga3+、in3+和fe3+中的至少之一。进一步的,lix和mx3的纯度可以分别独立的不小于95%,例如,lix可以为无水且纯度为99.0%的lix,mx3可以为无水且纯度为99.99%的mx3。进一步的,混合研磨的时间可以为1-2h,例如可以为1h、1.2h、1.4h、1.6h、1.8h、2.0h。发明人发现,该研磨时间相对于现有球磨合成的技术方案,时间显著降低,同时通过研磨lix与mx3可发生固相反应,生成少量的li3mx6。
s200:将混合研磨后所得的混合物在惰性气氛下进行烧结
该步骤中,将混合研磨后所得的混合物在惰性气氛下进行烧结,冷却后得到固态电解质li3mx6。发明人发现,混合研磨后的混合物在惰性气氛下烧结后,能使得原料lix与mx3进行高温固态反应并且反应充分,按照化学计量比生成相应量的li3mx6,冷却后得到固态电解质li3mx6。进一步的,发明人经过大量实验意外发现,该方法通过采用简单的研磨和烧结相结合的工艺,既便于实现工业化生产,又能制备得到柔软、密度低、易于挤压,并且纯度高,室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,氧化稳定性和热稳定性好,与电极活性材料的反应性低的固态电解质。同时,发明人也研究了采用球磨机球磨制备固态电解质li3mx6的方法,但大量实验发现,要想通过球磨使得lix与mx3的反应程度较高,同时得到电导率较高的固态电解质li3mx6,球磨转速必须非常高,例如大于600rpm。而现有工业化使用的球磨机中,很少有能达到该转速的,能达到该转速的大多是小容量的,无法满足工业化生产的需求。
根据本发明的一个实施例,烧结的温度可以不大于800℃,时间可以为10-60h。发明人发现,该温度相对于现有需在大于1000℃的温度下进行烧结的工艺来说,温度显著降低,但所烧结出来的固态电解质室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,氧化稳定性和热稳定性好,同时与电极活性材料的反应性低。进一步的,烧结的温度可以为550-800℃,例如可以为550℃、600℃、650℃、700℃、750℃、800℃,时间可以为10-60h。发明人经过大量实验意外发现,在上述温度和时间范围内烧结有利于提高lix与mx3的固相反应速率,同时提高固态电解质li3mx6的品质。进一步的,烧结可以以5℃/min的速度从200℃升温至750℃,烧结10-60h,例如烧结10h、20h、30h、40h、50h、60h。发明人经过大量实验意外发现,采用上述升温形式可进一步提高lix与mx3的固相反应速率,同时提高固态电解质li3mx6的品质。进一步的,冷却可以以5℃/min的速度冷却至200℃。由此,有利于维持固态电解质li3mx6品质的稳定性。进一步的,惰性气氛可以为氮气或氩气,同时在烧结过程中,惰性气体的流量并不受特别限制,本领域技术人员可以根据实际需要进行选择。
进一步的,根据本发明的实施例,采用本申请的上述方法制备得到的固态电解质,由x射线衍射图谱可知,固态电解质li3mx6中基本不含原料lix与mx3,即lix与mx3反应充分。而采用相同原料lix与mx3但采用不同转速(包括200rpm、400rpm、600rpm)的普通行星式球磨机或者来自retsch的emax非行星式高能球磨机球磨合成所得的固态电解质li3mx6中,原料的反应程度无法达到100%。同时采用本申请的上述方法制备得到的固态电解质的电导率相对于采用相同原料lix与mx3但采用不同转速(包括200rpm、400rpm、600rpm)的普通行星式球磨机或者来自retsch的emax非行星式高能球磨机球磨合成所得的固态电解质的电导率相对也较低。根据本发明的具体实施例,采用libr与mbr3为原料,采用不同转速(包括200rpm、400rpm、600rpm)的普通行星式球磨机或者来自retsch的emax非行星式高能球磨机球磨合成固态电解质li3mx6的反应程度和电导率如表1所示。由表1可知,转速对原料反应程度和电导率的影响,反应程度随球磨机转速的增加而增加,类似地,最终所得固态电解质的电导率也随球磨转速增加而增加。
表1不同制备工艺下libr与mbr3的反应程度及所得固态电解质的电导率
需要说明的是,虽然固态电解质li3mx6可以通过球磨合成,但目前适合商业应用的球磨机的转速被限定在较低范围内。少数具有1l容量的大罐的商业球磨机可以以高于400rpm的速度旋转,大部分大容量的球磨机的转速为200rpm。由表1可知,在低转速下采用球磨机合成的固态电解质显示出较低的电导率和原料反应程度。当转速超过600rpm时,原料的xrd信号减少或没有。不幸的是,能够快速旋转的球磨机通常只具有小的罐,例如50ml或更少,不适于大规模的商业应用。
根据本发明实施例的制备固态电解质的方法,通过按照化学计量比将lix与mx3混合研磨,有利于提高lix与mx3的接触面积,同时能使得少量lix与mx3反应生成li3mx6;混合研磨后的混合物在惰性气氛下烧结后,能使得原料lix与mx3进行高温固态反应并且反应充分,按照化学计量比生成相应量的li3mx6,冷却后得到固态电解质li3mx6。发明人经过大量实验意外发现,该方法通过采用简单的研磨和烧结相结合的工艺,既便于实现工业化生产,又能制备得到柔软、密度低、易于挤压,并且纯度高,室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,氧化稳定性和热稳定性好,与电极活性材料的反应性低的固态电解质。
在本发明的又一个方面,本发明提出了一种固态电池,根据本发明的实施例,该固态电池具有上述固态电解质。因该固态电解质柔软、易于挤压,使得固态电解质可根据电池的要求灵活变换具体形态,显著提高了该固态电解质的适用性;同时因该固态电解质纯度高,室温下离子电导率达1.2ms/cm,电子电导率低至10-9s/cm,与电极活性材料的反应性低,使得该电池具有较好的充放电性能;进一步的,因该固态电解质的氧化稳定性和热稳定性好,有利于提高固态电池对环境的适应性,避免因温度过高导致固态电池爆炸等事故的发生,同时可避免因氧化性环境导致的电池性能损坏问题。
在本发明的又一个方面,本发明提出了一种车辆,根据本发明的实施例,该车辆具有上述固态电池。该固态电池具有较好的充放电性能,同时对环境的适应性强,使得车辆能在具有较高里程数的同时对环境的适应性提高。
下面参考具体实施例,对本发明进行描述,需要说明的是,这些实施例仅仅是描述性的,而不以任何方式限制本发明。
实施例1
按照化学计量比将无水且纯度为99.0%的libr与无水且纯度为99.99%的ybr3混合研磨1-2h;然后将混合研磨后所得的混合物在氮气气氛下以5℃/min的速度从200℃升温至750℃,烧结24h,接着以5℃/min的速度冷却至200℃后得到白色玻璃状/蜡状的片状材料固态电解质li3ybr6,该材料柔软,当压制薄时可形成半透明的粒料。其xrd图谱如图2和3所示。由图2可知,在固态电解质li3ybr6中,不存在ybr3图谱,即ybr3反应完全。由图3可知,在固态电解质li3ybr6中,不存在libr图谱,即libr反应完全。即该固态电解质li3ybr6具有高纯度。同时在不锈钢电极之间将该固态电解质li3ybr6压制成小球,其阻抗谱如图9所示,由图9可知,在室温下该固态电解质li3ybr6的电导率为1.2ms/cm。进一步的,对该该固态电解质li3ybr6进行电子电导率测试,具体的,颗粒厚度为300μm,面积为0.785cm2,测试电压为2v,1min后的稳态电流为0.24μa。所得电流随时间的关系图如图10所示,由图10计算可知,该固态电解质li3ybr6的电子电导率为10-9s/cm。进一步的,对该固态电解质li3ybr6进行热稳定性测试,其差分扫描量热法热稳定性如图11所示,由图11可知,该固态电解质li3ybr6在高达500摄氏度时依然稳定。进一步的,其氧化稳定性如图12所示。
对比例1
按照化学计量比将无水且纯度为99.0%的libr与无水且纯度为99.99%的ybr3送至转速为400rpm的普通行星式球磨机球磨120h,得到电导率为0.2ms/cm的固态电解质li3ybr6。且所得li3ybr6与libr的质量比为1.8:1,libr的反应程度约50%。
其xrd图谱如图2和3所示。由图2可知,在固态电解质li3ybr6中,ybr3图谱仍然可见,即ybr3反应不完全。由图3可知,在固态电解质li3ybr6中,libr图谱仍然可见且具有较高的比率,即libr反应不完全。
对比例2
按照化学计量比将无水且纯度为99.0%的licl与无水且纯度为99.99%的ycl3送至转速为400rpm的普通行星式球磨机球磨120h,得到电导率为0.1ms/cm的固态电解质li3ycl6。且所得li3ycl6与licl的质量比为1:4.3,licl的反应程度小于20%。
对比例3
按照化学计量比将无水且纯度为99.0%的lii与无水且纯度为99.99%的yi3送至转速为400rpm的普通行星式球磨机球磨120h,得到电导率为0.8ms/cm的固态电解质li3yi6。且所得li3yi6与lii的质量比为1:0,lii的反应程度为100%,有少量yi3存留。
对比例4
按照化学计量比将无水且纯度为99.0%的libr与无水且纯度为99.99%的ybr3送至转速为350rpm的普通行星式球磨机球磨120h,得到电导率为0.1ms/cm的固态电解质li3ybr6。其氧化稳定性如图12所示。
对比例5
按照化学计量比将无水且纯度为99.0%的libr与无水且纯度为99.99%的ybr3送至转速为600rpm的普通行星式球磨机球磨40h,得到电导率为0.8ms/cm的固态电解质li3ybr6。其氧化稳定性如图12所示。
由对比例1-3可知,在相同的400rpm的球磨转速下,对比例3的碘代反应进行的程度高于对比例1的溴代反应,对比例1的溴代反应进行的程度又高于对比例2的氯代反应。即要使反应程度达到100%,氯代反应所需的能量>溴代反应>碘代反应。即卤元素离子的具体类型决定了在较低转速下lix与mx3的反应程度。
在对比例1和对比例2中,虽然未反应的libr、licl可能降低电导率,但因libr、licl在锂金属上是稳定的,并且可以形成钝化膜,不会对锂金属的还原稳定性产生负面影响。然而,ybr3、ycl3是强路易斯酸,其具有准备好接受电子的空轨道。因此,ybr3、ycl3在低电压或存在锂金属的情况下容易还原。由对比例1和对比例2可知,对比例1所得的li3ybr6比对比例2所得的li3ycl6具有更高的电导率。
对对比例1所得的li3ybr6进行进一步研究。具体的,在低电压下,铟阳极在与含对比例1所得的li3mbr6的阴极循环之后的x射线能谱分析信号如图4所示,为了更好的分析在铟阳极中间进行了刮擦。由图4可知,铟阳极在与含上述li3mbr6固态电解质的阴极循环之后铟阳极上具有痕量的y和br,其表明存在分解,产生了少量的y和br。因li3mbr6中含有高含量的未反应的ybr3,ybr3是一种路易斯酸,其易于进行还原,而这种易还原的性质可能是造成上述分解的原因。即球磨反应产生的产物li3mx6含有不同量的未反应的路易斯酸,其降低了产物li3mx6总的还原稳定性。为了使固态电解质li3mx6的电压稳定窗口最大化,关键是驱使反应完全进行,以除去未反应的起始材料如ycl3路易斯酸。
以对比例1所得的li3ybr6为例,在li/li电池电镀/剥离循环中,通过对对比例1所得的li3ybr6剥离,实验面积为0.785cm2,其电压、电流随时间的关系如图5所示,cv循环曲线如图6所示。由图5可知,li/li电池在电镀/剥离循环中显示出略微增加的过电位。由图6可知,li会发生可逆镀覆,li3ybr6具有相对于li的高于5v的高氧化稳定性。
在室温且放电速率为c/10的条件下,对含对比例1所得的固态电解质li3ybr6的li/nmc811电池进行第一循环,其中,装配压力为400mpa,测试压力约1mpa,nmc811阴极的厚度为50μm,nmc811:固态电解质li3ybr6:c的比为70:29:1,导电隔膜厚度为400μm。得到ncm811活性材料的理论容量如图7所示。由图7可知,li/nmc811全电池可能是由于li阳极的反应性增加不能良好循环。然而,nmc811阴极可以与in阳极一起循环。在室温且放电速率为c/10的条件下,对含对比例1所得的固态电解质li3ybr6的in/nmc811电池进行循环,结果如图8所示。其中,装配压力为400mpa,测试压力约1mpa,nmc811阴极的厚度为50μm,nmc811:固态电解质li3ybr6:c的比为70:29:1,导电隔膜厚度为400μm。由图8可知,in的还原电位比li的还原电位高0.7v,并且in的反应性较低,这与对比例1所得的固态电解质li3ybr6中仍然存在ybr3路易斯酸有关。同时,in的还原电位也略高于y的还原电位,可从ybr3中排除不希望的电镀钇金属。
由图12可知,对比实施例1和对比例4、对比例5,在350rpm的普通行星式球磨机球磨所得的固态电解质li3ybr6具有最低的氧化稳定性,这可能是由于未反应的原料含量高。而600rpm的普通行星式球磨机球磨和采用本申请制备方法制备得到的固态电解质li3ybr6具有较高的稳定性,且采用本申请的方法制备得到的固态电解质li3ybr6是最稳定的。
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
- 还没有人留言评论。精彩留言会获得点赞!