一种人工固体电解质中间相及其制备方法、固态锂离子电池与流程
本发明属于锂离子电池
技术领域:
,具体涉及一种人工固体电解质中间相及其制备方法,还涉及一种固态锂离子电池。
背景技术:
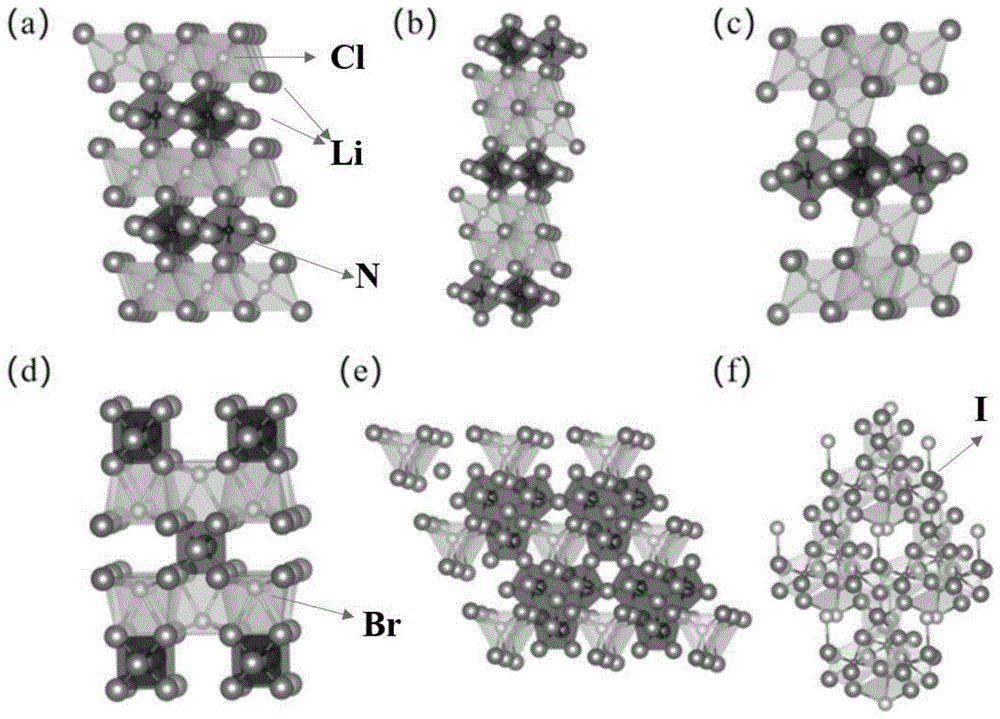
:传统的液态锂离子电池由于采用液态电解液,存在易泄漏、易挥发、易燃烧等安全问题。采用全固态电池替代液态锂离子电池是解决上述安全问题的重要途径。其中固体电解质是全固态电池的重要组成。无机固态电解质是常用的固体电解质之一。目前大多无机固态电解质已经能够达到液态电解质的锂离子电导率标准(即锂离子电导率大于1ms·cm-1)。但是由于锂金属负极过于活泼,无机固体电解质在与锂金属负极直接接触时会发生较为剧烈的电化学反应,使得无机固体电解质的稳定性受到较大影响,从而影响固态锂离子电池的循环稳定性。因此为提高无机固体电解质的稳定性,需要使用抑制固体电解质与锂金属负极反应的固体电解质中间相(solidelectrolyteinterphase,sei)。无机固体电解质与锂金属负极直接接触发生电化学反应能够原位生成的sei。如lgps电解质材料相对锂金属负极的还原电压为1.71v,会与锂金属负极逐步反应生成p、liges4、li2s等原位固体电解质中间相;li6ps5cl电解质材料相对锂金属负极的还原电压同样为1.71v,会与锂金属负极逐步反应生成p、li2s、li2s等原位固体电解质中间相;llto电解质材料相对锂金属负极的还原电压为1.75v,会与锂金属负极逐步反应生成li4ti5o15、li7/6ti11/6o4、la2ti2o7等原位固体电解质中间相。这些原位生成的固体电解质中间相虽然能够起到钝化作用,抑制固态电解质与锂金属负极继续反应,但其锂离子电导率相对较低,会影响锂离子的快速输运;并且在生成过程中会消耗掉固态电解质本身,进而影响电池的循环稳定性;在锂金属负极表面形成的原位固体电解质中间相大多分布不均匀,会促进锂枝晶和死锂的生成,减少电池寿命。基于上述问题,现有技术中通过人工固体电解质中间相的方法来抑制固体电解质与锂金属负极的反应。常用的人工固体电解质中间相有卤化锂、氮化锂、锂金属合金等。其中卤化锂相对锂的稳定电压很高(lif:6.02v,licl:3.71v,libr:2.66v,lii:2.44v),能起到钝化稳定作用,但其锂离子电导率非常有限(低于10-5s·cm-1),不能满足锂离子快速输运的需求。氮化锂的锂离子电导率很高(接近1ms·cm-1),但相对锂的电压仅为0.5v左右,并不能有效阻止固体电解质与锂金属负极发生反应,固体电解质甚至会与氮化锂本身发生较为剧烈反应。锂金属合金在一定程度上能够抑制了固态电解质与锂金属负极反应,但也会影响了锂离子的输运,同时降低了容量。技术实现要素:本发明的目的在于提供一种人工固体电解质中间相,该人工固体电解质中间相具有较快的锂离子电池传输能力并且能够有效抑制固体电解质与锂金属负极的反应。本发明的目的还在于提供一种上述人工固体电解质中间相的制备方法。本发明的目的还在于提供一种含上述人工固体电解质中间相的固态锂离子电池,该固态锂离子电池具有较好的循环稳定性。为实现上述目的,本发明的人工固体电解质中间相采用的技术方案为:一种人工固体电解质中间相,其化学组成为li3x+y+3a+bnx+aay+b,其中n为负三价的氮元素,a为cl元素、br元素、i元素中的一种或多种;1≤x≤3,1≤y≤3,-0.6≤a≤0.6,-0.5≤b≤0.5。本发明的人工固体电解质中间相的化学组成可以认为是(x+a)li3n·(y+b)lia,其中a、b表示可偏离标准成分值。由li3n以及lia两部分组合而成,其晶格尺寸主要由li-n或li-a间的离子键长所决定。而li-n或li-x间的离子键长主要决定于非金属离子(n及a)的电负性,电负性越强,相应键长越短。键越短则晶格尺寸越小,晶格尺寸越小使得锂离子电导率相对较高。本发明的人工固体电解质中间相的锂离子电导率由锂离子在人工固体电解质中间相中的扩散系数决定。锂离子的扩散系数则由主要由锂离子在li3n上的迁移所决定。锂离子在迁移时会受到卤族阴离子a的影响,由于阴阳离子的相互吸引,当卤族阴离子a含量过高或者电负性较大时会束缚住锂离子,影响锂离子的扩散系数。影响本发明的人工固体电解质中间相的电化学电压平台的主要因素为卤族阴离子a与氮元素的含量以及卤族阴离子a的种类。卤族阴离子a含量较高时电压平台会变大,氮元素含量较高时,电压平台会相应变小。这是由于氮化锂的电压平台较低而卤化锂的电压平台较高。对于不同类型的卤族阴离子a,往往其电负性越大电压平台越高,这可能主要是由于卤族元素的电负性越大,对锂离子的束缚越强,从而导致在较高电压下才会失去锂,即电压平台较高。综上所述,通过对卤族阴离子a与氮元素的含量以及卤族阴离子a的种类进行合理的选择以及优化,本发明的人工固体电解质中间相具有较高的锂离子电导率,以及合适的电化学电压平台,更低的扩散激活能以及稳定的热力学性能。与现有的人工固体电解质中间相相比,本发明的人工固体电解质中间相,具有较高的锂离子电子电导率,能够实现锂离子电池的快速运输;具有合适电化学电压平台,能够有效抑制固体电解质与锂金属负极的反应;具有较高的弹性模量,能够抑制锂枝晶的形成与生长。进一步优选的,当a为cl元素时,化学组成为li3x+y+3a+bnx+acly+b,其中1≤x≤3,1≤y≤3,-0.5≤a≤0.5,-0.5≤b≤0.5。进一步优选的,x=1,1≤y≤3,-0.5≤a≤0.5,-0.5≤b≤0.5。进一步优选的,当a为br元素时,化学组成为li3x+y+3a+bnx+abry+b,其中1≤x≤3,1≤y≤2,-0.6≤a≤0.6,-0.5≤b≤0.5。进一步优选的,当a为i元素时,化学组成为li3x+y+3a+bnx+aiy+b,其中1≤x≤2,1≤y≤3,-0.5≤a≤0.5,-0.5≤b≤0.5。进一步优选的,x=2,y=1,-0.5≤a≤0.5,-0.5≤b≤0.5。由于cl、br、i三种元素同为卤族元素,价态相同并且三者元素的电负性相差不大,因此本发明的人工固体电解质中间相中a同样可以为cl、br、i中的多种元素。本发明的人工固体电解质中间相为晶体或非晶体。所述非晶体为玻璃体。本发明的人工固体电解质中间相中,li为+1价,n为-3价,a为-1价,为典型的离子化合物体系,因此其玻璃体(尤其是弛豫玻璃态)中的离子化学环境与晶体状态相似。玻璃体中相对较高的空穴浓度,对锂离子扩散有利。本发明的人工固体电解质中间相可以采用现有技术如熔融法,机械合金化法,粉末冶金法,真空镀膜法或化学气相沉积法等方法进行制备。制备过程需要在能够对锂离子提供惰性保护的保护性气氛,保护性气氛为惰性气体或真空环境。其中低温制备过程如机械合金化法、真空镀膜法有利于制得玻璃体人工固体电解质中间相。为简化操作过程,便于大规模生产,本发明的人工固体电解质中间相的制备方法采用的技术方案为:一种人工固体电解质中间相的制备方法,包括以下步骤:(1)在保护气氛下,将原料lia粉与li3n粉混合均匀,得混合料;所述lia粉为licl粉、libr粉、lii粉中的一种或多种;(2)在保护气氛下对混合料进行热处理,然后冷却;所述热处理为在400~450℃温度下保温9~11h。本发明的人工固体电解质中间相中,步骤(1)中混合料可以为陶瓷坯体的形式,将混合料为陶瓷坯体时各原料成分结合更加紧密,有助于新的晶体生成和离子扩散。所述混合均匀为干混或将原料粉分散在无水质子惰性溶剂中混匀,所述无水质子惰性溶剂为环己烷、四氢呋喃、二氧五环、n,n-二甲基甲酰胺、丙酮、庚烷、乙酸乙酯中的至少一种。所述干混具体为将粉料球磨混合均匀。其中各原料在无水质子惰性溶剂中混匀时,还可以加入现有技术中常用的粘结剂如sbr、pvdf等来增加原料在溶剂中的粘结性。所述冷却为自然冷却或淬火冷却。采用不同的冷却方法即可得到不同形态的人工固体电解质中间相,如采用淬火冷却则得到玻璃体的人工固体电解质中间相,其中淬火冷却采用的介质为冰水。本发明的固态锂离子电池采用的技术方案为:一种含上述人工固体电解质中间相的固态锂离子电池。本发明的人工固体电解质中间相合适的电化学电压平台以及超快的锂离子传输能力,因此含本发明的人工固体电解质中间相的固态锂离子电池具有较好的循环稳定性以及倍率性能。在固态锂离子电池中,本发明的人工固体电解质中间相有以下两种添加方式:(1)将本发明的人工固体电解质中间相与现有技术中常用的无机固体电解质混合使得固固体电解质中含人工固体电解质中间相,所述固体电解质中人工固体电解质中间相的质量百分含量为5~50%。(2)固态锂离子电池中包括锂金属负极以及锂金属负极表面的保护层,所述保护层中含人工固体电解质中间相。具体为将人工固体电解质中间相涂覆在锂金属负极表面。附图说明图1为本发明的实施例1~6的人工固体电解质中间相的结构示意图;图2为本发明的实施例1~6的人工固体电解质中间相的xrd图;图3为本发明的试验例5中采用纯固体电解质li6ps5cl时的对电测试结果;图4为本发明的试验例5中将固体电解质li6ps5cl与li6ncl3结合后的对电测试结果;图1中,(a)为li4ncl,(b)为li5ncl2,(c)为li6ncl3,(d)为li5nbr2,(e)为li10n3br,(f)为li7n2i。具体实施方式下面结合具体实施例对本发明作进一步说明。一、人工固体电解质中间相的实施例实施例1~19实施例1~19的人工固体电解质中间相的化学组成具体如表1所示。表1各实施例的人工固体电解质中间相的化学组成二、人工固体电解质中间相的制备方法的实施例实施例20本实施例为实施例1的人工固体电解质中间相li4ncl的制备方法,具体包括以下步骤:(1)将氮化锂粉、氯化锂粉分别在真空干燥箱中干燥24h;(2)在手套箱中氩气气氛保护下,将干燥后的氮化锂粉以及氯化锂粉按照1:1的摩尔比均匀混合后装入球磨罐中,然后将15个直径为10mm的氧化锆球磨球装入球磨罐中,然后密封;(3)将密封好的球磨罐从手套箱中取出,装入全方位行星球磨机中进行球磨,球磨时球磨机转速为300rpm,每球磨20min静置冷却5min,总有效球磨时间为10h,球磨后得混合粉体;(4)将混合粉体取出后称取0.2g冷压成直径为16mm的陶瓷坯体,然后在真空管式炉中在氩气气氛中进行热处理,热处理的温度为400℃,时间为10h,热处理结束后缓慢冷却(即随炉冷却)至室温,即得晶体li4ncl。本实施例中所得晶体li4ncl在使用时,粉碎即可。实施例21本实施例为实施例2的人工固体电解质中间相li5ncl2的制备方法,具体包括以下步骤:(1)将氮化锂粉、氯化锂粉分别在真空干燥箱中干燥24h;(2)在手套箱中氩气气氛保护下,将干燥后的氮化锂粉以及氯化锂粉按照1:2的摩尔比均匀混合后装入球磨罐中,然后将15个直径为10mm的氧化锆球磨球装入球磨罐中,然后密封;(3)将密封好的球磨罐从手套箱中取出,装入全方位行星球磨机中进行球磨,球磨时球磨机转速为300rpm,每球磨20min静置冷却5min,总有效球磨时间为10h,球磨后得混合粉体;(4)称取0.5g混合粉体在真空环境下密封于石英玻璃管中(通过橡胶圈以及密封阀密封),然后在马弗炉中进行热处理,热处理温度为430℃,保温时间为10h;待粉体融化完全后将石英玻璃管放入冰水进行淬火处理,即得玻璃体li5ncl2。实施例22本实施例为实施例3的人工固体电解质中间相li6ncl3的制备方法,制备过程基本与实施例20相同,区别仅在于:步骤(2)中氮化锂粉与氯化锂粉按照1:3的摩尔比均匀混合;步骤(4)中热处理温度为450℃。本实施例的制备方法制得的li6ncl3为晶体。实施例23本实施例为实施例4的人工固体电解质中间相li5nbr2的制备方法,制备过程与实施例20的区别在于:将氯化锂粉替换为溴化锂粉,并且步骤(2)中氮化锂粉与溴化锂粉按照1:2的摩尔比均匀混合;步骤(4)为:将混合粉体在氩气气氛下于真空管式炉中进行热处理,热处理为在430℃温度下保温10h,热处理结束后缓慢冷却至室温即得li5nbr2。本实施例的制备方法制得的li5nbr2为晶体。实施例24本实施例为实施例5的人工固体电解质中间相li10n3br的制备方法,制备过程与实施例20的区别在于:将氯化锂粉替换为溴化锂粉,并且步骤(2)中氮化锂粉与溴化锂粉按照3:1的摩尔比均匀混合;步骤(4)为:称取0.5g混合粉体在真空环境下密封于石英玻璃管中,然后在马弗炉中进行热处理,热处理为在450℃温度下保温10h;待粉体融化完全后使用冰水进行淬火处理,即得玻璃体li10n3br。实施例25本实施例为实施例6的人工固体电解质中间相li7n2i的制备方法,制备过程与实施例20的区别在于:将氯化锂粉替换为碘化锂粉,并且步骤(2)中氮化锂粉与碘化锂粉按照2:1的摩尔比均匀混合;步骤(4)为:将球磨后的混合粉体在真空管式炉中于氩气气氛下进行热处理,热处理为在450℃温度下保温10h,热处理结束后缓慢冷却至室温即得li7n2i。本实施例的制备方法制得的li7n2i为晶体。实施例26本实施例为实施例7的人工固体电解质中间相li3.5ncl0.5,具体包括以下步骤:(1)将氮化锂粉、氯化锂粉分别在真空干燥箱中干燥24h;(2)在手套箱中氩气气氛保护下,将氮化锂与氯化锂按照1:0.5的摩尔比均匀混合后加入环己烷然后使用磁力搅拌机搅拌均匀,得混合液;(3)将混合液在真空管式炉中于氩气气氛下进行热处理,热处理为在400℃温度下保温10h,在热处理过程中环己烷挥发完全,热处理结束后缓慢冷却至室温,即得li3.5ncl0.5。本实施例的制备方法制得的li3.5ncl0.5为晶体。实施例27本实施例为实施例8的人工固体电解质中间相li4.5ncl1.5的制备方法,制备过程与实施例20基本相同,区别仅在于:步骤(2)中氮化锂粉与氯化锂粉按照1:1.5的摩尔比均匀混合。本实施例的制备方法制得的li4.5ncl1.5为晶体。实施例28本实施例为与实施例9的人工固体电解质中间相li5.5ncl2.5的制备方法,制备过程与实施例21基本相同,区别仅在于:步骤(2)中氮化锂粉与氯化锂粉按照1:2.5的摩尔比均匀混合。本实施例的制备方法制得的li5.5ncl2.5为玻璃体。实施例29本实施例为实施例10的人工固体电解质中间相li6.5ncl3.5的制备方法,制备过程与实施例20基本相同,区别仅在于:步骤(2)中氮化锂粉与氯化锂粉按照1:3.5的摩尔比均匀混合;步骤(4)中热处理的温度为450℃。本实施例的制备方法制得的li6.5ncl3.5为晶体。实施例30本实施例为实施例11的人工固体电解质中间相li4.5nbr1.5的制备方法,制备过程与实施例23基本相同,区别仅在于:步骤(2)中氮化锂粉与溴化锂粉按照1:1.5的摩尔比均匀混合。本实施例的制备方法制得的li4.5nbr1.5为晶体。实施例31本实施例为实施例12的人工固体电解质中间相li10.5n3br1.5的制备方法,制备过程与实施例24基本相同,区别仅在于:步骤(2)中氮化锂粉与溴化锂粉按照3:1.5的摩尔比均匀混合。本实施例的制备方法制得的li10.5n3br1.5为玻璃体。实施例32本实施例为实施例13的人工固体电解质中间相li7.5n2i1.5的制备方法,制备过程与实施例25基本相同,区别仅在于:步骤(2)中氮化锂粉与碘化锂粉按照2:1.5的摩尔比均匀混合。本实施例的制备方法制得的li7.5n2i1.5为晶体。实施例33本实施例为实施例14的人工固体电解质中间相li4.6n1.2cl的制备方法,制备过程与实施例20基本相同,区别仅在于:步骤(2)中氮化锂粉与氯化锂粉按照1.2:1的摩尔比均匀混合。本实施例的制备方法制得的li4.6n1.2cl为晶体。实施例34本实施例为实施例15的人工固体电解质中间相li5.6n1.2cl2的制备方法,制备过程与实施例21基本相同,区别仅在于:步骤(2)中氮化锂粉与氯化锂粉按照1.2:2的摩尔比均匀混合。本实施例的制备方法制得的li5.6n1.2cl2为玻璃体。实施例35本实施例为实施例16的人工固体电解质中间相li6.6n1.2cl3的制备方法,制备过程与实施例20基本相同,区别仅在于:步骤(2)中氮化锂粉与氯化锂粉按照1.2:3的摩尔比均匀混合;步骤(4)中热处理温度为450℃。本实施例的制备方法制得的li6.6n1.2cl3为晶体。实施例36本实施例为实施例17的人工固体电解质中间相li5.6n1.2br2的制备方法,制备过程与实施例23基本相同,区别仅在于:步骤(2)中氮化锂粉与溴化锂粉按照1.2:2的摩尔比均匀混合。本实施例的制备方法制得的li5.6n1.2br2为晶体。实施例37本实施例为实施例18的人工固体电解质中间相li11.8n3.6br的制备方法,制备过程与实施例24基本相同,区别仅在于:步骤(2)中氮化锂粉与溴化锂粉按照3.6:1的摩尔比均匀混合。本实施例的制备方法制得的li11.8n3.6br为玻璃体。实施例38本实施例为实施例19的人工固体电解质中间相li8.2n2.4i的制备方法,制备过程与实施例25基本相同,区别仅在于:步骤(2)中氮化锂粉与溴化锂粉按照2.4:1的摩尔比均匀混合。本实施例的制备方法制得的li8.2n2.4i为晶体。三、固态锂离子电池的实施例实施例39本实施例的固态锂离子电池,包括锂负极以及固体电解质li6ps5cl以及实施例3的人工固体电解质中间相li6ncl3,具体为:将实施例3中的人工固体电解质中间相粉末与固体电解质分上下层冷压结合(人工固体电解质中间相粉末与固体电解质的质量比为1:1),然后将人工固体电解质中间相介于锂负极和固体电解质之间。四、试验例部分通过材料基因组工程方法,在密度泛函(dft)方法及第一原理分子动力学(aimd)的理论框架下,对本发明的人工固体电解质中间相的性质进行研究。试验例1对本发明的实施例1~6的人工固体电解质中间相通过理论计算,得各人工固体电解质中间相的结构如图1所示,图1中(b)~(f)中li原子与n原子采用与(a)中相同颜色以及大小的形状表示,(b)、(c)中cl原子采用与(a)中相同颜色以及大小的形状表示,(e)中的br原子采用与(d)中相同颜色以及大小的形状表示。理论计算得到的各人工固体电解质中间相的具体信息如表2所示。表2各人工固体电解质的晶型结构信息由图1以及表2可知,li4ncl、li5ncl2、li6ncl3主要由li-n层和li-cl层交替结合,li5nbr2,li10n3br主要由li6br单元和不同形式li-n单元结合,li7n2i主要由笼状li-n结构结合而成。试验例2对本发明的实施例1~6的人工固体电解质中间相进行xrd测试,测试结果如图2所示。所得xrd图谱中各峰与li3n以及卤化锂(licl、libr以及lin)的晶型峰均不相符,表明本发明的人工固体电解质中间相并不是li3n以及卤化锂的物理混合,而是由二者结合形成了一种新的物质。试验例3对本发明的实施例1~6的人工固体电解质中间相的弹性模量(体积模量(b),剪切模量(g),杨氏模量(e))以及泊松比(ν)进行理论计算,结果如表3所示。表3各人工固体电解质中间相的弹性模量以及泊松比实施例成分b(gpa)g(gpa)e(gpa)ν1li4ncl40.9429.8071.940.212li5ncl238.2526.4464.460.213li6ncl336.8824.9761.120.224li5nbr227.2016.2840.710.255li10n3br43.4526.4765.860.246li7n2i37.4325.7362.790.22由表3可知实施例1~6的弹性模量远远高于锂枝晶(<1gpa)的弹性模量并且泊松比接近0.3,因此可有效抑制锂枝晶的形成与生长。试验例4采用电化学工作站对本发明的实施例1~19的人工固体电解质中间相的锂离子电导率以及相对锂金属负极的电压进行测试。并对其扩算激活能ea进行理论计算,计算结果如表4所示。表4各人工固体电解质中间相的相对锂的电压、锂离子电导率和扩散激活能ea。由表4可知,实施例中化学组成为li4ncl、li10n3br、li7n2i的锂离子电导率在常温接近或高于1ms·cm-1。li6ncl3电压平台接近目前大多数固态电解质的还原电压(如lgps为1.71v,li6ps5cl为1.71v,llto为1.75v),能够有效抑制固态电解质与锂金属负极反应,因此li6ncl3的性能最好。在实施例7~19中的偏相中,可以看到,当增加氮化锂的比例时人工固体电解质中间相的电压平台会降低,锂离子电导率会增高;而当卤化锂含量增高时,则与此相反。试验例5将人工固体电解质中间相粉末li6ncl3与固体电解质li6ps5cl分上下层冷压结合(二者的质量比为1:1),然后将人工固体电解质中间li6ncl3相介于锂负极和固体电解质之间,进行60℃热处理后,然后进行对电测试(具体结构为:锂负极/li6ncl3/li6ps5cl/li6ncl3/锂负极),测试结果如图4所示。同时,采用纯固体电解质li6ps5cl置于两锂负极之间进行对电测试(具体结构为锂负极/li6ps5cl/锂负极),测试结果如图3所示。由测试结果可知,同样在0.05ma/cm2电流下,纯固态电解质li6ps5cl在对电过程中运行50h后发生短路而且极化严重。而加入人工固体电解质中间相后,运行200h后仍然稳定,表明本发明的人工固体电解质中间相能够有效减弱固体电解质与锂负极的副反应。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1