一种含钴废旧锂离子电池回收利用的方法与流程
1.本发明属于电池回收利用技术领域,具体涉及一种含钴废旧锂离子电池回收利用的方法。
背景技术:
2.近年来我国新能源汽车产业迅猛发展。车用动力电池退役之后,若未经过循环利用而肆意丢弃会带来一系列安全、污染和资源浪费问题。目前,国内外在废旧锂离子电池资源化回收领域尚处于起步阶段,湿法回收是在废旧锂离子电池回收利用方法中应用最为广泛的方法,其可以针对电池容量损耗严重的废旧电池进行元素提取,回收有利用价值的再生资源,主要针对三元电池。
3.湿法回收是将镍钴锰酸锂三元粉料通过酸浸出、化学除杂、萃取深度除杂或分离镍钴锰,得到硫酸盐,含锂溶液加入碳酸钠蒸发浓缩得到碳酸锂。
4.wo2017/091562ai公开了将从报废锂离子电池中的得到的正极材料浸出溶解回收镍、钴、锰、锂等有价金属。通过调节溶液中摩尔比,进行共沉淀获得所需的正极材料前驱体。
5.申请号为cn200910304134的中国专利申请公开了采用浓度为2~4mol/l的硫酸+质量百分比为30%的双氧水,在硫酸溶液中还原过渡金属元素实现有价元素的提取。由于需要消耗大量双氧水使得该方法的成本大大提高。此外,该浸出过程中,有价元素li和过渡金属元素一同进入酸性溶液中,在后续提取及分离过渡金属元素过程中,li元素的夹带不可避免,使锂收率较低。
6.cn108011150a公开了采用真空炉将废旧三元电池粉料在高温下煅烧,得到镍钴金属及碳酸锂,通过通入二氧化碳水浸出碳酸锂来回收锂,该方法所用设备要求较高,难以实现工业化,同时后续镍钴回收酸浸出时会产生大量氢气,造成安全隐患。
7.因此,急需开发一种操作简单、易于工业应用的含钴废旧锂离子电池回收利用方法。
技术实现要素:
8.本发明是基于发明人对以下事实和问题的发现和认识做出的:目前的含钴废旧锂离子电池回收利用方法存在以下问题:1)将镍钴锰锂等有价金属同步还原浸出,需消耗大量双氧水或次氯酸钠等还原剂;后续各工序中每一步都存在锂的损失,造成最终锂的回收率仅能达到65
‑
70%左右;得到的碳酸锂为工业级碳酸锂,需要氢化提纯后方可得到高纯碳酸锂;2)产生大量含有负极碳的浸出渣,增加了处置成本;3)需要大量萃取工序,消耗有机试剂以及产生较多废水;4)对设备要求高,难以实现工业化规模生产。
9.本发明旨在至少在一定程度上解决相关技术中的技术问题之一。
10.为此,本发明实施例提出一种含钴废旧锂离子电池回收利用的方法,该方法能够大幅提高锂收率至95%,提高镍钴锰有价金属回收率至98%,降低了酸碱消耗且工艺流程
简单,适宜大规模工业化生产。
11.根据本发明实施例的一种含钴废旧锂离子电池回收利用方法,包括如下步骤:
12.a、向废旧锂离子电池回收粉料中加入氢氧化钠溶液,进行球磨,得到混合粉料;
13.b、将所述步骤a得到的混合粉料进行煅烧,得到煅烧粉料;
14.c、将所述步骤b得到的煅烧粉料与水混合,并通入co2,反应后过滤得到碳酸氢锂溶液及浸出渣。
15.根据本发明实施例的含钴废旧锂离子电池回收利用方法带来的优点和技术效果,1、本发明实施例的方法中采用了碳还原煅烧优先提锂的方式,解决了湿法回收中锂在各工序中损耗的问题,而且回收得到的碳酸锂纯度高,能够达到电池级标准;2、本发明实施例的方法中,采用了氢氧化钠湿法球磨,在球磨过程中氢氧化钠不仅可以除去杂质铝,还可以催化碳还原反应过程;3、本发明实施例的方法中,在碳还原煅烧中无需进行气氛保护,在节约保护气体使用量的同时降低了对设备的要求,制造成本低,易于规模化生产;4、本发明实施例的方法中,得到的浸出渣无负极碳,大幅降低了危废处置成本;5、采用本发明的含钴废旧锂离子电池回收利用方法,有价金属回收率高,锂收率可以达到90%以上,镍钴锰回收率可以达到98%。
16.在一些实施例中,所述步骤a中,所述含钴废旧锂离子电池选自钴酸锂、镍钴铝酸锂或镍钴锰酸锂中的至少一种。
17.在一些实施例中,所述步骤a中,所述氢氧化钠溶液浓度为1
‑
5mol/l;和/或,所述氢氧化钠溶液与废旧锂离子电池回收粉料的液固比为2
‑
5:1;和/或,球磨中球料比为5
‑
10:1,球磨时间为1
‑
3h。
18.在一些实施例中,所述步骤b中,所述煅烧为空气气氛,和/或,所述煅烧温度为500
‑
900℃,和/或,所述煅烧时间为1
‑
5h。
19.在一些实施例中,所述步骤c中,所述水与煅烧粉料的液固比为3
‑
10:1,和/或,所述反应时间为1
‑
3小时。
20.在一些实施例中,还包括步骤d,将所述步骤c得到的碳酸氢锂溶液加热,反应,经洗涤、烘干得到高纯碳酸锂。
21.在一些实施例中,所述步骤d中,所述反应温度为85
‑
95℃,和/或,所述反应时间为1
‑
2h。
22.根据本发明实施例的含钴废旧锂离子电池回收利用方法,其中,还包括如下步骤:
23.e、向所述步骤c得到的浸出渣中加入酸液浸出,得到浸出液;
24.f、向所述步骤e得到的浸出液中加入铁粉,反应,得到除铜后液;
25.g、向所述步骤f得到的除铜后液中加入硫酸钠、双氧水和碱液,反应,得到除铁铝后液;
26.h、向所述步骤g得到的除铁铝后液中加入萃取剂得到镍钴锰净化液。
27.在一些实施例中,所述步骤e中,所述酸液选自硫酸、盐酸或硝酸中的至少一种,和/或,所述酸液浓度为0.5
‑
2mol/l,和/或,所述浸出渣与酸液的固液比为1:3
‑
5,和/或,所述浸出温度为60
‑
80℃,浸出时间为2
‑
4h;和/或,所述步骤f中,所述铁粉加入量与浸出液中铜的摩尔比为(1
‑
3):1,和/或,所述反应温度为30
‑
80℃,和/或,所述反应时间为10
‑
60min。
28.在一些实施例中,所述步骤g中,所述硫酸钠浓度为20
‑
30g/l,和/或,所述碱液选
自氢氧化钠、氨水、氢氧化钾、氢氧化锂、碳酸钠、碳酸钾、碳酸铵、碳酸氢钠、碳酸氢钾或碳酸氢铵中的至少一种,和/或,所述反应温度为85
‑
95℃,反应时间为1
‑
2h;所述步骤h中,所述萃取剂为p204,体积分数为15
‑
25%,和/或,所述水相ph值为2
‑
4,和/或,所述有机相与水相体积比为0.2
‑
1:1。
附图说明
29.图1是本发明实施例的含钴废旧锂离子电池回收利用方法的工艺流程图;
30.图2是本发明实施例1得到的碳酸锂的xrd分析图。
具体实施方式
31.下面详细描述本发明的实施例,所述实施例的示例在附图中示出。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
32.如图1所示,根据本发明实施例的一种含钴废旧锂离子电池回收利用方法,包括如下步骤:
33.a、向废旧锂离子电池回收粉料中加入氢氧化钠溶液,进行球磨,得到混合粉料,优选地,氢氧化钠浓度为1
‑
5mol/l,氢氧化钠溶液与废旧锂离子电池回收粉料的液固比为2
‑
5:1,球料比为5
‑
10:1,球磨时间为1
‑
3h,所述含钴废旧锂离子电池选自钴酸锂、镍钴铝酸锂或镍钴锰酸锂中的至少一种,所述废旧锂离子电池回收粉料可以包括正极材料、负极碳粉、铜铝粉和铁等,只要回收粉料中含有c元素都可以采用发明实施例的方法对含钴废旧电池中的锂元素进行回收利用;
34.b、将所述步骤a得到的混合粉料进行煅烧,得到煅烧粉料,优选地,所述煅烧温度为500
‑
900℃,所述煅烧时间为1
‑
5h,煅烧反应方程式为:
35.4limeo2+c=2li2o+4meo+co236.其中,me为ni、co、mn及其混合物;
37.c、将所述步骤b得到的煅烧粉料与水混合,优选地,液固比为3
‑
10:1,并通入co2,优选地,反应温度为室温,反应时间为1
‑
3小时,反应后过滤得到碳酸氢锂溶液及浸出渣,发生的反应方程式如下:
38.li2o+2co2+h2o
→
2lihco339.li2co3+co2+h2o
→
2lihco3。
40.上述反应式中,li2co3部分来源于步骤b,步骤b得到的产物中含有氧化锂和二氧化碳,会有少量二氧化碳与氧化锂反应生成碳酸锂,该部分碳酸锂在步骤c中继续与通入的co2和水反应得到lihco3;另外,在步骤c中,氧化锂与水混合后生成氢氧化锂,氢氧化锂与二氧化碳气体优先反应生成碳酸锂,之后碳酸锂与二氧化碳、水继续反应生成碳酸氢锂。
41.本发明实施例的方法中,在球磨的过程中加入了氢氧化钠溶液,氢氧化钠湿法球磨可以起到如下作用:
42.1、去除废旧锂离子电池回收粉料中的铝,降低后续湿法除铁铝的负荷,使得到的碳酸锂纯度大幅提高,化学反应方程式为:
43.2al+2naoh+2h2o
→
2naalo2+3h2;
44.2、通过湿法球磨可以使limeo2和c充分接触混匀,增加两种反应物质接触,提高化
学反应率;
45.3、氢氧化钠对碳还原反应起到催化剂作用,催化机理如下:
46.2naoh+c
→
na2o+co+h247.2limeo2+co
→
li2o+2meo+co248.2limeo2+h2
→
li2o+2meo+h2o
49.na2o+h2o
→
2naoh
50.4limeo2+c=2li2o+4meo+co2。
51.根据本发明实施例的含钴废旧锂离子电池回收利用方法,采用了碳还原煅烧优先提锂的方式,解决了湿法回收中锂在各工序中损耗的问题,而且回收得到的碳酸锂纯度高,能够达到电池级标准;本发明实施例的方法中,采用了氢氧化钠湿法球磨,在球磨过程中氢氧化钠不仅可以除去杂质铝,还可以催化碳还原反应过程;本发明实施例的方法中,在碳还原煅烧中无需进行气氛保护,在节约保护气体使用量的同时降低了对设备的要求,制造成本低,易于规模化生产;本发明实施例的方法中,得到的浸出渣无负极碳,大幅降低了危废处置成本;采用本发明的含钴废旧锂离子电池回收利用方法,有价金属回收率高,锂收率可以达到95%,镍钴锰回收率可以达到98%。
52.在一些实施例中,还包括步骤d,将所述步骤c得到的碳酸氢锂溶液加热,反应,优选地反应温度为85
‑
95℃,反应时间为1
‑
2h,经洗涤、烘干得到高纯碳酸锂,发生的化学反应方程式如下:
53.2lihco3→
li2co3+co2+h2o。
54.在一些实施例中,还包括如下步骤:
55.e、向所述步骤c得到的浸出渣中加入酸液浸出,得到浸出液;
56.f、向所述步骤e得到的浸出液中加入铁粉,反应,得到除铜后液;
57.g、向所述步骤f得到的除铜后液中加入硫酸钠、双氧水和碱液,反应,得到除铁铝后液;
58.h、向所述步骤g得到的除铁铝后液中加入萃取剂得到镍钴锰净化液。
59.在一些实施例中,所述步骤e中,所述酸液选自硫酸、盐酸或硝酸中的至少一种,所述酸液浓度为0.5
‑
2mol/l,所述浸出渣与酸液的固液比为1:3
‑
5,所述浸出温度为60
‑
80℃,浸出时间为2
‑
4h,搅拌速率为200
‑
500r/min。本发明实施例的方法中,将浸出渣经过酸浸出处理,镍钴锰三价氧化物极难溶解,但是经所述步骤b煅烧后发生碳还原反应,三价镍钴锰被还原为二价,得到二价氧化物,而二价氧化物极易被酸溶解,使本发明实施例的方法中,在对浸出渣进行酸浸的过程中无需加入还原剂双氧水即可完成酸浸处理,浸出后得到含有镍、钴、锰、铝、铜、铁的浸出液,化学反应式为:
60.meo+h2so4→
meso4+h2o
61.其中,me表示镍、钴、锰、铝、铜或铁等金属离子。
62.在一些实施例中,所述步骤f中,所述铁粉加入量与浸出液中铜的摩尔比为(1
‑
3):1,所述反应温度为30
‑
80℃,所述反应时间为10
‑
60min。本发明实施例的方法中,向含有镍、钴、锰、铝、铜、铁的浸出液中加入铁粉除铜,过滤后得到除铜后液,反应方程式如下:
63.fe+cuso4→
feso4+cu。
64.在一些实施例中,所述步骤g中,所述硫酸钠浓度为20
‑
30g/l,所述碱液选自氢氧
化钠、氨水、氢氧化钾、氢氧化锂、碳酸钠、碳酸钾、碳酸铵、碳酸氢钠、碳酸氢钾或碳酸氢铵中的至少一种,所述反应温度为85
‑
95℃,反应时间为1
‑
2h。本发明实施例的方法中,向除铜后液中加入硫酸钠,缓慢加入适量双氧水,将二价铁离子氧化为三价铁离子,同步加入稀碱调整ph至1.5
‑
2.0,搅拌反应,反应温度为85
‑
95℃,反应时间为1
‑
2h,之后加入稀碱调整ph至3.0
‑
4.0,得到除铁铝后液,化学反应式为:
65.2feso4+h2o2+h2so4→
fe2(so4)3+2h2o
66.3fe2(so4)3+na2so4+12h2o
→
na2fe6(so4)4(oh)
12
(s)+6h2so467.al2(so4)3+6naoh
→
3na2so4+al(oh)3(s)。
68.在一些实施例中,所述步骤h中,所述萃取剂为p204,体积分数为15
‑
25%,皂化率为60
‑
75%,和/或,所述水相ph值为2
‑
4,和/或,所述有机相与水相体积比为0.2
‑
1:1。本发明实施例中,将除铁铝后液按一定相比经过逆流萃取后得到镍钴锰净化液,将该净化液按金属元素调配比可以制备不同型号的三元前驱体。
69.下面结合实施例和附图详细描述本发明。
70.实施例1
‑
3中所用废旧电池黑粉元素分析见表1。
71.表1
[0072] liconimnalfecuc实施例14.15%7.08%17.64%9.9%1.2%0.2%2%35%实施例22.85%2.4%5.1%15.2%0.98%0.2%0.2%30%实施例34.9%38.5%//1.5%0.3%1.2%33%
[0073]
实施例1
[0074]
称取废电池黑粉100g,加入2mol/l氢氧化钠200g,球料比为6:1,球磨1h后,压滤,将滤饼放入马弗炉中进行高温煅烧,煅烧温度为600℃,保温2h;煅烧后将黑粉加入300g水中,室温下通入2ml/min二氧化碳,并持续搅拌,反应1h,过滤得到碳酸氢锂滤液和水浸渣。
[0075]
将碳酸氢锂溶液于90℃反应1h,过滤洗涤烘干,得到碳酸锂20.5g,碳酸锂元素分析结果见表2,xrd分析见图2。
[0076]
将水浸渣加入300ml 1mol/l的稀硫酸溶液中,反应温度为60℃,搅拌速率为300r/min,反应2h后过滤,得到浸出液,ph=1.1;向浸出液中加入1mol/l氢氧化钠调整ph=1.8后,加入3g铁粉,在50℃下搅拌反应30min,过滤,得到除铜后液;除铜后液加入4g无水硫酸钠,搅拌并缓慢滴加20ml工业双氧水,反应温度为45℃,滴加时间为20min;升温至90℃,反应60min,待温度降至60℃以后,加入1mol/l氢氧化钠调整ph到3.5,将铁铝渣过滤,得到除铁铝后液;向除铁铝后液加入200ml皂化率65%的p204,控制水相平衡ph=3,经3级逆流萃取后得到镍钴锰净化液,镍钴锰净化液成分分析见表3。
[0077]
本实施例得到的碳酸锂回收率为92%,碳酸锂纯度为99.0%,镍钴锰回收率为98.3%。
[0078]
实施例2
[0079]
称取废电池黑粉1000g,加入1mol/l氢氧化钠3000g,球料比5:1,球磨2h后,压滤,将滤饼放入方形坩埚并盖好盖子后置于马弗炉中进行高温煅烧,煅烧温度700℃,保温1h;煅烧后将黑粉加入5000g水中,室温下通入30ml/min二氧化碳,并持续搅拌,反应2h,过滤得到碳酸氢锂滤液和水浸渣。
[0080]
将碳酸氢锂溶液于85℃反应2h,过滤洗涤烘干,得到碳酸锂142.5g,碳酸锂分析结果见表2。
[0081]
将水浸渣加入4000ml 0.5mol/l的稀硫酸溶液中,反应温度为70℃,搅拌速率为500r/min,反应3h后过滤,得到浸出液,ph=1.2;向浸出液中加入1mol/l氢氧化钠调整ph=1.5后,加入4g铁粉,在60℃搅拌反应20min,过滤,得到除铜后液;除铜后液加入30g无水硫酸钠,搅拌并缓慢滴加40ml工业双氧水,反应温度为30℃,滴加时间为30min;升温至95℃,反应120min,待温度降至50℃以后,加入1mol/l氢氧化钠调整ph到4.0,将铁铝渣过滤,得到除铁铝后液;向除铁铝后液加入2000ml皂化率60%的p204,控制水相平衡ph=2.8,经3级逆流萃取后得到镍钴锰净化液,镍钴锰净化液成分分析见表3。
[0082]
本实施例得到的碳酸锂回收率为93.5%,碳酸锂纯度为99.5%,镍钴锰回收率为98.5%。
[0083]
实施例3
[0084]
称取废电池黑粉100g,加入1mol/l氢氧化钠500g,球料比10:1,球磨3h后,压滤将滤饼放于马弗炉中进行高温煅烧,煅烧温度800℃,保温1h;煅烧后黑粉加入700g水中,室温下通入3ml/min二氧化碳,并持续搅拌,反应2h,过滤后得到碳酸氢锂滤液和水浸渣。
[0085]
将碳酸氢锂溶液于90℃反应1h,过滤洗涤烘干,得到碳酸锂24.5g,碳酸锂元素分析结果见表2。
[0086]
将水浸渣加入300ml 1mol/l的稀盐酸溶液中,反应温度为60℃,搅拌速率为500r/min,反应2h后过滤,得到浸出液,ph=1.3;加入1mol/l氢氧化钠调整ph=1.5后,加入3g铁粉,在30℃搅拌反应40min,过滤,得到除铜后液;除铜后液加入4g无水硫酸钠,搅拌并缓慢滴加15ml工业双氧水,反应温度50℃,滴加时间30min;升温至95℃,反应120min,待温度降至60℃以后,加入1mol/l氢氧化钠调整ph到4.0,将铁铝渣过滤,得到除铁铝后液;向除铁铝后液加入200ml皂化率65%的p204,控制水相平衡ph=3,经3级逆流萃取后得到镍钴锰净化液,镍钴锰净化液成分分析见表3。
[0087]
本实施例得到的碳酸锂回收率为93.1%,碳酸锂纯度为99.2%,镍钴锰回收率为98.3%。
[0088]
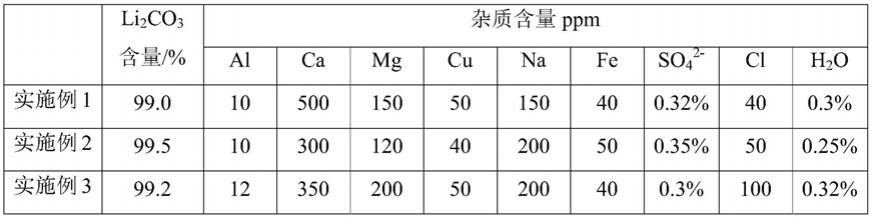
表2
[0089][0090]
表3
[0091][0092]
对比例1
[0093]
与实施例1的方法相同,不同之处在于,球磨过程中不加入氢氧化钠溶液。
[0094]
对比例1的方法得到碳酸锂13.25g,锂回收率为51%,碳酸锂纯度为85%。
[0095]
对比例2
[0096]
与实施例1的方法相同,不同之处在于,将废电池黑粉先进行球磨,球磨后加入氢氧化钠溶液除铝,压滤后再进行煅烧。
[0097]
对比例2的方法得到碳酸锂17.12g,锂回收率为69%,碳酸锂纯度为89%。
[0098]
在本发明中,术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0099]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1