硫化物型固体电解质、其制备方法和包含其的全固态电池与流程
硫化物型固体电解质、其制备方法和包含其的全固态电池
1.本发明专利申请是基于申请日为2017年1月12日,发明名称为“硫化物型固体电解质和应用其的全固态电池”,申请号为201780003777.5的中国专利申请的分案申请。
技术领域
2.本技术要求基于2016年1月12日提交的韩国专利申请第10-2016-0003514号和2017年1月12日提交的韩国专利申请第10-2017-0005605号的优先权,并通过引用的方式将其全部内容并入本文中。
3.本发明涉及含有硫化物型化合物的固体电解质和应用其的全固态电池。
背景技术:
4.从电池容量、安全性、功率输出、大型化、小型化等观点来看,目前正在研究能够克服锂二次电池的局限性的各种电池。
5.代表性地,学术界和工业界正在不断研究如下电池:在容量方面研究了金属-空气电池,其具有与锂二次电池相当的理论容量;在安全性方面研究了没有爆炸危险的全固态电池;在功率输出方面研究了超级电容器;在大型化方面研究了nas电池或rfb(氧化还原液流电池);在小型化方面研究了薄膜电池;等等。
6.其中,全固态电池是将常规锂二次电池中使用的液体电解质替换为固体电解质的电池,并且由于在电池中不使用可燃性溶剂,因此全固态电池可以显著提高安全性,且因此不会由于常规电解质溶液的分解反应而发生着火或爆炸。另外,存在以下优点:由于可以使用li金属或li合金作为负极材料,因此可以显著提高与电池的质量和体积相关的能量密度。
7.具体来说,全固态电池中使用的固体电解质中的无机固体电解质可以分为硫化物型电解质和氧化物型电解质。目前,最先进的固体电解质是硫化物型固体电解质,并且这种固体电解质的离子电导率已经发展到离子电导率接近于有机电解质溶液的水平。
8.但是,通常已知的是硫化物型固体电解质含有磷元素(p),并且与大气中的水分和氧气反应,导致性能急剧劣化。因此,由于在大气中的储存稳定性较低,所以难以进行处理,并且如以下反应式(1)所示通过与水反应而生成有毒气体如硫化氢(h2s),由此存在安全性和稳定性的问题:
9.[反应式1]
[0010]
技术实现要素:
[0011]
【技术问题】
[0012]
如上所述,大多数硫化物型固体电解质含有磷元素(p)并且显示10-3
s/cm至10-5
s/cm的高离子电导率,但存在与大气中的水分反应的问题。
[0013]
因此,本发明的一个目的是提供硫化物型固体电解质,其通过用另一种元素置换磷元素(p)而在保持高离子电导率的同时提高了安全性和稳定性。
[0014]
【技术方案】
[0015]
为了实现上述目的,本发明提供硫化物型固体电解质,其特征在于包含由以下通式1表示的锂-锡-金属-硫化物(ltms)型化合物:
[0016]
[通式1]
[0017]
liasnbmcsd[0018]
其中m以及a、b、c和d是本文中所定义的。
[0019]
另外,本发明提供所述硫化物型固体电解质的制备方法,其包括:
[0020]
i)将锂硫化物、锡硫化物和含m(其中m是选自属于元素周期表(iupac)的第4至6周期的元素中的第4族、第5族、第13族、第14族和第15族的元素(sn除外)中的至少一种金属)的硫化物混合;和
[0021]
ii)对所述混合物进行热处理。
[0022]
另外,本发明提供包含所述硫化物型固体电解质的全固态电池。
[0023]
【有益效果】
[0024]
根据本发明的硫化物型固体电解质和应用其的全固态电池,改善了对水分的反应性,防止了有毒气体如硫化氢(h2s)的产生,提高了安全性和稳定性,并且即使在空气中放置后离子电导率也不降低,并且所述固体电解质由于其改善的贮存稳定性而易于进行处理和储存。
附图说明
[0025]
图1是表示本发明的liasnbmcsd中可用的元素(m)(sn除外)的周期表。
[0026]
图2是通过比较本发明的liasnbmcsd中各元素(m)的形成能而获得的数据。
[0027]
图3是通过比较本发明的liasnbmcsd中的各元素(m)的晶格体积而获得的数据。
[0028]
图4是通过比较本发明的liasnbmcsd中的各元素(m)的带隙能量而获得的数据。
[0029]
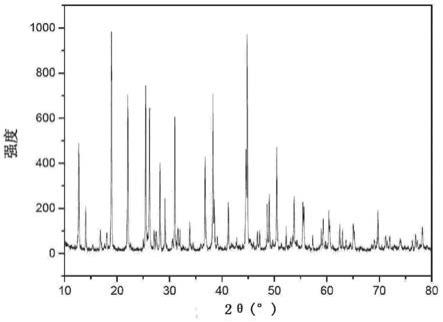
图5是本发明的实施例1制备的li
13
sn2ins
12
的xrd结果。
具体实施方式
[0030]
在下文中,将参照附图详细说明本发明以使本领域技术人员可以容易地实施本发明。然而,本发明可以以许多不同的形式来实施,并且不限于此。
[0031]
锂-锡-金属-硫化物型化合物
[0032]
通常,本领域中使用的硫化物型固体电解质由li-p-s或li-p-x-s(其中x是除p以外的金属元素)构成,因此含有磷元素(p)。然而,由于因磷元素(p)而导致的诸如产生有毒气体的安全性和稳定性问题,本发明旨在提供新的锂-锡-金属-硫化物(ltms:锂-锡-金属-硫化物)作为固体电解质,所述新的锂-锡-金属-硫化物一定含有锂(li)和硫(s)但不含磷元素(p)。
[0033]
ltms是在锂-锡-硫化物(lts)的基本晶体结构中被金属m部分置换的结构,并且优选由以下通式1表示:
[0034]
[通式1]
[0035]
liasnbmcsd[0036]
其中m是选自属于元素周期表(iupac)的第4至6周期的元素中的第4族、第5族、第13族、第14族和第15族的元素(sn除外)中的至少一种金属,并且0《a≤20,0《b≤5,0《c≤5且0《d≤20。
[0037]
通式1中所说明的m可以通过图1的周期表(iupac)确认。更具体地,元素m可以是选自由如下元素构成的组中的至少一种:过渡金属如锆(zr)、铌(nb)、铪(hf)和钽(ta),后过渡金属如镓(ga)、铟(in)、铊(tl)、铅(pb)和铋(bi),类金属如锗(ge)、砷(as)和锑(sb)。
[0038]
例如,这些元素m具有3至5个价电子,因此可通过与硫元素(s)化学键合而产生形态(m-s),并且这种形态(m-s)形成阴离子并且因此与金属阳离子如锂(li)形成电化学键(li
+
(m-s)-)。这些化合物允许锂阳离子(li
+
)的迁移。
[0039]
在本发明中,置换磷元素(p)的元素m必须能够通过与锂(li)和硫(s)合成而形成化合物,并且优选的是其离子电导率优异并且是电绝缘体,以用作全固态电池的固体电解质。因此,为了在下面的实验例中通过虚拟模拟确认上述条件是否得到满足,选择了十三种能够置换在室温下具有10-5
s/cm的离子电导率的li4sns4中的sn位点的元素(as(iii)、ga(iii)、in(iii)、sb(iii)、bi(iii)、pb(iv)、zr(iv)、hf(iv)、ce(iv)、as(v)、nb(v)、ta(v)、sb(v)),然后对其形成能、晶格体积和带隙能量进行模拟,并且这些值是基于密度泛函理论(dft(密度泛函理论),gga-pbe)得到的。
[0040]
形成能
[0041]
对用上述13种候选元素置换的锂-锡-金属-硫化物型化合物的结构模型进行了模拟,并且对各原子进行了形成焓(δh)的计算。可以说,在温度为0k且压力为0下的焓(δh)是优化网格模型中的总能量。在本发明中,使用标准生成焓来确定相对值,但是本发明不限于此。
[0042]
因此,模拟了作为固体电解质候选物的、用上述13种元素置换的化合物的形成能。所得数据示于图2中。结果,以作为置换前的化合物的li4sns4(lss)为基准,具有较低形成能的元素种类在形成化合物时具有更稳定的能级,因此可以置换sn位点。因此,从计算化学方
面来说,当基于li4sns4(lss)的形成能具有负值时,所述元素是可以自发地被置换和良好地合成的元素。可以确定满足这些条件的元素是ga(iii)、in(iii)、sb(iii)、bi(iii)、zr(iv)、hf(iv)、ce(iv)和ta(v)。
[0043]
晶格体积
[0044]
与液体中不同,固相中的离子的转移通过晶格中有限的路径进行。通常,固体电解质的离子电导率低于液体电解质的离子电导率。然而,对于一些固体,据报道离子电导率在理论上高于液体的离子电导率,并且测量或预测固体电解质的离子电导率对于全固态二次电池是重要的,因为电解质的离子电导率是决定电池的充放电速率以及输出速率的重要因素。
[0045]
这种固相中的离子迁移机制是由缺陷引起的离子点缺陷(ionic point defect)或晶格缺陷(lattice defect)、以及静电吸引和排斥为主要因素。离子点缺陷可以分为由阳离子/阴离子对形成空位的肖特基(schottky)缺陷和由不同位置的一对间隙原子形成空位的弗伦克尔(frenkel)缺陷。
[0046]
肖特基缺陷是原本应该存在于晶格点中的原子不存在的状态,并且该原子空位被称为攻击点。这意味着晶体中的一个原子离开其原始位置而存在于晶体表面上。此外,弗伦克尔缺陷是由于另一个原子插入构成晶格的原子的晶格之间的间隙而引起的缺陷,也就是由于从肖特基缺陷离开的原子插入晶格之间而引起的缺陷。
[0047]
晶格体积是指如上所述的晶格缺陷在这种固体电解质中的空间,并且这样的空间在晶格之间形成三维通道,并且通过将阳离子置于这样的通道中可实现离子传导。
[0048]
作为通过各元素进行置换的结果,整个骨架结构得到保持,但晶格体积发生变化。晶格体积越大,更适合于离子迁移的通道形成得越多,由此提高离子电导率(h.aono和e.sugimoto,“与锂盐(li3po4或li3bo3)混合的liti2(po4)3的电性质和烧结性(electrical property and sinterability of liti2(po4)3mixed with lithium salt(li3po
4 or li3bo3))”solid state ionics(固态离子学),47,257(1991))。
[0049]
因此,对作为固体电解质候选物的、用上述13种元素置换的化合物的晶格体积进行了模拟,并且所得数据示于图3中。在基于li4sns4(lss)(即置换前的化合物)的晶格体积具有较高晶格体积的化合物的情况下,由于当li离子扩散时的活化能趋于降低,因此可以说离子电导率也高。因此,可以预期离子电导率将大于li4sns4(lss)的10-5
s/cm的离子电导率。在上述13种元素中,当用除ga(iii)和as(v)以外的11种元素置换时,显示晶格体积大。特别是,当用其中的in(iii)、sb(iii)、bi(iii)或ce(iv)元素置换时,可以预期具有高的离子电导率。
[0050]
带隙能量
[0051]
带隙也称为能隙,是指存在电子的最高能级与不存在电子的最低能级之间的能级或能量差。绝缘体或半导体的带隙通常是指价电子带的最高部分与导带的最低部分之间的能量差,并且以电子伏特(ev)表示。这是将核周围的外层电子传送到自由状态所需的能量,并且可以预测,带隙大小越大,绝缘性越好。
[0052]
因此,对作为固体电解质候选物的、用13种元素置换的化合物的带隙能量进行了模拟,并且所得数据示于图4中。随着带隙变大,其具有优异的电绝缘性,可以稳定地用作固体电解质,并且具有宽的工作电压范围。考虑到li4sns4(lss)的带隙是2ev,可以认为,当被
带隙高于2ev的元素置换时,可以产生稳定的化合物。已显示,当利用作为满足这些条件的元素的ga(iii)、in(iii)、zr(iv)、hf(iv)、nb(v)、ta(v)置换时,带隙与参考值(即li4sns4(lss)的带隙)类似,因此确定其具有绝缘特性并且可以用作固体电解质。
[0053]
作为综合考虑形成能、晶格体积和带隙能量的结果,显示形成能为0ev以下、晶格体积为以上并且带隙能量为2ev以上均得到满足的三种元素in(iii)、zr(iv)和ta(v)对于可合成性、离子电导率和电绝缘性而言都是优异的。因此,确定这些元素适合用作硫化物型固体电解质中磷元素(p)的替代物。
[0054]
这些锂-锡-金属-硫化物型化合物可以制成几纳米到几千微米范围内的平均粒度。另外,关于形态,没有特别限制,但平均粒径优选在0.1μm至50μm的范围内。
[0055]
纳米级粒度容易扩大与通常的活性材料的接触面积,这可以通过扩大锂离子的传输路径而成为充放电的有利条件,因此具有纳米级粒度是有利的。
[0056]
锂-锡-金属-硫化物型化合物的制备方法
[0057]
本发明中提出的通式1的锂-锡-金属-硫化物型化合物的制备方法可以根据已知的锂-锡-金属-硫化物型化合物的制备方法来制备。
[0058]
通常,所述锂-锡-金属-硫化物型化合物通过包括以下步骤的方法来制备:i)将锂硫化物、锡硫化物和含m的硫化物混合;和ii)对所述混合物进行热处理。
[0059]
在下文中,将详细说明各步骤。
[0060]
首先,将粉末形态的锂硫化物、锡硫化物和含m的硫化物混合,以制备混合粉末。
[0061]
锂硫化物在本发明中不受特别限制,并且可以选择和使用已知物质。通常,可以是li2s、li2s2等,并且优选使用li2s。
[0062]
锡硫化物在本发明中不受特别限制,并且可以选择和使用已知的材料。通常,可以是sns2、sns等,并且优选使用sns2。
[0063]
作为含m的化合物,可以根据m的种类使用各种材料,例如,当m是in、zr或ta时,可以使用in2s3、zrs3、ta2s3等。
[0064]
在这种情况下,根据最终的锂-锡-金属-硫化物型化合物的摩尔比,可以以各种方式控制锂硫化物、锡硫化物和含m的硫化物的含量比,并且在本发明中对其没有特别限制。
[0065]
混合可以通过干式或湿式混合方法进行,并且在本发明中没有特别限制。
[0066]
通过用于常规混合粉末生产的方法进行混合,并且可以进行机械研磨以进行均匀颗粒混合。对于机械研磨,例如可以使用辊磨机、球磨机或喷磨机。混合可以进行1小时至8小时,优选1小时至6小时。
[0067]
接着,将对上述步骤中获得的混合粉末进行热处理以制造锂-锡-金属-硫化物型化合物。
[0068]
该步骤中的热处理优选在400℃至850℃的温度范围内进行约1分钟至约60分钟,具体地为1分钟至30分钟,更特别地为1分钟至10分钟。
[0069]
热处理可以进行至少一次,并且可以在包括第一热处理和第二热处理的两个步骤中进行,并且在这种情况下,当第二热处理在比第一热处理中的温度高的温度下进行时,有利于锂-锡-硫化物型化合物的颗粒形成和制造。
[0070]
在这种情况下,如果热处理的温度低于上述范围,则锂-锡-金属-硫化物型化合物的制备本身可能变得困难。相反,如果热处理的温度超过上述范围,则锂-锡-金属-硫化物
型化合物的颗粒变大,由此离子电导率可能降低,或者制造均匀大小的颗粒可能变得困难。
[0071]
全固态电池
[0072]
本发明的上述锂-锡-金属-硫化物型化合物可以优选用作全固态电池的固体电解质。
[0073]
所述全固态电池包含正极、负极和置于其间的固体电解质。
[0074]
本发明的锂-锡-金属-硫化物型化合物具有高的离子电导率并且同时不产生有毒气体,由此可以确保与其它常规硫化物型固体电解质相同或更高的物理性能。
[0075]
由锂-锡-金属-硫化物型化合物形成的固体电解质层的厚度根据全固态电池的结构而有很大不同。然而,例如,其优选为0.1μm以上且1mm以下,并且更优选为1μm以上且100μm以下。固体电解质优选具有高锂离子电导率,并且例如室温下的锂离子电导率优选为1
×
10-4
s/cm以上。
[0076]
在这种情况下,除了锂-锡-金属-硫化物型化合物之外,固体电解质还可包含全固态电池中通常使用的固体电解质。例如,可以使用无机固体电解质或有机固体电解质。
[0077]
在无机固体电解质的情况下,可以使用陶瓷材料、结晶材料或无定形材料,并且可以使用无机固体电解质如硫代-lisicon(li
3.25
ge
0.25
p
0.75
s4)、li2s-sis2、lii-li2s-sis2、lii-li2s-p2s5、lii-li2s-p2o5、lii-li3po
4-p2s5、li2s-p2s5、li3ps4、li7p3s
11
、li2o-b2o3、li2o-b2o
3-p2o5、li2o-v2o
5-sio2、li2o-b2o3、li3po4、li2o-li2wo
4-b2o3、lipon、libon、li2o-sio2、lii、li3n、li5la3ta2o
12
、li7la3zr2o
12
、li6bala2ta2o
12
、li3po
(4-3/2w)
nw(其中w为w《1)和li
3.6
si
0.6
p
0.4
o4。
[0078]
此外,有机固体电解质的实例包括通过将锂盐与聚合物材料如聚乙烯衍生物、聚环氧乙烷衍生物、聚环氧丙烷衍生物、磷酸酯聚合物、聚海藻酸盐赖氨酸、聚酯硫化物、聚乙烯醇和聚偏二氟乙烯混合制备的有机固体电解质。在这种情况下,这些可以单独使用或以至少一种的组合形式使用。
[0079]
同时,用于本发明的全固态电池的正极和负极不受特别限制,并且可以使用已知的正极和负极。
[0080]
在本发明中提出的全固态电池限定了如上所述的固体电解质的构成,并且构成电池的其它元件即正极和负极在本发明中不受特别限制并且遵循下面的说明。
[0081]
全固态电池用负极是单独的锂金属,或者可以将负极活性材料层压在负极集电器上。
[0082]
在这种情况下,负极集电器不受特别限制,只要其是导电的并且不在全固态电池中引起任何化学变化即可,并且可以使用例如铜,不锈钢,铝,镍,钛,烧结碳,表面用碳、镍、钛、银等处理后的铜或不锈钢,或者铝-镉合金等。另外,与正极集电器一样,负极集电器也可包括各种形式,例如在表面上形成有微细凹凸的膜、薄片、箔、网状物、多孔体、泡沫体和无纺布。
[0083]
负极活性材料可以是选自由锂金属、锂合金、锂金属复合氧化物、含锂的钛复合氧化物(lto)以及它们的组合构成的组中的任何一种。在这种情况下,锂合金可以是锂与选自na、k、rb、cs、fr、be、mg、ca、sr、ba、ra、al和sn中的至少一种金属的合金。此外,锂金属复合氧化物是锂和选自由si、sn、zn、mg、cd、ce、ni和fe构成的组中的任何一种金属(me)的氧化物(meo
x
),并且例如可以是lixfe2o3(0《x≤1)或lixwo2(0《x≤1)。
[0084]
另外,负极活性材料可以是金属复合氧化物,例如sn
x
me
1-x
me'yoz(me:mn、fe、pb、ge;me':al,b,p,si,周期表第1、2和3族的元素,卤素;0《x≤1;1≤y≤3;1≤z≤8);氧化物如sno、sno2、pbo、pbo2、pb2o3、pb3o4、sb2o3、sb2o4、sb2o5、geo、geo2、bi2o3、bi2o4和bi2o5,以及碳基负极活性材料如结晶碳、无定形碳或碳复合物,可以单独使用或以两种以上的组合形式使用所述负极活性材料。
[0085]
本发明的全固态电池用正极不受特别限制,并且可以是用于已知的全固态电池的材料。
[0086]
正极集电器不受特别限制,只要其具有高导电性并且不在相关电池中引起化学变化即可,并且可以使用例如不锈钢,铝,镍,钛,烧结碳,或者表面用碳、镍、钛、银等处理过的铝或不锈钢。
[0087]
正极活性材料可以根据锂二次电池的用途而改变,并且可以使用锂金属氧化物如lini
0.8-x
co
0.2
alxo2、lico
x
mnyo2、lini
x
coyo2、lini
x
mnyo2、lini
x
coymnzo2、licoo2、linio2、limno2、lifepo4、licopo4、limnpo4和li4ti5o
12
;硫属化合物如cu2mo6s8、fes、cos和nis,以及钪、钌、钛、钒、钼、铬、锰、铁、钴、镍、铜、锌的氧化物、硫化物或卤化物,并且更具体来说可以使用tis2、zrs2、ruo2、co3o4、mo6s8、v2o5等,但本发明不限于此。
[0088]
正极活性材料的形状不受特别限制,并且可以是颗粒形状,例如球形、椭圆形、矩形等。正极活性材料的平均粒径可以(但不限于)在1μm至50μm的范围内。正极活性材料的平均粒径例如可以通过利用扫描电子显微镜观察测量活性材料的粒径并计算其平均值而获得。
[0089]
包含在正极中的粘结剂不受特别限制,并且可以使用诸如聚偏二氟乙烯(pvdf)和聚四氟乙烯(ptfe)的含氟粘结剂。
[0090]
粘结剂的含量不受特别限制,只要其能够固定正极活性材料即可,并且以整个正极计,可以在0重量%至10重量%的范围内。
[0091]
正极还可包含导电材料。导电材料不受特别限制,只要它们能够提高正极的电导率即可,并且其实例可包括镍粉、钴氧化物、钛氧化物和碳。碳的实例可包括选自由科琴黑、乙炔黑、炉黑、石墨、碳纤维和富勒烯构成的组中的任何一种或者一种以上。
[0092]
在这种情况下,可以考虑电池的其它条件如导电材料的类型来选择导电材料的含量,并且例如可以相对于整个正极在1重量%至10重量%的范围内。
[0093]
具有如上所述构造的全固态电池的制备在本发明中不受特别限制,但可通过已知方法进行。
[0094]
例如,将固体电解质置于正极与负极之间,接着压缩成型以组装电池。
[0095]
将组装好的电池置于壳中并通过热压等密封。由铝、不锈钢等制成的层压包装以及圆柱形或正方形金属容器非常适合作为外包装材料。
[0096]
本发明的电池包含在本发明中提出的锂-锡-金属-硫化物型固体电解质作为成分,由此具有优异的充放电特性。尽管仅由固体构成的全固态电池能够防止爆炸等安全事故,因此是具有优异安全性的最终电池形式但全固态电池尚未得到广泛应用,这是因为它们尚未实现高容量和高功率。其主要原因是电解质的材料特性。
[0097]
通过包含本发明中提出的锂-锡-金属-硫化物型化合物作为固体电解质的成分,可以确保优异的电池特性。
[0098]
在下文中,说明本发明的优选实施例和比较例。然而,以下实施例只是本发明的优选实施例,并且本发明不限于以下实施例。
[0099]
实施例1:li
13
sn2ins
12
的合成
[0100]
为了合成本发明的li
13
sn2ins
12
(即其中m是in的li
4-x
sn
1-xmx
s4化合物),将li2s、sns2和in2s3以5:2:1的摩尔比进行混合。在这种情况下,通过将sn和s以1:2的摩尔比混合并在400℃下热处理来制备sns2。取样总共5g样品,并且通过使用cip来制备颗粒,然后在保持真空的同时将试样密封在石英管中,并且在600℃下充分热处理20小时以上,获得li
13
sn2ins
12
。
[0101]
实验例1:xrd结果
[0102]
对实施例1中制备的固体电解质进行x射线衍射分析(xrd)以确认其结晶度。结果示于图5中。
[0103]
如图5所示,确定实施例1的固体电解质颗粒与li4sns4的晶体结构类似,并且部分峰由于铟(in)置换而偏移。
[0104]
因此,本发明的全固态电池更安全并且具有高的能量密度,由此可以优选用作可再生能源或电动车辆电源的替代物。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1