一种三相复合包覆的富锂锰基正极材料及其制备方法和应用与流程
1.本发明涉及锂离子电池技术领域,特别涉及一种al2o3/alf3/lialf4三相复合包覆的富锂锰基正极材料及其制备方法和应用。
背景技术:
2.近些年我国新能源汽车取得了飞速发展,同时也迎来了由量向质的发展方向转变。研究开发新一代300-400wh/kg动力锂电池,是未来锂电材料在政策红利逐步退出的同时还能保持核心竞争力的必然要求。因此寻找具有高容量同时生产成本较低的正极材料成为电池行业发展的关键。
3.在已知正极材料中,富锂锰基正极材料放电比容量达250mah/g以上,远高于现阶段商业化动力电池中的高镍三元和磷酸铁锂正极材料;同时这种材料中低廉锰元素含量高,与常用的钴酸锂和镍钴锰三元系正极材料相比,不仅容量高、成本低,而且安全性好。尽管富锂锰基正极材料被视为下一代锂动力电池的理想之选,然而目前还存在一些问题限制其商业化,比如,首周循环库伦效率较低、循环过程中放电电压滞后和衰减问题、循环稳定性较差以及倍率性能较差。
4.目前,作为改善材料的电化学性能和缓解电压衰减的有效途径,表层在富锂锰基正极材料中逐步受到广泛应用。目前,对于表面包覆的作用机理主要可以分为以下几类:(1)物理屏障,抑制副反应;(2)清除hf,防止电解质的化学侵蚀,减轻过渡金属溶解;(3)提升电子和离子导电;(4)表面化学改性,促进界面离子电荷转移;(5)稳定结构,减轻相变应力。在实际应用过程中,某些表面包覆会阻碍离子扩散,但提供其他优势,而某些包覆可以增强离子扩散,但损害其他性能,因此多元多组分包覆成为研究的重点。然而多次包覆虽然提高了性能,但是相对的导致了制备方法繁琐,成本高,如何在提高性能的同时降低生产成本仍然是一项挑战。
5.中国专利cn111710866a公开了一种核壳结构富锂锰基复合正极材料,该发明通过将镍盐、钴盐、酸液和水混合搅拌后得到的混合溶液与富锂锰基正极氧化物粉末混合形成混合悬浊液,使得富锂锰基体相的表面形成含有尖晶石相包覆层的次外层,从而保证内核中尖晶石纳米缺陷分布均匀而又不过度生长,然后将混合悬浊液干燥后得到第一粉末,第一粉末与有机碳源混合后进行过滤、洗涤和干燥后进行非氧化煅烧,进而形成无定形碳的最外层,该最外层能够提升正极材料的电子导电能力和形成保护作用,由此提高正极材料的循环性能。该专利技术存在制备方法繁琐、成本高等缺点,难以应用于商业化生产中。
6.中国专利cn112310351a公开了一种具有双氧化物符合包覆层的富锂锰基正极材料,该正极材料的表面具有由氧化铝和氧化硅组成的复合包覆层,能够抑制副反应发生,阻碍电解液对电极的侵蚀,提高了正极材料的首次库伦效率,改善了循环稳定性和倍率性能。然而,该复合氧化物包覆层导电性差,其会明显正极材料的电子导电能力。
技术实现要素:
7.本发明的发明目的在于:针对上述存在的问题,提供一种三相复合包覆的富锂锰基正极材料及其制备方法和应用,本发明的正极材料表面的包覆层由内向外依次形成有金属氧化物al2o3、金属氟化物alf3和快离子导体lialf4,可以稳定富锂氧化物正极材料中的氧晶格和氧变价反应,提升材料循环性能,包覆层中金属氧化物al2o3作为hf的清除剂,可以抑制过渡金属的溶解,提高层状结构稳定性,金属氟化物alf3充当物理屏障,不参与电化学反应,阻止电极和电解液直接接触发生副反应,快离子导体lialf4具有高锂离子电导率,能够改善正极/电解质界面的电荷转移,提高材料结构,提升倍率性能,本发明的制备方法操作简单、成本低,能够避免引入杂质以及避免出现组分偏差等问题,克服了现有技术中所存在的不足。
8.本发明采用的技术方案如下:一种三相复合包覆的富锂锰基正极材料,所述富锂锰基正极材料表面的包覆层由内向外依次由al2o3、alf3、lialf4组成,所述al2o3、alf3、lialf4三者的质量比为60-80:10-20:5-20。在上述中,al2o3、 alf3、lialf4三者的具体质量比根据实际需求来确定,例如其可以为60:20:20、65:20:15、70:15:15、75:15:10、80:10:10、75:20:5、70:20:10等。
9.在本发明中,包覆层中金属氧化物al2o3作为hf的清除剂,可以抑制过渡金属的溶解,提高层状结构稳定性,金属氟化物alf3充当物理屏障,不参与电化学反应,阻止电极和电解液直接接触发生副反应,快离子导体lialf4具有高锂离子电导率,能够改善正极/电解质界面的电荷转移,提高正极材料结构的稳定性,提升其倍率性能,三合一复合包覆层产生了协同效应,兼顾电化学稳定性、化学稳定性、较高的锂离子电导率并实现了优势互补,材料一致性好,克服了现有技术所存在的不足。
10.在本发明中,所述包覆层的厚度为5-10nm。包覆层的厚度不宜过大或过小,包覆层过厚则增大非活性物质比例,会降低比容量和能量密度;包覆层过薄则不利于均匀包覆,会降低包覆层的改善效果。通过试验总结得到,包覆层的厚度在5-10nm最为合适,例如厚度可以为5nm、6nm、6.5nm、7nm、7.5nm、8nm、 8.5nm、9nm、9.5nm、10nm等。
11.在本发明中,所述富锂锰基正极材料的化学式为xli2mno3·
(1-x)limo2,其中,m为过渡金属ni、mn、co中的一种或多种,x的取值范围为0《x《1。
12.进一步,所述富锂锰基正极材料的颗粒粒径为5-20μm,其可以是5μm、6 μm、7μm、9μm、10μm、11μm、13μm、15μm、16μm、18μm、20μm 等。
13.本发明还包括一种al2o3/alf3/lialf4三相复合包覆的富锂锰基正极材料的制备方法,包括以下步骤:
14.s1、将铝盐加入醇溶液中,搅拌均匀后,加入富锂锰基正极材料,搅拌混合均匀,得到悬浮液;
15.s2、将含氟盐和锂盐均匀分散于醇水混合溶液中(li、al、f生成lialf4,剩余f参与生成alf3,剩余al参与生成al2o3),其中f与li的摩尔比大于4,得到混合醇溶液;
16.s3、将混合醇溶液加入悬浮液中,混合搅拌均匀,并滴加氨水调节混合溶液ph值至7.5-8.5,然后蒸发得到粉末;
17.s4、对粉末进行真空干燥和研磨处理,然后置于马弗炉中于300-500℃煅烧 3-5h,即得。
18.在本发明的制备方法中,铝盐、含氟盐和锂盐的加入顺序比较重要,本发明先将铝盐与富锂锰基正极材料混合,以在正极材料颗粒的表面沉积铝盐,然后在f与li的摩尔比大于4的情况下(摩尔比一般为5-10:1),再在铝盐表面先后沉积出alf3和lialf4,如果改变铝盐、含氟盐和锂盐的加入顺序,则难以得到本发明设计的结构。同时,f与li的摩尔比也比较重要,如果f与li的摩尔比小于4,则不会得到lialf4组分,或者说lialf4组分生成量不足,最后也难以得到本发明设计的结构。本发明的制备方法通过湿法包覆的方式实现了多元化合物的复合包覆,制备方法简单可靠,需要控制的工艺参数少,产品质量稳定,得到的材料一致性好,制备过程安全性高且对环境友好,克服了现有技术在制备复合包覆层时所存在的步骤繁琐、成本高等问题。
19.在本发明中,所述铝盐为alcl3、alno3、al2(so4)3中的至少一种。进一步,在s1的悬浮液中,al离子浓度为20-50mmol/l。若al离子浓度过高,则生成的复合包覆层厚度较大,进而降低复合材料能量密度;反之,若al离子浓度过低,则生成的复合包覆层完整性和均一性会较差,导致包覆效果受到限制,通过试验总结得到,al离子浓度为20-50mmol/l最为合适,例如其浓度可以为 20mmol/l、25mmol/l、30mmol/l、35mmol/l、36mmol/l、37mmol/l、40mmol/l、 45mmol/l、50mmol/l等。
20.在本发明中,所述富锂锰基正极材料的浓度为0.05-0.1g/ml。富锂锰基正极材料的浓度不宜过大或过小,浓度过大不利于均匀包覆,浓度过小则不利于大规模制备,会产生较多废液,富锂锰基正极材料的浓度在上述数值范围内最为合适。进一步,加入富锂锰基正极材料搅拌混合时,混合温度为50-70℃。
21.在本发明中,所述含氟盐为lif或/和nh4f。相应地,所述锂盐为lif、lino3、 licl中的至少一种。进一步,所述f的浓度为10-20mmol/l,所述li的浓度为 2-4mol/l。
22.进一步,在s3中,混合搅拌的温度为50-70℃,混合搅拌至溶剂(即醇水混合溶液,醇水混合溶液中乙醇和水体积比为6-9:1-4,优选为8:2)全部挥发,得到粉末。
23.本发明还包括一种al2o3/alf3/lialf4三相复合包覆的富锂锰基正极材料在锂离子电池中的应用,所述富锂锰基正极材料作为锂离子电池的正极材料使用。
24.综上所述,由于采用了上述技术方案,本发明的有益效果是:
25.1、在本发明中的复合包覆层中,金属氧化物al2o3(由铝盐沉积物煅烧后形成)可以作为hf的清除剂,进而抑制过渡金属的溶解,提高层状结构稳定性;金属氟化物alf3则可以充当物理屏障,其不参与电化学反应,能够阻止电极和电解液直接接触发生副反应;快离子导体lialf4具有高锂离子电导率,能够改善正极/电解质界面的电荷转移,进而提高正极材料结构的稳定性,提升锂离子电池的倍率性能;三种化合物复合包覆层彼此之间产生协同效应,兼顾电化学稳定性、化学稳定性、较高的锂离子电导率,并实现了优势互补,克服了现有技术所存在的不足;
26.2、本发明al2o3/alf3/lialf4复合包覆的富锂锰基正极材料,在充/放电过程中同时存在过渡金属氧化还原与晶格氧氧化还原,复合包覆层有助于改善富锂材料的表面稳定性,提升富锂材料的界面离子电导率,提高循环稳定性而且没有损失富锂材料的倍率性能;
27.3、本发明的复合包覆层中al2o3作为导电隔层,有效阻止了副产物的堆积,减少了充放电循环过程中产生的热量,同时可以有效抑制相变,提高晶体结构的稳定性;alf3可抑制电解液与电极的接触,抑制副反应发生,提升富锂材料的循环稳定性;lialf4有助于促进
的锂离子传输,有效地提高了富锂锰基正极材料颗粒之间和电极本身的离子传导和电子传导;
28.4、本发明的制备方法通过湿法包覆的方式实现了多元化合物的复合包覆,制备方法简单可靠,需要控制的工艺参数少,产品质量稳定,得到的材料一致性好,制备过程安全性高且对环境友好,克服了现有技术在制备复合包覆层时所存在的步骤繁琐、成本高等问题。
附图说明
29.图1为实施例1中制备的复合包覆的富锂锰基正极材料的x射线光电子能谱图 (xps);
30.图2为实施例1中制备的复合包覆的富锂锰基正极材料的能量色散x射线光谱(eds)面扫能谱图;
31.图3为实施例2中制备的复合包覆的富锂锰基正极材料的x射线光电子能谱图 (xps);
32.图4为实施例2中制备的复合包覆的富锂锰基正极材料的能量色散x射线光谱 (eds)面扫能谱图;
33.图5为实施例3中制备的复合包覆的富锂锰基正极材料的x射线光电子能谱图 (xps);
34.图6为实施例3中制备的复合包覆的富锂锰基正极材料的能量色散x射线光谱 (eds)面扫能谱图;
35.图7为实施例4中制备的复合包覆的富锂锰基正极材料的扫描电子显微镜 (tem)图;
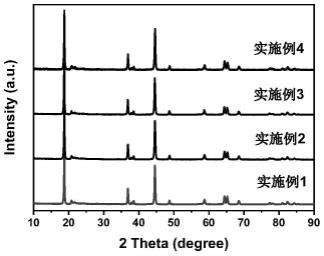
36.图8为实施例1-4中制备的复合包覆的富锂锰基正极材料的x射线衍射测试 (xrd)图;
37.图9为实施例1-4中制备的复合包覆的富锂锰基正极材料组装的电池在0.1c倍率下首周充放电图;
38.图10实施例1-4中制备的复合包覆的富锂锰基正极材料组装的电池在1c倍率下循环性能图;
39.图11实施例1-4中制备的复合包覆的富锂锰基正极材料组装的电池在1c倍率下电压衰减图;
40.图12实施例1-4中制备的复合包覆的富锂锰基正极材料组装的电池在不同倍率下的倍率性能图。
具体实施方式
41.下面结合附图,对本发明作详细的说明。
42.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明,其中,所述方法如无特别说明均为常规方法,所述原材料如无特别说明均能从公开商业途径而得。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
43.以下实施例中:高分辨透射电子显微镜(hrtem)测试:使用的透射电子显微镜是日本电子株式会社jem-2100f;
44.粉末x射线衍射(xrd)测试:使用的x射线衍射仪是日本理学公司生产的iv-185型号衍射仪;
45.x射线光电子能谱(xps)测试:使用的x射线光电子能谱仪是美国热电生产的thermo escalab 250xi;
46.cr2025钮扣电池的组装:将实施例和对比例制备的富锂锰基正极材料作为活性材料,将活性材料与乙炔黑、pvdf(聚偏氟乙烯)按照8:1:1的质量比混合,加入nmp研磨为浆料,用刮刀涂覆在铝箔上,进行烘干,裁片制成正极片;然后在氩气手套箱(水<0.01ppm,氧<0.01ppm)中组装成cr2025型扣式半电池,其中正极即为上述正极片,对电极为锂片,隔膜为celgard 2500,电解液是以体积比为1:1:1的碳酸二甲酯、碳酸二乙酯、碳酸乙酯为溶剂,以1mol/l 的lipf6为溶质制成的溶液。
47.实施例1
48.一种al2o3/alf3/lialf4复合包覆的富锂锰基正极材料,其包括如下制备步骤:
49.s1、将5mmol的alno3分散在100ml乙醇溶液中搅拌均匀,进一步加入10g共沉淀法制备的富锂锰基正极材料li
1.2
ni
0.2
mn
0.6
o2,然后置于磁力搅拌器上,于50℃下混合搅拌均匀分散;
50.s2、将2mmol的nh4f和0.4mmol的lino3分散在100ml乙醇水混合溶液中(乙醇和水体积比为8:2)搅拌均匀,逐滴加入到s1制备的混合溶液中,同时置于磁力搅拌器上,于50℃下混合搅拌均匀,并逐滴滴加氨水调节至混合溶液ph值稳定至7.5,继续置于磁力搅拌器上,于50℃混合搅拌至溶液全部挥发;
51.s3、将蒸干后所得粉末置于真空烘箱中,于80℃真空干燥过夜后研磨,然后在马弗炉中于500℃下高温煅烧3h,得到al2o3/alf3/lialf4复合包覆的富锂锰基正极材料。
52.所制备的复合包覆的富锂锰基正极材料颗粒分布均匀,大小均在10-15μm 之间,包覆层厚度为8nm。根据图1的xps图可知,复合包覆层由 al2o3/alf3/lialf4组成,三者含量(以包覆层总质量分数为100%计算)分别为 65.5%,19.7%,14.8%。根据图2中的eds图可知,所制备的复合包覆层没有明显改变材料的形态,f、al均匀地分散在材料表面,表明al2o3/alf3/lialf4三合一复合包覆层均匀包覆在材料表面。根据图8的xrd图可知,表明合成材料的层状结构具有很高的结晶度,但由于包覆量水平较低,未达到检测所需的包覆量,因此未找到对应的al2o3/alf3/lialf4包覆层的衍射峰。
53.将所制备的复合包覆的富锂锰基正极材料组装成cr2025钮扣电池进行电化学性能测试。如图9所示,首次0.1c倍率下活化测试截止电压为2v-4.8v (1c=250mah/g),活化容量为255.6mah/g,库伦效率为76.4%。进一步对其进行循环性能测试,其中测试截止电压为2v-4.6v。如图10示,1c倍率循环 100周后(1c=250mah/g)容量保持率为80.9%,表明复合包覆具有更好的循环稳定性。如图11示,循环100周后电压衰减为0.31v,表明复合包覆不会牺牲材料的电压稳定性。如图12示,5c倍率时容量可达155.3mah/g,包覆后倍率性能的提升主要归因于al2o3/alf3/lialf4复合包覆层具有良好的li
+
导电性,即使在大电流密度下仍然可以实现快速的li
+
脱嵌。
54.实施例2
55.一种al2o3/alf3/lialf4复合包覆的富锂锰基正极材料,其包括如下制备步骤:
56.s1、将2mmol的alcl3分散在100ml乙醇溶液中搅拌均匀,进一步加入 5g共沉淀法制备的富锂锰基正极材料li
1.2
ni
0.2
mn
0.6
o2,然后置于磁力搅拌器上,于70℃下混合搅拌均匀分散;
57.s2、将1mmol的nh4f和0.2mmol的licl3分散在100ml乙醇水混合溶液中(乙醇和水体积比为8:2)搅拌均匀,逐滴加入到s1制备的混合溶液中,同时置于磁力搅拌器上,于70℃下混合搅拌均匀,并逐滴滴加氨水调节至混合溶液ph值稳定至8.5,继续置于磁力搅拌器上,于70℃混合搅拌至溶液全部挥发;
58.s3、将蒸干后所得粉末置于真空烘箱中,于80℃真空干燥过夜后研磨,然后在马弗炉中于500℃下高温煅烧3h,得到al2o3/alf3/lialf4复合包覆的富锂锰基正极材料。
59.所制备的复合包覆的富锂锰基正极材料颗粒分布均匀,大小均在10-15μm 之间,包覆层厚度为5nm。根据图3的xps图可知,复合包覆层由 al2o3/alf3/lialf4组成,三者含量(以包覆层总质量分数为100%计算)分别为 69.2%,12.1%,18.7%。根据图4中的eds图可知,所制备的复合包覆层没有明显改变材料的形态,f、al均匀地分散在材料表面,表明al2o3/alf3/lialf4复合包覆层均匀包覆在材料表面。根据图8的xrd图可知,表明合成材料的层状结构具有很高的结晶度,但由于包覆量水平较低,未达到检测所需的包覆量,因此未找到对应的al2o3/alf3/lialf4包覆层的衍射峰。
60.将所制备的复合包覆的富锂锰基正极材料组装成cr2025钮扣电池进行电化学性能测试。如图9,首次0.1c倍率下活化测试截止电压为2v-4.8v(1c=250 mah/g),活化容量为245.9mah/g,库伦效率为75.4%。进一步进行循环性能测试,其中测试截止电压为2v-4.6v。如图10示,1c倍率循环100周后(1c=250 mah/g)容量保持率为88.8%,表明复合包覆具有更好的循环稳定性。如图11 示,循环100周后电压衰减为0.22v,表明复合包覆不会牺牲材料的电压稳定性。如图12示,5c倍率时容量可达161.1mah/g,包覆后倍率性能的提升主要归因于al2o3/alf3/lialf4复合包覆层具有良好的li
+
导电性,即使在大电流密度下仍然可以实现快速的li
+
脱嵌。
61.实施例3
62.一种al2o3/alf3/lialf4复合包覆的富锂锰基正极材料,其包括如下制备步骤:
63.s1、将5mmol的alno3分散在100ml乙醇溶液中搅拌均匀,进一步加入 10g共沉淀法制备的富锂锰基正极材料li
1.2
ni
0.2
mn
0.6
o2,然后置于磁力搅拌器上,于70℃下混合搅拌均匀分散;
64.s2、将2mmol的nh4f和0.4mmol的lino3分散在100ml乙醇水混合溶液中(乙醇和水体积比为8:2)搅拌均匀,逐滴加入到s1制备的混合溶液中,同时置于磁力搅拌器上,于60℃下混合搅拌均匀,并逐滴滴加氨水调节至混合溶液ph值稳定至7.5,继续置于磁力搅拌器上,于60℃混合搅拌至溶液全部挥发;
65.s3、将蒸干后所得粉末置于真空烘箱中,于80℃真空干燥过夜后研磨,然后在马弗炉中于300℃下高温煅烧5h,得到al2o3/alf3/lialf4复合包覆的富锂锰基正极材料。
66.所制备的复合包覆的富锂锰基正极材料颗粒分布均匀,大小均在10-15μm 之间,包覆层厚度为7nm。根据图5的xps图可知,复合包覆层由al2o3/alf3/lialf4组成,三者含量(以包覆层总质量分数为100%计算)分别为 68.6%,17.1%,14.4%。根据图6中的eds图可
知,所制备的复合包覆层没有明显改变材料的形态,f、al均匀地分散在材料表面,表明al2o3/alf3/lialf4复合包覆层均匀包覆在材料表面。根据图8中的xrd图可知,表明合成材料的层状结构具有很高的结晶度,但由于包覆量水平较低,未达到检测所需的包覆量水平,因此未找到对应的al2o3/alf3/lialf4包覆层的衍射峰。
67.将所制备的复合包覆的富锂锰基正极材料组装成cr2025钮扣电池进行电化学性能测试。如图9,首次0.1c倍率下活化测试截止电压为2v-4.8v(1c=250 mah/g),活化容量为248.5mah/g,库伦效率为73.9%。进一步进行循环性能测试,其中测试截止电压为2v-4.6v。如图10示,1c倍率循环100周后(1c=250 mah/g)容量保持率为89.1%,表明复合包覆具有更好的循环稳定性。如图11 示,循环100周后电压衰减为0.19v,表明复合包覆不会牺牲材料的电压稳定性。如图12示,5c倍率时容量可达152.7mah/g,改性后倍率性能的提升主要归因于al2o3/alf3/lialf4复合包覆层具有良好的li
+
导电性,即使在大电流密度下仍然可以实现快速的li
+
脱嵌。
68.实施例4
69.一种al2o3/alf3/lialf4复合包覆的富锂锰基正极材料,其包括如下制备步骤:
70.s1、将5mmol的alno3分散在100ml乙醇溶液中搅拌均匀,进一步加入 10g共沉淀法制备的富锂锰基正极材料li
1.2
ni
0.2
mn
0.6
o2,然后置于磁力搅拌器上,于50℃下混合搅拌均匀分散;
71.s2、将2mmol的nh4f和0.2mmol的lino3分散在100ml乙醇水混合溶液中(乙醇和水体积比为8:2)搅拌均匀,逐滴加入到s1制备的混合溶液中,同时置于磁力搅拌器上,于60℃下混合搅拌均匀,并逐滴滴加氨水调节至混合溶液ph值稳定至7.5,继续置于磁力搅拌器上,于60℃混合搅拌至溶液全部挥发;
72.s3、将蒸干后所得粉末置于真空烘箱中,于80℃真空干燥过夜后研磨,然后在马弗炉中于300℃下高温煅烧3h,得到al2o3/alf3/lialf4复合包覆的富锂锰基正极材料。
73.根据图7的tem图可知,al2o3/alf3/lialf4复合包覆层均匀包覆在材料表面,厚度大约为10nm。根据图7的xps图可知,复合包覆层由al2o3/alf3/lialf4组成。根据图8中的xrd图可知,表明合成材料的层状结构具有很高的结晶度,但由于包覆量水平较低,未达到检测所需的包覆量水平,因此未找到对应的 al2o3/alf3/lialf4包覆层的衍射峰。
74.将所制备的复合包覆的富锂锰基正极材料组装成cr2025钮扣电池进行电化学性能测试。如图9所示,首次0.1c倍率下活化测试截止电压为2v-4.8v (1c=250mah/g),活化容量为242.7mah/g,库伦效率为72.1%。进一步进行循环性能测试,其中测试截止电压为2v-4.6v。如图10所示,1c倍率循环100 周后(1c=250mah/g)容量保持率为88.3%,表明复合包覆具有更好的循环稳定性。如图11所示,循环100周后电压衰减为0.26v,表明复合包覆不会牺牲材料的电压稳定性。如图12所示,5c倍率时容量可达146.3mah/g,改性后倍率性能的提升主要归因于al2o3/alf3/lialf4复合包覆层具有良好的li
+
导电性,即使在大电流密度下仍然可以实现快速的li
+
脱嵌。
75.对比例1
76.对比例1与实施例1相同,其不同之处在于,将alno3与nh4f和lino3共混后,滴加入含有li
1.2
ni
0.2
mn
0.6
o2正极材料的乙醇溶液中。
77.试验结果:首次0.1c倍率下活化测试截止电压为2v-4.8v(1c=250 mah/g),活化
容量为235.8mah/g,库伦效率为70.1%。进一步进行循环性能测试,其中测试截止电压为2v-4.6v,1c倍率循环100周后(1c=250mah/g) 容量保持率为82.3%,循环100周后电压衰减为0.31v,5c倍率时容量仅为 126.8mah/g。改性后性能较差原因主要有两点:(1)nh4f直接与li
1.2
ni
0.2
mn
0.6
o2正极材料接触,nh4f溶液呈酸性,会与富锂锰基正极材料产生“h-li”置换作用,导致表面结构破坏;(2)同时混合后复合包覆层组分比例改变,导致包覆效果受到限制。
78.对比例2
79.对比例2与实施例1相同,其不同之处在于,nh4f的添加量为0.8mmol。
80.试验结果:首次0.1c倍率下活化测试截止电压为2v-4.8v(1c=250 mah/g),活化容量为243.6mah/g,库伦效率为74.1%。进一步进行循环性能测试,其中测试截止电压为2v-4.6v,1c倍率循环100周后(1c=250mah/g) 容量保持率为83.3%,循环100周后电压衰减为0.26v,5c倍率时容量仅为 133.5mah/g。改性后性能较差原因主要有两点:(1)nh4f添加量较少导致复合包覆层中alf3组分含量较少,alf3具有良好的抗氟化功效,较少的alf3组分含量不利于改善循环稳定改性;(2)nh4f添加量较少导致复合包覆层中lialf4组分含量较少,lialf4组分具有良好的离子迁移效率,较少的lialf4组分含量不利于改善倍率性能。
81.对比例3
82.对比例3与实施例1相同,其不同之处在于,alno3与nh4f和lino3用量较多,得到的包覆层的厚度约为18nm。
83.试验结果:首次0.1c倍率下活化测试截止电压为2v-4.8v(1c=250 mah/g),活化容量为231.2mah/g,库伦效率为71.6%。进一步进行循环性能测试,其中测试截止电压为2v-4.6v,1c倍率循环100周后(1c=250mah/g) 容量保持率为86.3%,循环100周后电压衰减为0.27v,5c倍率时容量仅为 124.7mah/g。改性后循环稳定性得到部分提升,主要是由于较厚包覆层具有良好的保护效果。然而包覆层不具有电化学活性,较厚的包覆层导致非活性组分增大,因此放电比容量显著降低不利于实际应用。
84.以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1