包括视网膜下递送治疗有效量的重组AAV9衍生载体的在对象的视锥细胞光感受器中表达目的多核苷酸的方法与流程
本发明涉及一种重组aav9衍生载体(aav9-derivedvector),并涉及其应用,特别是在对象的视锥细胞光感受器中表达目的多核苷酸的方法,所述方法包括视网膜下递送治疗有效量的重组aav9衍生载体。
背景技术:
位于黄斑中心的中央凹是视网膜的一个专门区域,其通过提供高度敏锐的色觉来主导灵长类动物的视觉感知(1)。发现在中央凹的中心(距中央凹中心<0.3mm)处视锥细胞密度最高,但缺乏视杆细胞光感受器(2)。视锥细胞密度随着距中央凹的距离降低多达100倍(3)。中央凹中的视锥细胞是旨在治疗遗传性视网膜疾病如中期色素性视网膜炎(4,5)和全色盲(6)的基因疗法的主要靶标。目前,为了向视锥细胞提供基因递送,需要将编码治疗蛋白的病毒载体注射到光感受器和视网膜色素上皮(rpe)细胞之间的视网膜下空间中。在这种方法中,用常规aav(即aav2)进行基因传递限于与注入流体局部“小泡(bleb)”接触的细胞。此外,视网膜下注射期间发生的视网膜脱离在具有视网膜变性的眼睛中是一种隐患。最早的临床试验是在leber先天性黑蒙症患者(7–9)中利用视网膜下递送腺相关病毒(aav)来递送健康的rpe65基因,该试验尽管为了递送病毒载体而使黄斑脱离,但带来一定的视力改善(10,11)。然而,该治疗在某些情况下并发黄斑裂孔并在中央凹下注射的情况下增加了黄斑变薄(11)。此外,与周边区域相反,在中央凹中没有治疗益处(12)。还研究了对无脉络膜症患者使用aav的基因疗法,其中黄斑是基因递送的靶标(13)。迄今为止,来自这后一项研究的6个月随访结果提示,中央凹下视网膜脱离并不会导致该区域中视力下降,但是,该试验中一名患者的经治疗的眼睛与他的未经治疗的眼睛相比较,有视觉敏锐度损失(13)。随着更多的基因疗法到达临床应用阶段,越来越需要找到将基因疗法递送到中央凹而不使该脆弱的区域脱离的新方法(14)。这可以通过使用横向扩散以到达中央凹区域的载体在周边进行视网膜下注射来实现。
技术实现要素:
本发明涉及一种重组aav9衍生的载体,并涉及其应用,包括在对象的视锥细胞光感受器中表达目的多核苷酸的方法,所述方法包括视网膜下递送治疗有效量的重组aav9衍生载体。特别地,本发明由权利要求书限定。
在第一方面,本发明涉及一种用于治疗影响视锥细胞光感受器的视网膜疾病的重组aav9衍生载体,所述载体包含:
-vp1衣壳蛋白,其中相对于相应的野生型aav9衣壳蛋白,在所述衣壳蛋白的gh环中插入了7至11个氨基酸长度的肽,其中所述肽包含seqidno:1至seqidno:8中的任一个;和
-在如seqidno:12所示的pr1.7启动子或所述启动子的功能变体控制下的目的多核苷酸。
优选地,相对于如seqidno:10所示的野生型aav9衣壳蛋白,所述肽被插入gh环中氨基酸588和589之间。
优选地,所述肽包含seqidno:9或由seqidno:9组成。
优选地,所述重组aav9衍生载体包含如seqidno:11所示的vp1衣壳蛋白和在如seqidno:12所示的pr1.7启动子控制下的目的多核苷酸。
优选地,由重组aav9衍生载体治疗的对象患有选自下列的视网膜疾病:年龄相关性黄斑变性,bassen-kornzweig综合征,无脉络膜症,回旋状萎缩,refsum综合征,usher综合征,色盲,蓝色视锥细胞单色视(blueconemonochromacy),全色盲,不完全性全色盲,寡视锥细胞三色视觉(oligoconetrichromacy),色素性视网膜炎(rp),黄斑变性,stargardt病,bardet-biedl综合征,bornholm眼病,best病,和leber先天性黑蒙症。
优选地,所述目的多核苷酸是可用于基因替代疗法的基因,优选选自编码色素性视网膜炎gtp酶调节因子(rpgrorf15)、cngb3(视锥细胞环核苷酸门控阳离子通道的β亚基)、cnga3(视锥细胞环核苷酸门控阳离子通道的α亚基)或gnat2的基因。
优选地,所述目的多核苷酸编码神经营养因子。更优选地,所述目的多核苷酸编码rdcvf、rdcvf2、rdcvfl或rdcvfl2。
优选地,所述目的多核苷酸编码视蛋白,例如视紫红质、光视蛋白、l/m波长(红/绿)视锥细胞视蛋白、或短波长(s)视锥细胞视蛋白(蓝)。更优选地,所述目的多核苷酸编码由如seqidno:13、seqidno:14或seqidno:15所示的氨基酸序列组成的视蛋白。
优选地,所述目的多核苷酸编码提供基因功能的位点特异性敲除的位点特异性核酸内切酶,所述核酸内切酶选自锌指核酸酶(zfn)、转录激活因子样效应子核酸酶(talen)和crispr相关核酸内切酶。更优选地,所述目的多核苷酸编码cas9核酸酶。
优选地,所述目的多核苷酸编码干扰rna(rnai),特别是sirna或shrna。
优选地,所述目的多核苷酸编码反义寡核苷酸。
优选地,所述治疗包括视网膜下递送治疗有效量的重组aav9衍生载体。
优选地,所述视网膜下递送在中央凹的一定距离处进行,不会使所述区域脱离。
在另一方面,本发明涉及一种重组aav9衍生载体,所述载体包含:
-vp1衣壳蛋白,其中相对于相应的野生型aav9衣壳蛋白,在所述衣壳蛋白的gh环中插入了7至11个氨基酸长度的肽,其中所述肽包含seqidno:1至seqidno:8中的任一个;和
-在如seqidno:12所示的pr1.7启动子或所述启动子的功能变体控制下的目的多核苷酸。
优选地,所述肽如上所述。
优选地,所述重组aav9衍生载体包含如seqidno:11所示的vp1衣壳蛋白和在如seqidno:12所示的pr1.7启动子控制下的目的多核苷酸。
优选地,所述目的多核苷酸如上所述。
在另一方面,本发明涉及一种在对象的视锥细胞光感受器中表达目的多核苷酸的方法,所述方法包括视网膜下递送治疗有效量的所述重组aav9衍生载体。
具体实施方式
我们对于在灵长类动物眼睛的视网膜下空间的解剖学独特环境内aav转导模式的了解上的缺口阻碍了在临床中建立向中央凹视锥细胞的无创而有效的基因递送。在此,本发明人建立了几种新的载体-启动子组合以克服与中央凹中aav介导的视锥细胞转导相关的局限性,并在小鼠模型、人类诱导多能干细胞衍生的类器官、人类死后视网膜外植体和活猕猴中进行了支持性研究。他们表明,aav9变体当被注入距中央凹几毫米远的视网膜下空间中时,提供了有效的中央凹视锥细胞转导,且不会使这个脆弱的区域脱离。这种递送方式依赖于视锥细胞特异性启动子,并导致与光遗传学视力恢复相容的高水平转基因表达。
因此,本发明的第一个目的涉及一种重组aav9衍生载体,所述载体包含:
-vp1衣壳蛋白,其中相对于相应的野生型aav9衣壳蛋白,在所述衣壳蛋白的gh环中插入了7至11个氨基酸长度的肽,其中所述肽包含seqidno:1至seqidno:8中的任一个;和
-在如seqidno:12所示的pr1.7启动子或所述启动子的功能变体控制下的目的多核苷酸。
特别地,所述重组aav9衍生载体可以包含如seqidno:11所示的vp1衣壳蛋白和在如seqidno:12所示的pr1.7启动子控制下的目的多核苷酸。
本发明的另一个目的涉及一种在对象的视锥细胞光感受器中表达目的多核苷酸的方法,所述方法包括视网膜下递送治疗有效量的本发明的重组aav9衍生载体。
如本文所用的术语“对象”通常旨在用于人类。通常,对象患有或可能患有影响视锥细胞光感受器的视网膜疾病。这样的视网膜疾病可直接或间接影响视锥细胞光感受器。因此,鉴于本文提供的教示,可以由此治疗影响视网膜视锥细胞光感受器的多种多样的视网膜疾病,所述视网膜疾病通常包括:年龄相关性黄斑变性,bassen-kornzweig综合征,无脉络膜症,回旋状萎缩,refsum综合征,usher综合征,色盲,蓝色视锥细胞单色视,全色盲,不完全性全色盲,寡视锥细胞三色视觉,色素性视网膜炎(rp),黄斑变性,stargardt病,bardet-biedl综合征,bornholm眼病,best病,和leber先天性黑蒙症。
因此,本发明的另一个目的是提供一种在有此需要的对象中治疗影响视锥细胞光感受器的视网膜疾病的方法,所述方法包括视网膜下递送治疗有效量的本发明的重组aav9衍生载体。在这个方面,当在视锥细胞光感受器中表达时,所述目的多核苷酸,特别是在如seqidno:12所示的pr1.7启动子控制下的,对所述视网膜疾病具有有益的效果,特别是能够治疗所述疾病。
本发明还涉及本发明的重组aav9衍生载体用于治疗影响视锥细胞光感受器的视网膜疾病。特别地,本发明涉及所述重组aav9衍生载体在制备用于治疗影响视锥细胞光感受器的视网膜疾病的药物中的用途。如上所述,优选地,所述治疗包括视网膜下递送治疗有效量的重组aav9衍生载体,并且所述目的多核苷酸能够治疗所述视网膜疾病。
如本文所用的术语“治疗”是指预防性或防预性治疗以及治愈性或疾病缓解性治疗,包括对有染病风险或怀疑已染病的患者以及生病或已诊断为患有疾病或医疗状况的患者的治疗,并包括抑制临床复发。所述治疗可以施用于有医学病症或最终可能获得该病症的对象,以预防、治愈、延缓病症或复发性病症的发作、减轻其严重程度、或改善其一种或多种症状。“治疗方案”是指疾病的治疗方式,例如治疗期间所用的剂量给药模式。治疗方案可以包括诱导方案和维持方案。短语“诱导方案”或“诱导期”是指用于疾病的初始治疗的治疗方案(或治疗方案的一部分)。诱导方案的一般性目标是在治疗方案的初始期期间为患者提供高药物水平。诱导方案可以(部分或全部)采用“负荷方案”,所述负荷方案可以包括施用的药物剂量比维持方案期间医生将采用的更高、施用的药物频率比维持方案期间医生将施用的更高、或二者兼而有之。短语“维持方案”或“维持期”是指在疾病治疗期间用于维持患者、例如使患者长时期(几个月或几年)保持缓解的治疗方案(或治疗方案的一部分)。维持方案可以采用连续疗法(例如,定期例如每周、每月、每年等施用药物)或间歇性疗法(例如,间断治疗,间歇治疗,复发治疗,或达到特定的预定标准[例如,疾病表现等]后的治疗)。
如本文所用的术语“视锥细胞光感受器”具有其在本领域中的一般含义,并且是哺乳动物眼睛的视网膜中三种类型的光感受器细胞之一。它们负责色觉,并且在相对明亮的光下功能最佳,而视杆细胞则相反,视杆细胞在暗光下工作更好。特异性载体和pr1.7启动子(或所述启动子的功能变体)之间的组合特异性驱动所述目的多核苷酸在视锥细胞光感受器中的表达。
如本文所用的术语“视网膜下递送”是指将载体施用到视网膜下空间中,这是指视网膜中光感受器细胞和视网膜色素上皮细胞之间的位置。视网膜下递送导致形成“小泡”,“小泡”是指在眼睛的视网膜下空间内充满液体的囊袋。本发明的小泡可以通过将流体单次注射到单个空间中、通过将一种或多种流体多次注射到相同的空间中、或通过多次注射到多个空间中而生成,它在重新定位时生成用于在视网膜下空间的目标部分上达到治疗效果的总流体空间。
根据本发明,所述视网膜下递送在中央凹的一定距离处进行,这意味着在离中央凹中心大于或等于0.5毫米处形成小泡,没有使该脆弱区域脱离。如本文所用的术语“中央凹”具有其在本领域中的一般含义,是指在灵长类动物的视网膜中央直径大约等于或小于0.5mm的一个小区域,该区域仅含视锥细胞光感受器,并且有整个视网膜中最高的视锥细胞密度。
如本文所用的术语“目的多核苷酸”在本文中是指编码出于任何种类的原因希望在靶细胞中表达的任何多肽、结构蛋白、酶等的任何核苷酸序列。它也可以是指非编码序列,例如反义序列或旨在降低基因表达的干扰rna序列。本领域技术人员通过其领域中科学文献的知识知道,哪些多核苷酸可更适合于治疗特定的视网膜疾病。
基因疗法可以通过在视锥细胞光感受器中引入在其中有缺陷的目的多核苷酸(例如基因)的功能拷贝来进行(基因替代疗法),或者通过向视锥细胞光感受器递送将会对要治疗的眼病具有有益效果的目的多核苷酸来进行(对症疗法)。换句话说,所述目的多核苷酸优选能够治疗影响视锥细胞光感受器的视网膜疾病。可用于基因替代治疗的目的多核苷酸的例子是在视锥细胞光感受器中特异性或优先表达的基因,例如色素性视网膜炎gtp酶调节因子(rpgrorf15)(参考:1.b.s.pawlyk,o.v.bulgakov,x.sun,m.adamian,x.shu,a.j.smith,e.l.berson,r.r.ali,s.khani,a.f.wright,m.a.sandberg,t.li,x连锁色素性视网膜炎小鼠模型中通过简缩的人类rpgr基因对光感受器的拯救(photoreceptorrescuebyanabbreviatedhumanrpgrgeneinamurinemodelofx-linkedretinitispigmentosa).genether23,196-204(2016).;2.d.h.hong,b.s.pawlyk,m.adamian,m.a.sandberg,t.li,单一简缩rpgr-orf15变体在体内重构了rpgr功能(asingle,abbreviatedrpgr-orf15variantreconstitutesrpgrfunctioninvivo).investophthalmolvissci46,435-441(2005).;3.w.a.beltran,a.v.cideciyan,a.s.lewin,w.w.hauswirth,s.g.jacobson,g.d.aguirre,由rpgr中的突变引起的x连锁色素性视网膜炎的基因增强(geneaugmentationforx-linkedretinitispigmentosacausedbymutationsinrpgr).coldspringharborperspectivesinmedicine5,a017392(2014).;4.w.t.deng,f.m.dyka,a.dinculescu,j.li,p.zhu,v.a.chiodo,s.l.boye,t.j.conlon,k.erger,t.cossette,w.w.hauswirth,aav载体治疗rpgr-orf15x连锁色素性视网膜炎的稳定性和安全性(stabilityandsafetyofanaavvectorfortreatingrpgr-orf15x-linkedretinitispigmentosa).humgenether26,593-602(2015).5.z.wu,s.hiriyanna,h.qian,s.mookherjee,m.m.campos,c.gao,r.fariss,p.a.sieving,t.li,p.colosi,a.swaroop,基因替代疗法对rpgr相关的视网膜变性的长期疗效研究(along-termefficacystudyofgenereplacementtherapyforrpgr-associatedretinaldegeneration).hummolgenet24,3956-3970(2015).;6.w.a.beltran,a.v.cideciyan,a.s.lewin,s.iwabe,h.khanna,a.sumaroka,v.a.chiodo,d.s.fajardo,a.j.román,w.-t.deng,m.swider,t.s.alemán,s.l.boye,s.genini,a.swaroop,w.w.hauswirth,s.g.jacobson,g.d.aguirre,proc.natl.acad.sci.u.s.a.(2012),109卷,2132-2137页)、cngb3(视锥细胞环核苷酸门控阳离子通道的β亚基)(例如,参见,kohl等人(2005)eurjhumgenet.13(3):302)、gnat2(转导蛋白的视锥细胞特异性α亚基)和cnga3(视锥细胞环核苷酸门控阳离子通道的α亚基)(参见,例如,genbank登录号np_001289;以及booij等人(2011)ophthalmology118:160-167)。
在一些实施方式中,所述目的多核苷酸可编码神经营养因子。如本文所用的“神经营养因子”是具有诸如神经细胞的存活和维持、促进神经元分化等生理作用的蛋白的通用术语。在一些实施方式中,神经营养因子是rdcvf。如本文所用的术语“rdcvf”具有其在本领域中的一般含义,并且是指视杆细胞源性视锥细胞生存力因子(rod-derivedconeviabilityfactor)(léveillardt,
在一些实施方式中,目的多核苷酸产物是视蛋白。视蛋白序列可以源自于任何合适的单细胞或多细胞生物,包括人类、藻类和细菌。在一些实施方式中,视蛋白是视紫红质、光视蛋白、l/m波长(红/绿)视锥细胞蛋白或短波长(s)视锥细胞视蛋白(蓝)。在一些实施方式中,视蛋白是通道视紫红质或盐细菌视紫红质或十字视紫红质(cruxhalorhodopsin)。在一些实施方式中,视蛋白是如下列文献中所述的光响应性视蛋白:美国专利公布no.2007/0261127(例如chr2;chop2);美国专利公布no.2001/0086421;美国专利公布no.2010/0015095;以及diester等人(2011)nat.neurosci.14:387。视蛋白的其他例子包括:nphr,enphr1.0,enphr2.0,enphr3.0,swichr,swichr2.0,swichr3.0,mac,mac3.0,arch,archt,arch3.0,archt3.0,ichr,chr2,c1v1-t,c1v1-tt,chronos,chrimson,chrimsonr,catch,vchr1-sfo,chr2-sfo,chr2-ssfo,chef,chief,jaws,chloc,slowchloc,ic1c2,ic1c22.0,和ic1c23.0。在一些实施方式中,视蛋白由如seqidno:13或seqidno:14或seqidno:15所示的氨基酸序列组成。
在一些实施方式中,目的多核苷酸产物是位点特异性核酸内切酶,其提供基因功能的位点特异性敲除,例如,其中所述核酸内切酶敲除与视网膜疾病相关的等位基因。例如,在显性等位基因编码缺损的基因拷贝,而该基因在野生型时是视网膜结构蛋白和/或提供正常的视网膜功能的情况下,位点特异性核酸内切酶可以靶向该缺损等位基因并敲除该缺损等位基因。在一些实施方式中,所述载体因此包含编码位点特异性核酸内切酶的多核苷酸;和编码缺损等位基因的功能拷贝的多核苷酸,其中所述功能拷贝编码功能性视网膜蛋白。适合使用的位点特异性核酸内切酶包括,例如,锌指核酸酶(zfn);转录激活因子样效应物核酸酶(talen),和crispr相关的核酸内切酶。如本文所用的术语“crispr相关的核酸内切酶”具有其在本领域中的一般含义,并且是指相关的簇状规则间隔的短回文重复,它们是含有碱基序列短重复的原核dna片段。如本领域中公知的,crispr相关的核酸内切酶可以与小向导rna(grna)和/或同源介导修复(hdr)模板相关。特别地,本发明的crispr相关的核酸内切酶是cas9或其衍生物。cas9核酸酶可具有与野生型化脓性链球菌(streptococcuspyrogenes)或金黄色葡萄球菌(staphylococcusaureus)序列同一(identical)的核苷酸序列,优选与野生型化脓性链球菌同一。或者,可以修饰野生型化脓性链球菌或金黄色葡萄球菌cas9序列。例如,cas9核酸酶序列可以是包含在可商购的载体例如出自addgene(cambridge,ma)的px330或px260内的序列。在一些实施方式中,cas9核酸内切酶可以具有作为genbank登录号km099231.1gl669193757、km099232.1、gl669193761、cp032481、lt996890、cp031130、cp022607、ap014942或km099233.1gl669193765中的任何cas9核酸内切酶序列的变体或片段的氨基酸序列或者px330或px260(addgene,cambridge,ma)的cas9氨基酸序列。可以修饰cas9核苷酸序列来编码cas9的生物活性变体,并且这些变体可以具有或可以包含,例如,由于含有一个或多个突变(例如添加、缺失或取代突变或这样的突变的组合)而不同于野生型cas9的氨基酸序列。例如,cas9核酸酶可以在参与链特异性切割的保守finh和ruvc结构域中发生突变。例如,ruvc催化结构域中的天冬氨酸至丙氨酸(d10a)突变允许cas9切口酶突变体(cas9n)对dna切口而不是切割,从而产生单链断裂,并且随后通过hdr进行的优先修复可潜在减少由脱靶双链断裂而引起的无用插入缺失突变的频率。在一些实施方式中,载体包含一种或多种向导rna。如本文所用的术语“一种或多种向导rna”是指引导残基的插入或缺失的rna。在本发明的环境下,向导rna用于将cas9募集到特定的基因组基因座。在一些实施方式中,所述向导rna可以是与编码或非编码序列互补的序列。在一些实施方式中,给对象施用至少一种包含一种编码cas9核酸内切酶的多核苷酸的载体和至少一种包含所述向导rna的载体的组合。
在一些实施方式中,所述多核苷酸产物是干扰rna(rnai),特别是sirna。“小干扰”或“短干扰rna”或sirna是靶向目的基因(“靶基因”)的核苷酸的rna双链体。“rna双链体”是指由rna分子的两个区域之间的互补配对形成的结构。sirna被“靶向”到基因,因为该sirna的双链体部分的核苷酸序列与靶基因的核苷酸序列互补。在一些实施方式中,sirna的双链体的长度小于30个核苷酸。
在一些实施方式中,多核苷酸产物是短发夹rna(shrna)。术语“短发夹”或shrna是指含有环结构的核苷酸的rna,并且其被加工成sirna。因此,shrna也以依赖于靶基因的互补结合的序列特异性方式导致基因的敲除(know-down)。
在一些实施方式中,多核苷酸产物是反义寡核苷酸。如本文所用的术语“反义寡核苷酸”应理解为是指与pre-mrna分子、hnrna(不均一核rna)或mrna分子中的靶核苷酸序列基本互补的核苷酸序列。反义序列的互补性(或基本互补性)的程度优选使得包含所述反义序列的分子可以在生理条件下与rna分子中的靶核苷酸序列形成稳定的杂交体。
如本文所用的术语“aav”是指超过30种天然存在且可获得的腺相关病毒,以及人造aav。通常,本文所述的aav衣壳、itr和其他选择的aav组分可以很容易地从任何aav之中选择,所述aav包括但不限于:aav1,aav2,aav3,aav4,aav5,aav6,aav6.2,aav7,aav8,aav9,rh10,aavrh64r1,aavrh64r2,rh8,任何已知或提及的aav的变体,或尚未发现的aav,或其变体或混合物。参见,例如,wo2005/033321。aav的各种血清型的基因组和蛋白序列,以及天然末端重复(tr)、rep蛋白和包含vp1蛋白的衣壳亚基的序列是本领域已知的。这样的序列可以在文献中或在公共数据库例如genbank或蛋白数据库(proteindatabank,pdb)中找到。参见,例如genbank和pdb登录号nc_002077和3ng9(aav-1)、af043303和1lp3(aav-2)、nc_001729(aav-3)、u89790和2g8g(aav-4)、nc_006152和3ntt(aav-5)、3oah(aav6)、af513851(aav-7)、nc_006261和2qa0(aav-8)、ay530579和3ux1(aav-9(分离株hu.14));其中对于教示aav核酸和氨基酸序列的公开内容通过引用并入本文。还参见,例如srivistava等人(1983)j.virology45:555;chiorini等人(1998)j.virology71:6823;chiorini等人(1999)j.virology73:1309;bantel-schaal等人(1999)j.virology73:939;xiao等人(1999)j.virology73:3994;muramatsu等人(1996)virology221:208;shade等人(1986)j.virol.58:921;gao等人(2002)proc.nat.acad.sci.usa99:11854;moris等人(2004)virology33:375-383;国际专利公布wo00/28061、wo99/61601、wo98/11244;以及美国专利no.6,156,303和us7906111。
如本文所用的术语“重组aav9衍生载体”或“raav9衍生载体”是指9型腺相关病毒,其包含非aav9来源的目的多核苷酸序列(即异源序列,例如要递送给细胞的转基因)和/或其中天然dna或蛋白(cap和/或rep)已被修饰例如以改变其向性。换句话说,所述raav9衍生载体不是天然存在的。在本发明的环境下,所述raav9衍生载体包含在特定启动子控制下的上述目的多核苷酸序列(作为异源序列),以及修饰的aav9vp1衣壳蛋白,以便在视锥细胞光感受器中提供有效递送以及多核苷酸的高水平表达,优选在视网膜下注射后,同时最小化任何潜在的副作用,例如针对所述载体的中和抗体的发生和/或在邻近细胞中的脱靶表达。
更特别地,本发明的重组aav9衍生载体包含:
-vp1衣壳蛋白,其中相对于相应野生型aav9衣壳蛋白,在所述衣壳蛋白的gh环中插入了7至11个氨基酸长度的肽,其中所述肽包含seqidno:1至seqidno:8中的任一个;和
-在如seqidno:12所示的pr1.7启动子或所述启动子的功能变体控制下的目的多核苷酸。
如上所述,将长度为7-11个氨基酸并包含seqidno:1至seqidno:8中的任一个的肽(在本文中也称为插入肽)插入所述vp1衣壳蛋白的gh环中。这意味着所述插入肽可以具有7个氨基酸、8个氨基酸、9个氨基酸、10个氨基酸或11个氨基酸的长度。更特别地,所述插入肽可在seqidno:1至seqidno:8中的任一个的氨基末端和/或羧基末端具有间隔子。本发明的合适的间隔子包括但不限一个或多个亮氨酸、丙氨酸、甘氨酸和丝氨酸。例如,本发明的插入肽优选包含seqidno:9或由seqidno:9组成。更优选地,本发明的插入肽由seqidno:9组成。所述插入肽的作用是与野生型aav9相比,增加raav9-载体进入视锥细胞光感受器的感染性。
由于该插入肽的存在,所述raav9-载体的vp1衣壳蛋白被认为是相对于野生型(即天然的)aav9衣壳蛋白(例如seqidno:10)进行了修饰。任选地,本发明的vp1衣壳蛋白可以包含其他修饰(即突变),例如氨基酸缺失、氨基酸取代或其他氨基酸插入,只要所述衣壳蛋白保持其封装目的多核苷酸以及与目的靶细胞结合、内化和在所述细胞内通行的能力即可。允许引入这样的突变的方法是本领域技术人员已知的。例如,可以在编码基准蛋白的核苷酸序列中通过随机或定向诱变、通过使用简并引物的pcr,来引入突变。sambrook等人在“分子克隆:实验室手册(molecularcloning:alaboratorymanual)”,第4版,coldspringharborlaboratorypress,(2012,并从2014年起更新),和ausubel等人在“current25protocolsinmolecularbiology”,johnwiley&sons(2012)中,特别描述了这些技术。
所述肽插入发生在所述衣壳蛋白的gh环(也称为环iv)内,更特别地,在gh环的溶剂可及区域中(vanvliet等人(2006)mol.ther.14:809;padron等人(2005)j.virol.79:5047;以及shen等人(2007)mol.ther.15:1955)。在一个优选实施方式中,所述肽的插入位点是位于aav9衣壳蛋白的氨基酸570-614之间的两个相邻氨基酸之间的单个插入位点。例如,所述插入位点在aav9衣壳蛋白的氨基酸571至612内。更优选地,所述肽的插入位点位于aav9衣壳蛋白的氨基酸588和589之间。
因此,在一个优选实施方式中,相对于如seqidno:10所示的野生型aav9衣壳蛋白,将如上所述的肽插入到gh环中氨基酸588和589之间。
在一个更优选的实施方式中,将如上所述的肽插入到如seqidno:10所示的野生型aav9衣壳蛋白的gh环中氨基酸588和589之间。
更加优选地,将包含seqidno:1的肽,优选seqidno:9的肽,插入到如seqidno:10所示的野生型aav9衣壳蛋白的gh环中氨基酸588和589之间。换句话说,本发明的raav9载体最优选包含如seqidno:11所示的vp1衣壳蛋白和所述目的多核苷酸序列(即,与aav异源的多核苷酸)。因此,在本发明的重组aav9衍生载体中,如seqidno:10所示的aav9的天然vp1衣壳蛋白可以被如seqidno:11所示的vp1衣壳蛋白取代。
本发明的重组aav9衍生载体通常包含5'和3'腺相关病毒反向末端重复(itr)、与启动子pr1.7操作性连接的目的多核苷酸(即异源多核苷酸)。为了本发明的目的,与启动子pr1.7操作性连接的目的多核苷酸优选侧接两个aavitr。使用本领域已知的方法产生本发明的载体。简而言之,所述方法通常包括(a)将所述aav载体引入宿主细胞,(b)将aav辅助构建体引入宿主细胞,其中所述辅助构建体包含所述aav载体缺失的病毒功能,以及(c)将辅助病毒引入宿主细胞。用于aav病毒体复制和包装的所有功能均需要存在,以实现aav载体在aav病毒体中的复制和包装。所述引入宿主细胞可以使用标准病毒学技术同时或顺序进行。最后,培养宿主细胞以产生aav病毒体,并使用例如碘克沙醇或cscl梯度等标准技术或其他纯化方法进行纯化。纯化的aav病毒体然后即可用于所述方法。
如本文所用的术语“启动子”具有其在本领域的一般含义,并且是指控制一个或多个基因的转录的核酸片段,位于相对于基因转录起始位点的转录方向的上游,并且在结构上通过dna依赖性rna聚合酶的结合位点、转录起始位点和任何其他dna序列的存在进行鉴定,所述其他dna序列包括但不限于转录因子结合位点、阻遏子和激活蛋白结合位点、以及本领域技术人员已知的直接或间接作用以调节从启动子转录的量的任何其他核苷酸序列。如本文所用的术语“pr1.7启动子”是指在humgenether.2016jan;27(1):72-82中描述并以如seqidno:12所示的核酸序列为特征的1.7-kbl-视蛋白启动子。启动子和目的多核苷酸操作性连接。如本文所用的术语“可操作地连接”是指两个或更多个核酸或氨基酸序列元件以使它们相互处于功能关系的方式物理连接。例如,如果启动子能够启动或以其他方式控制/调节编码序列的转录和/或表达,则该启动子与该编码序列可操作地连接,在这种情况下,该编码序列应被理解为“在该启动子的控制之下”。通常,当两个核酸序列可操作地连接时,它们将处于相同的取向,并且通常也在相同的阅读框中。它们通常也将基本上是邻接的,尽管这可能不需要。
本发明还包括本文所述的raav9衍生载体,其中所述目的多核苷酸在pr7.1启动子的功能变体的控制下。pr7.1启动子的“功能变体”通常相对于天然的pr7.1启动子(seqidno:12)具有一个或多个核苷酸突变(例如核苷酸缺失、添加和/或取代),所述突变不会显著改变目的多核苷酸的转录。在本发明的环境下,所述功能变体保留了驱动目的多核苷酸在视锥细胞光感受器中强表达的能力。这样的能力可以如ye等人(2016)(18)和khabou等人(2018)(17)所述进行测试。
在一个优选实施方式中,所述目的多核苷酸在seqidno:12所示的pr1.7启动子的控制下,或者在所述启动子的具有与其至少70%、优选至少75%、80%、85%、90%、95%或99%序列同一性的功能变体的控制下。
如技术人员公知的,两个核苷酸(或氨基酸)序列之间的“序列同一性%”是在为了最佳比较的比对时所述序列共有的同一的位置数量的函数。当比较序列中的一个位置被相同的核苷酸(或氨基酸)占有时,该序列在该位置被认为是同一的。实际上,同一性仅指完全匹配,并不考虑核苷酸(或氨基酸)彼此的相似程度。序列同一性的百分比可以通过将同一的位置数量乘以100并除以比对区域包括缺口(仅内部缺口,而不是序列末端的缺口)在内的长度(重叠位置)来计算。在这种比较中,序列可以长度相同,或可以长度不同。如果使用相同或相似长度的序列进行比对,则最佳序列比对在此可以优选通过总体同源性比对算法进行,例如通过needleman和wunsch描述的算法(journalofmolecularbiology;1970,48(3):443–53)、通过该算法的计算机实现(例如,使用
“治疗有效量”是指所述载体以合理的益处/风险比治疗视网膜疾病的足够量。应该理解,所述载体的每日总用量将由主治医师在合理的医学判断范围内决定。任何特定患者的具体治疗有效剂量水平将取决于多种因素,包括患者的年龄、体重、一般健康状况、性别和饮食;所使用的特定化合物的施用时间、施用途径和排泄速率;治疗持续时间;与所使用的特定多肽联合使用或同时使用的药物;以及医学领域公知的类似因素。例如,以低于达到期望的治疗效果所需的剂量水平开始化合物的剂量,并逐渐增加剂量直至达到期望的效果,是本领域技术内公知的。因此,载体的剂量可以取决于疾病状况、对象(例如,根据对象的体重和/或年龄、代谢、视网膜状态等)、治疗计划等进行调适。在本发明的环境内,优选的有效剂量是允许视锥细胞光感受器最佳转导的剂量。通常,在小鼠中每剂施用108至1010个病毒基因组(vg)。通常,要在人类中施用的aav载体的剂量范围可为109至1012vg,优选每只眼睛。
因此,本发明的载体可以配制成药物组合物。除了所述载体之外,这些组合物还可以包含药学上可接受的赋形剂、载剂(carrier)、缓冲剂、稳定剂或本领域技术人员公知的其他材料。这样的材料应该是无毒的,并且不应干扰活性成分(即本发明的载体)的功效。载剂或其他材料的精确性质可以由技术人员根据施用途径、即在此是视网膜下注射来确定。所述药物组合物通常为液体形式。液体药物组合物一般包括液体载剂,例如水、石油、动物或植物油、矿物油或合成油。可以包括生理盐水溶液、氯化镁、葡萄糖或其他糖类溶液或二醇例如乙二醇、丙二醇或聚乙二醇。为了注射,所述活性成分将以水溶液的形式,其无热原并具有合适的ph、等渗性和稳定性。本领域相关技术人员能够很好地使用例如等渗介质如氯化钠注射液、林格注射液、乳酸盐林格注射液来制备合适的溶液。根据需要,可以包括防腐剂、稳定剂、缓冲剂、抗氧化剂和/或其他添加剂例如洗涤剂以避免与注射材料结合(即pluronic)。为了延迟释放,可以将所述载体包含在被配制用于缓慢释放的药物组合物中,例如根据本领域已知的方法在由生物相容性聚合物形成的微胶囊中或脂质体载剂系统(carriersystems)中。通常,本发明的药物组合物以预充式注射器供应。“即用型注射器”或“预充式注射器”是指以填充状态供应的注射器,即待施用的药物组合物已存在于注射器中并准备好施用。与分开提供的注射器和小瓶相比,预充式注射器具有许多益处,例如便利性、可购性、准确性、无菌性和安全性得到改善。使用预充式注射器导致剂量精度更高、降低从小瓶吸取药物时可发生的针刺伤害的可能性、预先测量的剂量降低了因需要重构和/或将药物吸入注射器而导致的剂量给药误差、以及减少注射器的过量填充有助于通过最小化药物浪费来降低成本。在一些实施方式中,本发明的液体药物组合物的ph在5.0至7.0、5.1至6.9、5.2至6.8、5.3至6.7或5.4至6.6的范围内。
尽管有权利要求书,本发明还通过以下条款来限定。
条款1.一种在对象的视锥细胞光感受器中表达目的多核苷酸的方法,所述方法包括视网膜下递送治疗有效量的重组aav9衍生载体,所述载体包含如seqidno:11所示的vp1衣壳蛋白以及在如seqidno:12所示的pr1.7启动子控制下的目的多核苷酸。
条款2.条款1的方法,其中所述对象患有或可能患有影响视锥细胞光感受器的视网膜疾病。
条款3.条款1的方法,其中所述对象患有选自下列的视网膜疾病:年龄相关性黄斑变性,bassen-kornzweig综合征,无脉络膜症,回旋状萎缩,refsum综合征,usher综合征,色盲,蓝色视锥细胞单色视,全色盲,不完全性全色盲,寡视锥细胞三色视觉,色素性视网膜炎(rp),黄斑变性,stargardt病,bardet-biedl综合征,bornholm眼病,best病,和leber先天性黑蒙症。
条款4.条款1的方法,其中所述目的多核苷酸编码色素性视网膜炎gtp酶调节因子(rpgrorf15)、cngb3(视锥细胞环核苷酸门控阳离子通道的β亚基)、cnga3(视锥细胞环核苷酸门控阳离子通道的α亚基)或gnat2。
条款5.条款1的方法,其中所述目的多核苷酸编码神经营养因子。
条款6.条款1的方法,其中所述目的多核苷酸编码rdcvf、rdcvf2、rdcvfl或rdcvfl2。
条款7.条款1的方法,其中所述目的多核苷酸编码视蛋白,例如视紫红质如盐细菌视紫红质或十字视紫红质、光视蛋白、l/m波长(红/绿)视锥细胞视蛋白、或短波长(s)视锥细胞视蛋白(蓝)。
条款8.条款7的方法,其中所述目的多核苷酸编码由如seqidno:13、seqidno:14或seqidno:15所示的氨基酸序列组成的视蛋白。
条款9.条款1的方法,其中所述目的多核苷酸编码提供基因功能的位点特异性敲除的位点特异性核酸内切酶,所述核酸内切酶选自锌指核酸酶(zfn)、转录激活因子样效应子核酸酶(talen)和crispr相关核酸内切酶。
条款10.条款1的方法,其中所述目的多核苷酸编码cas9核酸酶。
条款11.条款1的方法,其中所述目的多核苷酸编码干扰rna(rnai),特别是sirna或shrna。
条款12.条款1的方法,其中所述目的多核苷酸编码反义寡核苷酸。
条款13.条款1的方法,其中所述视网膜下递送在中央凹的一定距离处进行,不会使所述区域脱离。
条款14.一种重组aav9衍生载体,其包含如seqidno:11所示的vp1衣壳蛋白以及在如seqidno:12所示的pr1.7启动子控制下的目的多核苷酸。
条款15.条款14的重组aav9衍生载体,其用于治疗影响视锥细胞光感受器的视网膜疾病的方法。
通过以下附图和实施例将进一步说明本发明。然而,这些实施例和附图不应以任何方式解释为限制本发明的范围。
附图说明
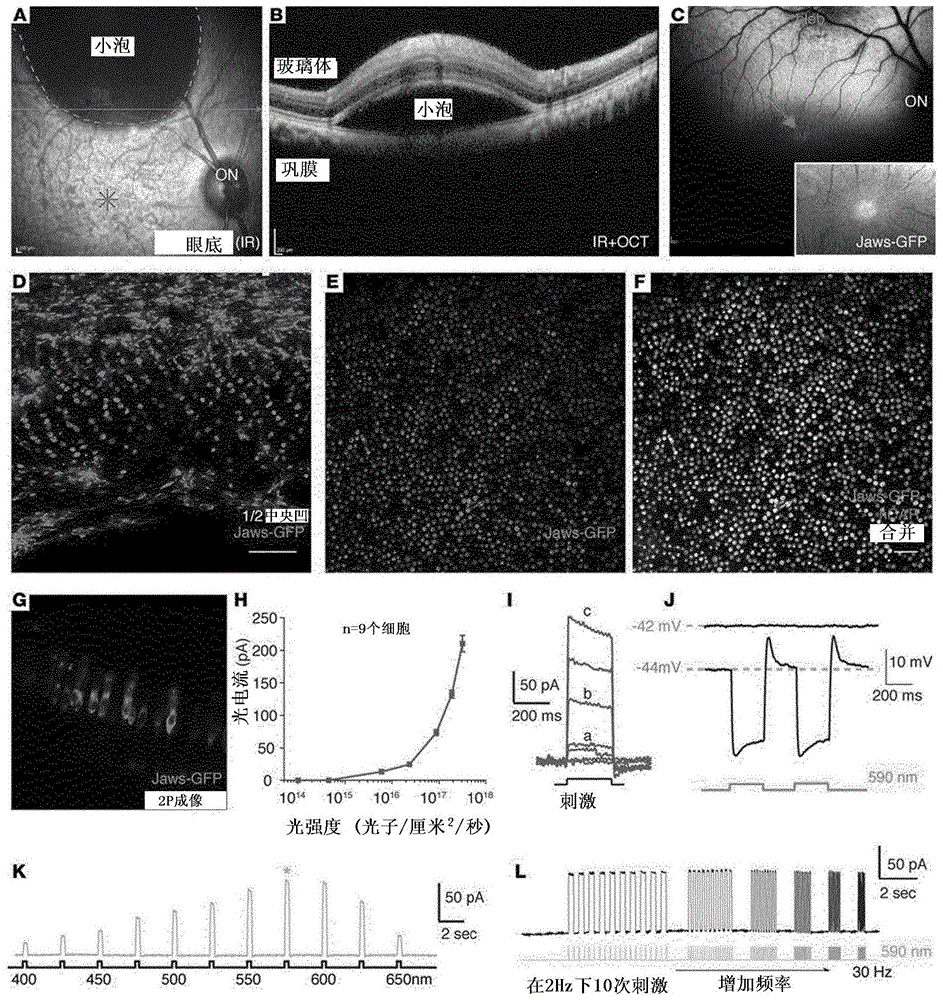
图1.aav9-7m8通过在远端小泡中递送来转导中央凹,并与pr1.7-jaws一起提供稳健的光遗传学光响应。(a)在周边视网膜中视网膜下递送aav9-7m8后即刻的眼底红外图像和(b)光学相干断层扫描(oct)图像。(c)注射后1个月的眼底荧光图像显示,在视网膜下的小泡内和远离注射部位、包括中央凹的强jaws-gfp表达。插图放大倍数:×1.5。(d–f)中央凹平铺片(flatmount)显示了使用视网膜下aav9-7m8-pr1.7-jaws-gfp的高效且特异性的中央凹转导。比例尺:50μm。(g–l)通过jaws的光遗传学刺激触发的光响应的特征。(g)利用2光子成像,活组织中表达jaws的视锥细胞的侧视图。(h和i)jaws-gfp+猕猴视锥细胞的全细胞膜片钳记录。jaws诱导的光电流随光强度的变化。施加从1×1014至3×1017光子厘米-2秒-1的刺激(n=9个来自2只动物的2个视网膜的细胞)。(j)在电流钳配置中以零电流模式记录的jaws-gfp+视锥细胞(静息膜电位以灰色指示),显示了光引发的超级化继以短去极化。(k)在视网膜下注射的猕猴眼睛中jaws诱导的光电流随刺激波长的变化。从400-650nm施加刺激,间隔25nm步长,强度等于8×1016光子厘米-2秒-1。在575nm(星号)处获得了最大响应。(l)时间特性的表征。在表达jaws的猕猴视锥细胞中,在从2–30hz的渐增的刺激频率下以8×1016光子厘米-2秒-1对jaws诱导的膜光电流的调制。aav,腺相关病毒;pr1.7:基于人类红视蛋白基因增强子和启动子序列,长度1.7千碱基的启动子;ir:红外。
图2.用于表征剂量响应的猕猴眼底图像。视网膜下注射aav9-7m8-pr1.7-jaws-gfp的1x1010个粒子(n=1只眼睛,上部的小泡)(a)和5x109个粒子(n=2只眼睛,下部的小泡)(b)两周后,jaws-gfp的表达。
图3.利用体内眼底和光学相干断层扫描(oct)成像对远端下部视网膜下施用的追踪。在周边注射aav9-7m8-pr1.7-jaws-gfp,5x109个病毒粒子(n=2只眼睛)之前和之后获取图像。眼底红外图像以黄斑为中心,oct图像在注射之前和之后不久在中央凹水平处或小泡水平处拍摄。注射后一小时,在保持动物坐下的同时获取追踪图像。注射24小时后获取另一个图像。小泡:视网膜下注射的流体;hr:小时;星号:中央凹;粗体箭头:强调视网膜的oct图像,在每个图像的右侧部分显示;虚线:小泡的界限。
图4.来自用高剂量的avv9-7m8-pr1.7-jaws-gfp注入视网膜下空间的动物的代表性组织学发现。比例尺100μm。rpe:视网膜色素上皮;onl:外核层;inl:内核层;gcl:神经节细胞层。
图5.中央凹附近的免疫组织化学提示玻璃体内注射后没有适应性细胞免疫响应。左侧图块显示了视网膜下注射后用aav9-7m8-pr1.7-jaws-gfp(1010vg)处理的2只眼睛之一的代表性图像。右侧图块显示了四只未注射的眼睛之一的代表性图像。
实施例
材料&方法:
aav产生
如前所述使用共转染方法产生aav载体,并通过碘克沙醇梯度超速离心进行纯化(49)。使用sybrgreen(thermofischerscientific),通过定量pcr(50)滴定aav载体原种。
动物和眼内注射
本研究使用野生型c57bl6/j小鼠(janvierlabs)或rd10小鼠(在视力研究所(visioninstitute)的动物设施中繁殖和饲养)和食蟹猕猴(noveprim,毛里求斯)。
为了眼睛注射(n=6只眼睛/条件),将6周龄雌性小鼠通过吸入异氟烷麻醉。使瞳孔散大并将33号针头插入眼中,玻璃体内递送2μl的aav载体溶液或视网下膜递送1μl。
关于猕猴眼睛注射,首先基于没有针对aav的中和抗体滴度来选择猕猴。在手术前,通过肌内注射10mg/kg氯胺酮和0.5mh/kg甲苯噻嗪使灵长类动物麻醉。用静脉注射丙泊酚1ml/kg/h(propovetmultidose10mg/ml,zoetis)维持麻醉。然后,将它们的瞳孔散大,并使用开睑器保持它们的眼睑张开。使用配备32毫米的27号针头的1毫升注射器进行玻璃体内注射。将针头插入角膜缘后约2mm的巩膜中,以递送100μl病毒载体溶液。最后,慢慢取出针头。动物没有接受局部皮质类固醇注射。
对于视网膜下aav注射,在所述角膜缘后约2mm设置两个25号玻璃体切除口,一个用于内照明探头,另一个用于视网膜下套管。使用配备25号视网膜下套管和41号尖头的1毫升hamilton注射器进行注射。将所述内照明探头和套管引入眼睛。视网膜下注射所述病毒载体溶液(50μl)以在中央凹下方或上方生成小泡。然后撤出器具。眼睛接受由球侧注射(laterobulbarinjection)12mg的kenacort(bristol-myerssquibb)组成的皮质类固醇处理(47),但nhp5的右眼除外。视网膜下或玻璃体内施用载体后,在注射后将眼科用类固醇和抗生素软膏(fradexam,tvm)施加于角膜。
猕猴眼睛体内成像
瞳孔散大后,使用spectralishra+oct系统(heidelbergengineering,德国)获取oct图像,并使用“眼底自发荧光模式(fundusautofluoresencemode)”获取gfp的荧光图像,该模式由488nm的激发波长和500nm的吸收滤光片组成。
猕猴视网膜的双光子成像和离体电生理记录
使用配备40x水浸物镜(lumplfln40x/w/0.80,olympus)和脉冲飞秒激光器(insighttmdeepseetm-newportcorporation)的双光子显微镜,对完整安装的视网膜(光感受器细胞侧朝上)或视网膜切片(纵切片)的gfp阳性视网膜细胞进行成像。将aav处理的猕猴视网膜分离,然后在充氧(95%o2,5%co2)的ames培养基(sigma-aldrich)中成像。为了活体双光子成像,将视网膜放置在显微镜的记录槽(recordingchamber)中,并使用在930nm波长的激发激光获取z-栈。图像使用imagej(nih)离线处理。为了全细胞膜片钳记录,使用了axonmulticlamp700b放大器。电极由硼硅玻璃(bf100-50-10,sutterinstruments)制成,并拉至6-9mω。将移液管填充115mm葡萄糖酸钾、10mmkcl、1mmmgcl2、0.5mmcacl2、1.5mmegta、10mmhepes和4mmatp-na2(ph7.2)。将细胞钳制在电压钳配置中-40mv的电位下,或在电流钳(电流为零)配置中记录。在记录之前,将视网膜在记录槽中暗适应至少半小时。
人ipsc培养物
我们根据以前发布的方案(37),从人ipsc生成了视网膜类器官。克隆hipsc-2在如已经描述的“促神经形成培养基(proneuralmedium)”中在成纤维细胞饲养细胞(frbroblastfeeders)上从出生后人包皮细胞(atcccrl2429)扩增和分化(37)。从高度汇合的贴壁ips细胞培养物开始并且没有成纤维细胞生长因子2(fgf2),可以在2周后鉴定出自形成的视网膜类器官。此时,将所述类器官被机械分离并在3d条件下培养直至43天。机械分离所述类器官后,以3种条件向培养基补充7天的fgf2以促进它们的生长。在分化的第28天,用携带在pr1.7启动子控制下的gfp基因的aav2-7m8载体,以5x1010vg/类器官的剂量感染所述视网膜类器官。从第28天起向培养基添加一周的10μmdapt(selleck),以促进现有细胞群的细胞周期停滞。在感染后5天首次观察到荧光强度,并持续增加直至第43天。
人类死后视网膜外植体
使用以前描述的方案(38)制备人类视网膜外植体。简而言之,在co2非依赖性培养基(thermofisherscientific)中解剖眼睛。去除前部,分离视网膜并切成小块。将这些外植体光感受器侧朝上放置在transwell细胞培养插入物(corning)上,并向在每个外植体下面的每个孔中添加2ml补充有b27(thermofischerscientific)的neurobasal培养基(thermofischerscientific)。第二天,用0.5μl的一滴的含有1010个病毒粒子的aav-pr1.7-gfp感染每个外植体。将载体感染的外植体温育10-15天以使gfp表达,所述表达使用落射荧光显微镜检查。
组织学,免疫组织化学和显微镜检查
摘出小鼠眼睛,并立即在10%福尔马林–4%甲醛中固定2小时以备冷冻切片。在解剖后,将猕猴视网膜在4%甲醛中固定3小时。在培养期结束时,将视网膜类器官和人类视网膜外植体在pbs中清洗,并在4%多聚甲醛中固定10分钟。为了冷冻切片,将小鼠和猕猴视网膜、视网膜类器官和人类视网膜外植体在4℃下浸泡在pbs-30%蔗糖中过夜。将小鼠眼杯体、人视网膜外植体、猕猴视网膜包埋在oct(最佳切割温度)培养基中,并在液氮中冷冻,而将视网膜类器官包埋在含7.5%明胶和10%蔗糖的pbs中,并在干冰冷却的异戊烷中冷冻。用microm低温恒温器切割10μm厚的纵切片。在封闭缓冲液中温育后,将切片与一级抗体在4℃下温育过夜,所述一级抗体是:人视锥细胞抑制蛋白(hcar)抗体(来自美国洛杉矶南加州大学(universityofsoutherncalifornia)的cherylcraft的礼物);m/l视蛋白抗体(milliporeab5405)和小鼠视锥细胞抑制蛋白抗体(millipore,ab15282)。多次洗涤所述切片后,添加二级抗体(alexafluor488、594或647,thermofisher)和dapi,随后洗涤数次。将视网膜平铺片或冷冻切片封固在vectashield封固剂(vector实验室)中进行荧光显微镜检查,并使用olympusupright共聚焦显微镜对视网膜切片进行可视化,然后用fiji软件进行分析。使用imaris软件(bitplane)创建中央凹的三维投影。
潜在调控元件的计算机鉴定以及转录组分析
在红视蛋白基因启动子序列–pr2.1和pr1.7序列–以及视锥细胞抑制蛋白3基因组区域上进行tf结合位点分析。transfac数据库8.3(http://alggen.lsi.upc.es/)用于tf结合位点预测。使用感觉系统知识库(knowledgebaseforsensorysystem)(kbass,http://kbass.institut-vision.org/kbass/transcriptomics/index.php)对预测名单中的每个tf进行分析,以使用转录组实验rng209来选择在人类视网膜中表达的tf(51)。使用过滤器保留从实验rng209制备的样品中在通过如前所述的鲁棒多阵列平均(rma)归一化后,信号强度值优于40单位的tf(52)。在该实验中,用作对照的人类视网膜标本是在没有眼科疾病或糖尿病既往病史的患者死亡后12小时内收集的死后标本。从代表17位患者的19只眼睛中收集了19个样品。性别比为12名男性/7名女性,平均年龄为61岁(范围为25-78岁)。
统计学
使用graphpadprism中的单因素anova检验分析数据(多重比较,tukey校正)。图表上的误差棒显示平均值的标准误差(sem)。p值表示如下*p<0,033,ns:非显著性。
研究许可
对于动物,根据《国立卫生研究院实验动物护理和使用指南(nationalinstitutesofhealthguideforcareanduseoflaboratoryanimals)》进行实验。该方案经当地动物伦理委员会(localanimalethicscommittees)批准,并根据欧洲议会的2010/63/eu指令实施。捐赠者的人类死后眼球从外科学院(schoolofsurgery)(ecoledechirugie,assitancepublique
结果:
在小鼠模型中选择强而特异性的视锥细胞特异性启动子
为了找到适合强而特异性的远离注射部位视锥细胞靶向的载体-启动子组合,我们在小鼠视网膜中玻璃体内和视网膜下递送后比较了几种aav。为了能够实现有效地视锥细胞光感受器靶向,我们使用了一种被称为aav2-7m8的工程化aav变体,该变体已被证明通过这两种施用路径有效靶向光感受器(16,17)。从未尝试过使用玻璃体施用的aav来特异性靶向视锥细胞。为了找到用于适于临床的视锥细胞中限制性基因表达的合适的启动子序列,我们集中于先前已在非人灵长类动物(nhp)(18)或人类组织中验证的启动子(4)。我们生成了在mcar(小鼠视锥细胞抑制蛋白)、pr2.1和pr1.7启动子(基于人类红视蛋白基因增强子和启动子序列的合成启动子)控制下编码gfp的aav2-7m8载体,并以相等的滴度将它们注射到六周龄野生型小鼠的眼睛中。视网膜下注射后三周,用视锥细胞抑制蛋白对视网膜横截面进行染色,并检查gfp表达(数据未显示)。我们在有mcar启动子的视杆和视锥细胞光感受器两者中均发现了高gfp表达,而pr2.1和pr1.7导致主要在视锥细胞中强表达。使用相同的载体,我们在玻璃体内递送后获得了截然不同的表达模式(数据未显示)。mcar启动子在一些视锥细胞中导致gfp表达,但向视杆细胞以及内核层(inl)和神经节细胞层(gcl)的细胞渗漏(数据未显示)。pr2.1和pr1.7启动子两者都比mcar启动子导致更多的视锥细胞标记(数据未显示)。pr2.1比pr1.7转导更多的视锥细胞,但在inl和gcl中也产生非特异性的gfp表达。只有pr1.7启动子在视锥细胞中显示gfp表达而在视杆细胞中表达最少,并且不向内视网膜渗漏(数据未显示)。最后,由于视网膜疾病状态可影响aav介导的基因递送和转基因表达模式(20,21),因此我们在视网膜变性小鼠模型中验证了aav2-7m8-pr1.7载体-启动子组合。我们在色素性视网膜炎的rd10小鼠模型中玻璃体内注射aav2-7m8-pr1.7-gfp。注射后两个月,gfp表达限于视锥细胞(数据未显示),支持了该载体对于通过玻璃体内和视网膜下这两种注射进行视锥细胞定向基因疗法的适用性。
mcar、pr1.7和pr2.1启动子序列的生物信息学分析
在继续进行其他物种的进一步研究之前,我们旨在更好地了解由所述三种启动子获得的不同表达模式背后的原因。为此,我们使用生物信息学分析了每个启动子序列内的转录因子(tf)结合位点(数据未显示)。本分析旨在回答以下问题:(i)为什么在视锥细胞中pr1.7比pr2.1更有效?(ii)为什么pr2.1和mcar启动子在玻璃体内施用后会导致脱靶表达?我们假设在pr1.7和pr2.1之间观察到的差异表达模式是由于在位于pr2.1启动子的5'区域的337bp序列中发现的其它tf结合位点,而在pr1.7启动子中则没有(数据未显示)。有趣的是,我们在该337bp序列内发现了鸡卵清蛋白上游启动子转录因子i(coup-tfi)结合位点(数据未显示)。coup-tfi已被证明抑制小鼠视网膜中绿视蛋白基因(opn1mw)表达(22),因此可能可以解释当视网膜下递送aav时用pr2.1启动子在猕猴视锥细胞中表达较低的原因。在该相同的特定337bp区域内,我们还发现了通用的遍在激活因子tf的多个结合位点(数据未显示),例如ccaat/增强子结合蛋白β(cebpb)和通用转录因子ii-i(gtf2i)。这些其它tf结合位点增强结合和基础转录机制装配并且不在视锥细胞中特异性表达,可能是造成与pr1.7相比,用pr2.1观察到的一些脱靶表达的原因(数据未显示)。我们还分析了基因组mcar启动子序列(也称为小鼠arr3)中的tf结合位点,以解释使用在aav构建体中所用的这种启动子的短版缺乏特异性。所述短序列由基因组近端car启动子的521bp部分组成(数据未显示),该部分呈现了tata框、tata样框、以及crx(锥杆同源框蛋白)和sp(特异性蛋白)tf(23)的结合位点(数据未显示)。然而,位于所述521bp区域的直接上游的调制car启动子活性的‘reg’序列(23)被排除在所述短mcar序列之外(数据未显示)。根据从string数据库获得的tf结合mcar启动子的相互作用组(24),crx和sptf彼此相互作用,并与rara(视黄酸受体α)、rxra(类视色素x受体α)和thrb(甲状腺激素受体β)tf相互作用(数据未显示)。这三种核受体(nr)通过形成细胞特异性转录共激活因子复合物(26,27)(数据未显示),通过med1(25)(中介体复合物亚基1)参与基因表达的细胞类型特异性调节。crx和sp结合位点位于所述521bp区域,而rxra、rara和thrb结合位点位于所述reg区域(数据未显示)。此外,所述reg区域含有五个theβ2结合位点,theβ2是在视锥细胞中表达的重要核受体(28)(数据未显示)。由于所有这些原因,所述reg区域的去除可能是造成用所述短mcar启动子观察到的脱靶表达的原因。
通过玻璃体内施用aav将基因安全递送到猕猴中央凹视锥细胞
其他人和我们已经表明了使用有遍在启动子的aav变体转导猕猴视锥细胞(16,29–31),但是通过玻璃体施用aav实现视锥细胞转导仅在高剂量下是可能的,而高剂量导致炎症(16,29)。我们推论,如果我们以与安全性相容的较低玻璃体内注射aav剂量来使用强视锥细胞特异性启动子,就可以实现中央凹视锥细胞靶向(29,32)。为了检验这样的“节省剂量(dosesparing)”是否可能,我们以1011病毒基因组(vg)的剂量对两只猕猴眼睛注射aav2-7m8-pr1.7-gfp并对2只其他猕猴眼睛注射aav2-7m8-cmv-gfp(表1)。使用体内眼底成像,我们观察到cmv早在注射后两周就有gfp表达,并增加直到注射后2个月(数据未显示)。gfp荧光主要在周边和中央凹旁区域。用pr1.7的gfp表达在施用后6至8周变得可检测,并且限于中央凹(数据未显示)。通过光学相干断层扫描(oct)评估,对中央凹没有可检测的损伤(数据未显示)。注射后3个月处死动物。然后我们制备了黄斑的平铺片(数据未显示)和中央凹水平处的视网膜冷冻切片(数据未显示),并使用共聚焦显微镜检查对gfp荧光进行成像,每只眼睛的采集设置相等。这些图像印证了所述体内发现,并显示了从玻璃体以1011个粒子的剂量使用aav2-7m8-pr1.7的特异而稳健的视锥细胞转导。发现约58%的hcar+细胞在中央小凹中表达可检测的gfp水平。使用相似的剂量,不可能用cmv转导视锥细胞(没有可检测的转基因表达)。
表1:在非人灵长类动物中注射的总结
nhp,非人灵长动物;kg,千克;m,雄性;sup,上部的小泡;inf,下部的小泡;le:左眼;re,右眼;aav,腺相关病毒;cmv,巨细胞病毒启动子;pr1.7,启动子1.7千碱基,基于人类红视蛋白增强子和启动子序列;vg,病毒基因组
使用光遗传学将治疗性基因递送至中央凹视锥细胞以恢复视力
接下来,我们旨在评价使用该启动子进行治疗性基因递送的可能性。目前尚不存在视网膜变性的盲猕猴或灵长类动物模型来测试基因置换(即用于治疗全色盲的cngb3)后的功能结果。但是,使用光遗传学策略评价野生型猕猴的视力恢复是可能的,因为我们可以对光遗传学介导的光响应与内源性视锥细胞视蛋白介导的响应之间进行区分(4)。我们通过在中央凹视锥细胞中表达jaws(jaws是一种超极化的微生物视蛋白(15)),来评价光遗传学视力恢复的潜力。我们向一只猕猴在玻璃体中注射了1011vg的aav2-7m8-pr1.7-jaws-gfp,以评价如以前在小鼠中所描述的,其在中期色素性视网膜炎中再活化休眠视锥细胞的治疗潜力(4,15)。我们发现,与单独的gfp表达(数据未显示)相似,在被注射的眼睛中高水平jaws-gfp表达限于中央凹视锥细胞(数据未显示)。然后在注射后两个月处死动物,并对视网膜的一半进行组织学处理。视网膜平铺片显示了中央小凹中视锥细胞的典型解剖结构,中央凹的该区域含有密集堆积的视锥细胞,负责我们高度敏锐的视力。利用对视锥细胞抑制蛋白的免疫染色来定量转导的视锥细胞(数据未显示)。发现在该视网膜中约50%的视锥细胞抑制蛋白阳性细胞(hcar+)表达可检测水平的jaws-gfp。视网膜的另一半作为外植体保存(33),用于表征因超极化泵jaws而产生的光遗传学光响应(数据未显示)。对表达jaws的转导的视锥细胞并在没有gfp表达的对照视锥细胞中进行电生理记录(数据未显示)。在gfp阳性jaws-视锥细胞中的全细胞膜片钳记录表现出对橙色闪光的稳健光响应(n=4)(数据未显示)。记录的细胞的作用光谱显示,如先前对jaws所显示的,使用575和600nm之间的橙色光获得最高的光响应(数据未显示),(14)。在电流钳配置中记录的jaws表达型视锥细胞表现出光引发的超极化继之以短的去极化(n=4个细胞),而对照视锥细胞对相同的光刺激没有作出响应(n=3个细胞)(数据未显示)。
最后,我们向另一只猕猴玻璃体内注射了1010个aav2-7m8-pr1.7-jaws-gfp粒子,以评价在更加低的剂量下中央凹转导的可行性。即使在这种更低剂量下,我们仍获得了可检测的中央凹jaws表达,尽管表达水平低于用1011个粒子的(数据未显示)。总之,用aav2-7m8-pr1.7-gfp(n=2)或jaws-gfp(n=2)注射的所有4只猕猴眼睛均显示出可与光遗传学再活化视锥细胞相容的玻璃体内方法的再现性和强度。
通过远端视网膜下施用aav9-7m8-jaws增强中央凹视锥细胞中的光遗传学响应
通过玻璃体腔注射有强视锥细胞启动子的aav2-7m8来转导中央凹视锥细胞,可能是治疗休眠视锥细胞主要存在于中央小凹中的色素性视网膜炎患者的脆弱视网膜中的视锥细胞的理想方法。然而,对于全色盲患者,以及色素性视网膜炎患者中的抗aav2中和抗体滴度强的亚群(32),视网膜下方法可能是有利的。以前的研究表明,视网膜下注射aav9导致在低剂量下向中央和周边两者的视锥细胞中的有效转基因表达,这可能是由于视锥细胞光感受器上存在大量的半乳糖基化聚糖,这是aav9的主要受体(30,34)。基于此,我们推论增强的aav9变体可能提供了从远端小泡的有效的中央凹视锥细胞转导。为了促进通过远端视网膜下注射部位的中央凹视锥细胞基因递送,我们使用了aav9-7m8变体,该变体与野生型aav9相比,感染力增加了30倍。我们向一只动物视网膜下注射了5x1010个这种编码jaws-gfp的载体粒子到周边的视网膜中(图1,a-b),没有使中央凹脱离。早在注射后两周,我们就在小泡(以虚线划界)并且也在中央小凹(图1c)中观察到了强jaws-gfp荧光。与玻璃体内处理的视网膜相比,中央小凹中的荧光强度更高。我们用注射了1010vg较低剂量的相同载体的第二只眼睛观察到了同样的数据(图2a)。为了进一步确认一旦动物处于直立位置,上部外周小泡不会向中央凹下降并查看是否可能进一步降低剂量,我们给另外2只眼睛注射了510vg的剂量,这次低于中央凹(表1)。使用oct,我们观察到中央凹在手术后没有脱离(图3)。在这些视网膜中获得了相同的表达模式,扩展到中央凹视锥细胞(图2b)。这些结果共同显示了这种方法的再现性及其与低病毒剂量的相容性。
然后制备视网膜平铺片。对中央凹进行组织学处理,并在注射部位和中央凹内部之间的区域中的大量视锥细胞中(图1d)显示出强jaws-gfp表达(图1,d-f)。中央凹中的gfp和视锥细胞抑制蛋白阳性(car+)细胞的细胞计数显示,使用这种视网膜下方法标记了约95%的视锥细胞(图1,e-f),与此相比,玻璃体内注射得到的约为50%(数据未显示)。视网膜下递送后jaws视锥细胞中的光电流幅度(图1,g-h)比玻璃体内递送后jaws视锥细胞中的光电流幅度(数据未显示)高5倍,光敏度曲线的形状相似。这可能是由于与玻璃体内转导的视锥细胞相比,视网膜下转导的视锥细胞中的jaws表达更高。使用不同频率的闪烁刺激进行的时间分析显示,在8x1016个光子厘米-2秒-1下从2hz直至30hz的光电流响应非常快速且稳健(图1l)。在这两种情况下,观察到光强度响应阈值均在1015个光子厘米-2秒-1左右。虽然在电流钳配置中以零电流模式记录视锥细胞使实验人员能够记录该细胞的实际静息膜电位,但我们观察到光引发的超极化(图1,ij)继之以短去极化,这些在视网膜下注射的视网膜更明显,与jaws-gfp表达水平比在玻璃体内注射的视网膜中更高相关。正如预期,jaws诱导的光电流的幅度随激发波长而变化,峰值在575nm处(图1k)。施加渐增的刺激频率显示,在8.1016个光子厘米-2秒-1下,直至30hz都可以获得可靠的光电流并伴返回基线(图1l)。
pr1.7启动子在人类视锥细胞中驱动强大且高度特异性的基因表达
总之,我们在非人灵长类动物中的数据首次显示了与光遗传学视力恢复应用相容的非侵入性、特异性和高水平灵长类动物中央凹视锥细胞转导。然而,由于启动子活性显示出重大的跨物种变化(29,35,36),我们认为有必要在人类细胞和组织中验证pr1.7。由于缺乏良好的人类光感受器细胞系或其他可用于测试视锥细胞启动子活性的效率的模型,我们使用了源自人类诱导性多能干细胞(ips)的3d视网膜类器官(37)。我们生成了富含光感受器的视网膜类器官,并用在pr1.7启动子的控制下编码gfp的aav2-7m8载体感染它们(数据未显示)。早在感染后5天就观察到gfp表达,并持续增加直到在第43天终止实验以进行分析。这些类器官中的gfp表达与人视锥细胞抑制蛋白(hcar)免疫染色共定位(数据未显示)。最后,由于人类视网膜类器官并不代表成熟的人类视网膜的所有特征,我们验证了pr1.7启动子在人类死后视网膜外植体中的功效和特异性。如以前所述培养人类视网膜外植体(38),并用一滴aav2-7m8-pr1.7-gfp进行感染(数据未显示)。感染15天后,在冷冻切片上分析gfp表达。所述表达限于onl(仅未显示),并与视锥细胞标志物m/l-视蛋白共定位(数据未显示)。这些数据共同指向pr1.7在导致在人类视锥细胞中限制的基因表达上的高效率和特异性。
体内眼睛注射安全性研究
然后,我们在玻璃体内注射aav2-7m8-pr1.7-jaws-gfp和视网膜下注射aav9-7m8-pr1.7-jaws-gfp后评价了免疫响应。
检测视网膜异常和浸润
注射后2个月,通过对视网膜冷冻切片的h&e染色和炎性细胞免疫化学(ihc)来评价炎症(免疫反应)。基于视网膜切片中的h&e染色和显微镜观察,既没有玻璃体内施用aav2-7m8-pr1.7-jaws-gfp(图4a)也没有视网膜下注射avv9-7m8-pr1.7-jaws-gfp(图4b)与细胞浸润或与视网膜组织紊乱有关,与以前部分中的killerred和gfp眼睛相反。
免疫组织化学检测炎症标志物
为了分析局部适应性免疫响应,我们对注射了aav2-7m8-pr1.7-jaws-gfp和avv9-7m8-pr1.7-jaws-gfp这两种构建体的猴子视网膜进行了ihc分析。将来自视网膜下处理的动物和玻璃体内处理的动物的冷冻切片用抗人hlaabc(mhci)、抗hla-dr(主要组织相容性复合物ii(mhcii)、抗人cd8、抗f4/80进行染色。没有切片对上述标志物呈阳性。对胶质原纤维酸性蛋白(gfap)离子钙结合接头分子1(iba1)——一种小胶质细胞和巨噬细胞的造血标志物——的染色为阴性(图5与avv9-7m8-pr1.7-jaws-gfp相关;aav2-7m8-pr1.7-jaws-gfp的数据未显示)。
讨论:
在灵长类动物中,中央凹占视网膜表面积的不到1%,但它为初级视觉皮层中约50%的细胞提供输入(1)。视锥细胞在视网膜最薄和最脆弱的部分——中央凹中的高度集中,给予了高度敏锐的视力,而在治疗干预期间维护该区域中视锥细胞的独特功能(39)和结构(40)是极为重要的。通过利用视网膜下或玻璃体内注射的不同施用途径,可以靶向中央凹视锥细胞(35,41,42),但中央凹脱离可能会导致机械损伤,尤其是在退化的视网膜中(43)。由于所有这些原因,需要向中央凹递送治疗剂而不使该区域脱离的方式。玻璃体内注射是一种递送治疗剂而不使视网膜脱离的简单外科方式。基因治疗载体可在啮齿动物中通过玻璃体内注射靶向外视网膜,而不会损害光感受器(17,35)。但是,到目前为止,尚未实现通过玻璃体内注射向灵长类动物视锥细胞的安全有效基因递送,这可能是由于所述载体在玻璃体内明显稀释并导致功效丧失之故。使用以较低的局部浓度提供高水平基因表达的细胞类型特异性启动子对于克服这一挑战至关重要(29,44)。
在这项研究中,我们试图利用各种启动子与aav2-7m8衣壳相结合,通过非侵入性玻璃体内注射来首次实现强而专一的视锥细胞转导。我们选择了三种启动子,并且并列测试了它们的视锥细胞转导特异性和强度。当视网膜下递送时,在小鼠视网膜中体内测试的所有启动子均导致在感光层中的转基因表达。mcar启动子导致在视杆细胞和视锥细胞中的表达。出乎意料的是,玻璃体内递送后,只有pr1.7维持了它对视锥细胞的特异性,而pr2.1和mcar引起了在内视网膜神经元中的非特异性基因表达。mcar和pr2.1在内视网膜细胞中引起了非特异性表达,使得它们不适合光遗传学应用,在光遗传学应用中,下游神经元中的任何表达都将抵消来自光感受器的响应。随后对每个启动子序列内tf结合位点的计算机分析,提出了用pr1.7的转导更特异性和观察到用mcar启动子缺乏特异性的基础。接下来,为了研究配备有pr1.7启动子的aav2-7m8转导中央凹视锥细胞的能力,我们在猕猴眼睛中实施了基因递送研究。通过玻璃体内施用在中央凹中使用aav2-7m8-pr1.7,将基因表达完全限制在灵长类动物视锥细胞中。
玻璃体内注射途径的一个缺点是,与视网膜下施用相比,施用到该隔室中的aav与免疫系统相互作用的敏感性更高(32)。已经显示,抗体中和对非人灵长类动物中玻璃体内aav载体介导的基因递送造成障碍,并且这可能对人类应用造成挑战。因此,我们旨在为具有针对aav2的中和抗体的患者开发另一种基因递送方法。为了这个目的,我们通过在远端位点处视网膜下施用aav9-7m8来测试向中央凹视锥细胞的基因递送(表2)。我们证明了用这种新的递送方法可以获得稳健的光响应,这要归功于载体横向扩散并在小泡之外介导表达的能力。使用相同的光遗传学视锥细胞再活化策略,我们证明了这种方法也提供由jaws介导的稳健光响应,但与玻璃体内途径相比,视锥细胞的百分比更高(4,15)。
我们的体内发现共同指出了视网膜基因递送中的三个重要考虑因素。首先,增强的aav载体,无论是通过定向进化(aav2-7m8(35))还是合理设计(aav9-7m8(17))获得的,都可以在亲本血清型无法提供足够基因递送的情况下实现治疗目的。确实,aav2和aav9不能进行有效的非侵入性中央凹靶向(30,31),而7m8修饰的载体弥合了这个差距。其次,强大的细胞类型特异性启动子允许节省剂量,这对于基因疗法的安全性是重要的(即避免免疫响应)。第三,我们的研究表明,载体施用途径对转基因表达模式的影响不可忽视。最后,为了补充我们在动物中的体内结果,我们在人体组织中进行了一组离体测试,该测试与体内实验相结合,构成了一个用于验证临床应用的基因疗法的多用途平台。在此描述的载体-启动子组合将在所有需要视锥细胞靶向的视网膜疾病中找到用途。可以基于患者的血清学状态和靶疾病的自然病史来考虑各施用途径和载体(见表2)。pr1.7和aav2-7m8的组合当递送到玻璃体中时,对于在人类中央凹视锥细胞中表达治疗基因是理想的,并且可以是与光遗传学一起使色素性视网膜炎中仍然休眠的视锥细胞复苏的理想方式(4)。由于在全色盲中视锥细胞既存在于中心,也存在于周边,因此使用aav9-7m8-pr1.7在周边进行基因递送会更加有效,因为它将治疗基因既递送到中央凹视锥细胞中又递送到周边视锥细胞中。
我们的体内实验进一步确认aav9-7m8-pr1.7和aav2-7m8-pr1.7载体的安全性,因为它们在注射后不会引发免疫响应。
表2:用于视锥细胞定向基因疗法的aav载体施用策略(nab:中和抗体;cgna3:环核苷酸门控通道α3;cgnb3:环核苷酸门控通道β3)。
序列:
seqidno:1:没有间隔子的插入肽7m8
lgettrp
seqidno:2:插入肽
netitrp
seqidno:3:插入肽
kagqann
seqidno:4:插入肽
kdpkttn
seqidno:5:插入肽
kdtdttr
seqidno:6:插入肽
raggsvg
seqidno:7:插入肽
avdttkf
seqidno:8:插入肽
stgkvpn
seqidno:9:插入肽7m8
aalgettrpa
seqidno:10:野生型aav9vp1衣壳
maadgylpdwlednlsegirewwalkpgapqpkanqqhqdnarglvlpgykylgpgngldkgepvnaadaaalehdkaydqqlkagdnpylkynhadaefqerlkedtsfggnlgravfqakkrlleplglveeaaktapgkkrpveqspqepdssagigksgaqpakkrlnfgqtgdtesvpdpqpigeppaapsgvgsltmasgggapvadnnegadgvgsssgnwhcdsqwlgdrvittstrtwalptynnhlykqisnstsggssndnayfgystpwgyfdfnrfhchfsprdwqrlinnnwgfrpkrlnfklfniqvkevtdnngvktiannltstvqvftdsdyqlpyvlgsahegclppfpadvfmipqygyltlndgsqavgrssfycleyfpsqmlrtgnnfqfsyefenvpfhssyahsqsldrlmnplidqylyylsktingsgqnqqtlkfsvagpsnmavqgrnyipgpsyrqqrvsttvtqnnnsefawpgasswalngrnslmnpgpamashkegedrffplsgslifgkqgtgrdnvdadkvmitneeeikttnpvatesygqvatnhqsaqqaqtgwvqnqgilpgmvwqdrdvylqgpiwakiphtdgnfhpsplmggfgmkhpppqilikntpvpadpptafnkdklnsfitqystgqvsveiewelqkenskrwnpeiqytsnyyksnnvefavntegvyseprpigtryltr
seqidno:11:重组aav9衍生载体的vp1衣壳
maadgylpdwlednlsegirewwalkpgapqpkanqqhqdnarglvlpgykylgpgngldkgepvnaadaaalehdkaydqqlkagdnpylkynhadaefqerlkedtsfggnlgravfqakkrlleplglveeaaktapgkkrpveqspqepdssagigksgaqpakkrlnfgqtgdtesvpdpqpigeppaapsgvgsltmasgggapvadnnegadgvgsssgnwhcdsqwlgdrvittstrtwalptynnhlykqisnstsggssndnayfgystpwgyfdfnrfhchfsprdwqrlinnnwgfrpkrlnfklfniqvkevtdnngvktiannltstvqvftdsdyqlpyvlgsahegclppfpadvfmipqygyltlndgsqavgrssfycleyfpsqmlrtgnnfqfsyefenvpfhssyahsqsldrlmnplidqylyylsktingsgqnqqtlkfsvagpsnmavqgrnyipgpsyrqqrvsttvtqnnnsefawpgasswalngrnslmnpgpamashkegedrffplsgslifgkqgtgrdnvdadkvmitneeeikttnpvatesygqvatnhqsaqaalgettrpaqaqtgwvqnqgilpgmvwqdrdvylqgpiwakiphtdgnfhpsplmggfgmkhpppqilikntpvpadpptafnkdklnsfitqystgqvsveiewelqkenskrwnpeiqytsnyyksnnvefavntegvyseprpigtryltr
seqidno:12:pr1.7启动子
ggaggctgaggggtggggaaagggcatgggtgtttcatgaggacagagcttccgtttcatgcaatgaaaagagtttggagacggatggtggtgactggactatacacttacacacggtagcgatggtacactttgtattatgtatattttaccacgatctttttaaagtgtcaaaggcaaatggccaaatggttccttgtcctatagctgtagcagccatcggctgttagtgacaaagcccctgagtcaagatgacagcagcccccataactcctaatcggctctcccgcgtggagtcatttaggagtagtcgcattagagacaagtccaacatctaatcttccaccctggccagggccccagctggcagcgagggtgggagactccgggcagagcagagggcgctgacattggggcccggcctggcttgggtccctctggcctttccccaggggccctctttccttggggctttcttgggccgccactgctcccgctcctctccccccatcccaccccctcaccccctcgttcttcatatccttctctagtgctccctccactttcatccacccttctgcaagagtgtgggaccacaaatgagttttcacctggcctggggacacacgtgcccccacaggtgctgagtgactttctaggacagtaatctgctttaggctaaaatgggacttgatcttctgttagccctaatcatcaattagcagagccggtgaaggtgcagaacctaccgcctttccaggcctcctcccacctctgccacctccactctccttcctgggatgtgggggctggcacacgtgtggcccagggcattggtgggattgcactgagctgggtcattagcgtaatcctggacaagggcagacagggcgagcggagggccagctccggggctcaggcaaggctgggggcttcccccagacaccccactcctcctctgctggacccccacttcatagggcacttcgtgttctcaaagggcttccaaatagcatggtggccttggatgcccagggaagcctcagagttgcttatctccctctagacagaaggggaatctcggtcaagagggagaggtcgccctgttcaaggccacccagccagctcatggcggtaatgggacaaggctggccagccatcccaccctcagaagggacccggtggggcaggtgatctcagaggaggctcacttctgggtctcacattcttggatccggttccaggcctcggccctaaatagtctccctgggctttcaagagaaccacatgagaaaggaggattcgggctctgagcagtttcaccacccaccccccagtctgcaaatcctgacccgtgggtccacctgccccaaaggcggacgcaggacagtagaagggaacagagaacacataaacacagagagggccacagcggctcccacagtcaccgccaccttcctggcggggatgggtggggcgtctgagtttggttcccagcaaatccctctgagccgcccttgcgggctcgcctcaggagcaggggagcaagaggtgggaggaggaggtctaagtcccaggcccaattaagagatcaggtagtgtagggtttgggagcttttaaggtgaagaggcccgggctgatcccacaggccagtataaagcgccgtgaccctcaggtgatgcgccagggccggctgccgtcggggacagggctttccatagcc
seqidno:13:jaws-gfp=halo57+2个突变+kgc+gfp+er2
mtavsttattvlqatqsdvlqeiqsnfllnssiwvnialagvvillfvamgrdlesprakliwvatmlvplvsissyaglasgltvgflqmppghalagqevlspwgryltwtfstpmillalglladtdiaslftaitmdigmcvtglaaalitsshllrwvfygiscaffvavlyvllvqwpadaeaagtseifgtlriltvvlwlgypilfalgsegvallsvgvtswgysgldilakyvfaflllrwvaanegtvsgsgmgigsggaapaddrpvvksritsegeyipldqidinvapagavskgeelftgvvpilveldgdvnghkfsvsgegegdatygkltlkficttgklpvpwptlvttltygvqcfsrypdhmkqhdffksampegyvqertiffkddgnyktraevkfegdtlvnrielkgidfkedgnilghkleynynshnvyimadkqkngikvnfkirhniedgsvqladhyqqntpigdgpvllpdnhylstqsalskdpnekrdhmvllefvtaagitlgmdelykvafcyenev
seqidno:14:jaws=halo57+2个突变+kgc+er2
mtavsttattvlqatqsdvlqeiqsnfllnssiwvnialagvvillfvamgrdlesprakliwvatmlvplvsissyaglasgltvgflqmppghalagqevlspwgryltwtfstpmillalglladtdiaslftaitmdigmcvtglaaalitsshllrwvfygiscaffvavlyvllvqwpadaeaagtseifgtlriltvvlwlgypilfalgsegvallsvgvtswgysgldilakyvfaflllrwvaanegtvsgsgmgigsggaapaddrpvvksritsegeyipldqidinvapagavafcyenev
seqidno:15:halo57+2个突变+kgc
mtavsttattvlqatqsdvlqeiqsnfllnssiwvnialagvvillfvamgrdlesprakliwvatmlvplvsissyaglasgltvgflqmppghalagqevlspwgryltwtfstpmillalglladtdiaslftaitmdigmcvtglaaalitsshllrwvfygiscaffvavlyvllvqwpadaeaagtseifgtlriltvvlwlgypilfalgsegvallsvgvtswgysgldilakyvfaflllrwvaanegtvsgsgmgigsggaapaddrpvvksritsegeyipldqidinv
参考文献:
在整个本申请中,各种参考文献描述了本发明所属领域的现状。这些参考文献的公开内容特此通过引用并入本公开中。
1.
2.kolbh,zhangl,dekorverl,cuencan.猴子视网膜中钙视网膜蛋白免疫反应性无长突细胞类型的新发现(anewlookatcalretinin-immunoreactiveamacrinecelltypesinthemonkeyretina.)j.comp.neurol.2002;453(2):168–84.
3.wiklerkc,williamsrw,rakicp.光感受器马赛克:恒河猴视网膜中视杆细胞和视锥细胞的数量和分布(photoreceptormosaic:numberanddistributionofrodsandconesintherhesusmonkeyretina.)j.comp.neurol.1990;297(4):499–508.
4.busskampv等人,视锥细胞光感受器的遗传再活化恢复色素性视网膜炎的视觉响应(geneticreactivationofconephotoreceptorsrestoresvisualresponsesinretinitispigmentosa.)[互联网].science2010;329(5990):413–7.
5.byrnelc等人,病毒介导的rdcvf和rdcvfl表达在视网膜变性中保护视锥细胞和视杆细胞光感受器(viral-mediatedrdcvfandrdcvflexpressionprotectsconeandrodphotoreceptorsinretinaldegeneration.)[互联网].j.clin.invest.2015;125(1):105–16.
6.komáromyam等人,基因疗法拯救先天性全色盲的视锥细胞功能(genetherapyrescuesconefunctionincongenitalachromatopsia.)hum.mol.genet.2010;19:2581–2593.
7.maguiream等人,基因转移对leber先天性黑蒙症的安全性和有效性(safetyandefficacyofgenetransferforleber’scongenitalamaurosis.)n.engl.j.med.2008;358(21):2240–2248.
8.bainbridgejwb等人,基因治疗对leber先天性黑蒙症的视功能的效应(effectofgenetherapyonvisualfunctioninleber’scongenitalamaurosis.)n.engl.j.med.2008;358(21):2231–9.
9.cideciyanav等人,对rpe65异构酶缺乏症的人类基因疗法激活视力的类视色素循环,但视杆细胞动力学缓慢(humangenetherapyforrpe65isomerasedeficiencyactivatestheretinoidcycleofvisionbutwithslowrodkinetics.)proc.natl.acad.sci.u.s.a.2008;105(39):15112–7.
10.bainbridgejwb等人,基因疗法对leber先天性黑蒙症的长期效应(long-termeffectofgenetherapyonleber’scongenitalamaurosis.)n.engl.j.med.2015;150504083137004.
11.jacobsonsg等人,儿童失明基因治疗的视力改善和下降(improvementanddeclineinvisionwithgenetherapyinchildhoodblindness.)n.engl.j.med.2015;150503141523009.
12.jacobsonsg等人,由rpe65突变导致的leber先天性黑蒙症的基因疗法:在15名儿童和成人中随访3年的安全性和有效性(genetherapyforlebercongenitalamaurosiscausedbyrpe65mutations:safetyandefficacyin15childrenandadultsfollowedupto3years.)arch.ophthalmol.2012;130(1):9–24.
13.maclarenre等人,无脉络膜症患者的视网膜基因疗法:1/2期临床试验的初步发现(retinalgenetherapyinpatientswithchoroideremia:initialfindingsfromaphase1/2clinicaltrial.)lancet2014;383(9923):1129–1137.
14.duncanjl.向视网膜下空间递送疗法的视觉后果(visualconsequencesofdeliveringtherapiestothesubretinalspace.)jamaophthalmol.2017;135(3):242-243.doi:10.1001/jamaophthalmol.2016.5659.
15.chuongas等人,用红移微生物视紫红质的非侵入性光学抑制(noninvasiveopticalinhibitionwithared-shiftedmicrobialrhodopsin)[互联网].natneurosci2014;17(8):1123–1129.
16.dalkarad等人,用于从玻璃体递送治疗性外视网膜基因的新型腺相关病毒的体内定向进化(invivo-directedevolutionofanewadeno-associatedvirusfortherapeuticouterretinalgenedeliveryfromthevitreous).sci.transl.med.2013;5(189):189ra76-189ra76.
17.khabouh等人,对通过工程化aav2衣壳变体-7m8增强视网膜转导的机制的见解(insightintothemechanismsofenhancedretinaltransductionbytheengineeredaav2capsidvariant-7m8.)biotechnol.bioeng.[在印刷之前在线发表:2016年6月];doi:10.1002/bit.26031
18.yeg-j等人,全色盲和其他视网膜疾病的基因疗法的视锥细胞特异性启动子(cone-specificpromotersforgenetherapyofachromatopsiaandotherretinaldiseases.)hum.genether.2016;27(1):72–82.
19.yeg等人,raav2tyf-pr1.7-hcngb3,一种用于治疗全色盲的重组aav载体,在cngb3基因缺陷小鼠中的安全性和生物分布评价(safetyandbiodistributionevaluationincngb3-deficientmiceofraav2tyf-pr1.7-hcngb3,arecombinantaavvectorfortreatmentofachromatopsia)2016;27(1):27–37.
20.kolstadkd等人,视网膜变性中腺相关病毒介导的基因递送的变化(changesinadeno-associatedvirus-mediatedgenedeliveryinretinaldegeneration.)hum.genether.2010;21(5):571–578.
21.vaccao等人,在屏障受损的dp71-null小鼠模型中aav介导的基因递送(aav-mediatedgenedeliveryindp71-nullmousemodelwithcompromisedbarriers.)[互联网].glia2014;62(3):468–76.
22.satohs等人,小鼠视锥细胞视蛋白表达的空间构图由骨形态发生蛋白通过下游效应子coup-tf核受体的信号传导进行调节(thespatialpatterningofmouseconeopsinexpressionisregulatedbybonemorphogeneticproteinsignalingthroughdownstreameffectorcoup-tfnuclearreceptors.)j.neurosci.2009;29(40):12401–11.
23.pickrellsw,zhux,wangx,craftcm.破译小鼠视锥细胞抑制蛋白基因中已知的顺式元件对其视锥细胞特异性表达的贡献。(decipheringthecontributionofknowncis-elementsinthemouseconearrestingenetoitscone-specificexpression.)investig.ophthalmol.vis.sci.2004;45(11):3877–3884.
24.vonmeringc等人,string7-蛋白相互作用的整合和预测中的最新进展(string7-recentdevelopmentsintheintegrationandpredictionofproteininteractions.)nucleicacidsres.2007;35(suppl.1):358–362.
25.blazeke,mittlerg,meisterernstm.rna聚合酶ii的中介体(themediatorofrnapolymeraseii.)chromosoma2005;113(8):399–408.
26.regulatorslt.致编辑的信:中介体复合物蛋白亚基的统一命名法(lettertotheeditoraunifiednomenclatureforproteinsubunitsofmediatorcomplexes.)mol.cell2004;14:553–557.
27.boydjm,vermas,uhlmanne.14584个更正(14584corrections.)annu.rev.microbiol.1998;95:2–3.
28.vietsk,eldredkc,jrrjj.脊椎动物和无脊椎动物中光感受器构图的机理(mechanismsofphotoreceptorpatterninginvertebratesandinvertebrates.)trendsgenet.2016;32(10):638–659.
29.ramachandranps等人,非人类灵长类动物视网膜中aav7m8和aav8bp2的剂量和安全性评价(evaluationofdoseandsafetyofaav7m8andaav8bp2inthenon-humanprimateretina.)hum.genether.[在印刷之前在线发表:2016年10月];doi:10.1089/hum.2016.111
30.vandenberghelh等人,aav9靶向非人类灵长类动物视网膜中的视锥细胞光感受器(aav9targetsconephotoreceptorsinthenonhumanprimateretina.)plosone2013;8(1):e53463.
31.vandenberghelh等人,在猴子中aav2和aav8光感受器基因疗法的剂量阈值(dosagethresholdsforaav2andaav8photoreceptorgenetherapyinmonkey.)sci.transl.med.2011;3(88):88ra54.
32.kottermanma等人,抗体中和造成向非人灵长类动物玻璃体内递送腺相关病毒载体基因的障碍(antibodyneutralizationposesabarriertointravitrealadeno-associatedviralvectorgenedeliverytonon-humanprimates.)genether.2014;(august):1–11.
33.senguptaa等人,红移的通道视紫红质刺激恢复失明小鼠、猕猴视网膜和人视网膜中的光响应(red-shiftedchannelrhodopsinstimulationrestoreslightresponsesinblindmice,macaqueretina,andhumanretina.)embomolmed2016;1–17.
34.bellcl,gurdabl,vanvlietk,agbandje-mckennam,wilsonjm.腺相关病毒血清型9衣壳的半乳糖结合域鉴定。(identificationofthegalactosebindingdomainoftheadeno-associatedvirusserotype9capsid.)j.virol.2012;86(13):7326–7333.
35.dalkarad等人,用于从玻璃体治疗性外视网膜基因递送的新型腺相关病毒的体内定向进化(invivo-directedevolutionofanewadeno-associatedvirusfortherapeuticouterretinalgenedeliveryfromthevitreous.)[互联网].sci.transl.med.2013;5:189ra76.
36.yinl等人,玻璃体内注射aav2转导猕猴内视网膜(intravitrealinjectionofaav2transducesmacaqueinnerretina.)invest.ophthalmol.vis.sci.2011;52(5):2775–83.
37.reichmans,terraya,slembroucka,nanteauc,orieuxg.从汇合的人ips细胞到自形成神经视网膜和视网膜色素上皮(fromconfluenthumanipscellstoself-formingneuralretinaandretinalpigmentedepithelium)[在印刷之前在线发表:2014];doi:10.1073/pnas.1324212111
38.fradotm,busskampv,bennettj.眼科学中的基因疗法:在培养物上的验证(genetherapyinophthalmology:validationoncultured)2011;593(may):587–593.
39.sinhar等人,塑造灵长类动物中央凹感觉性质的细胞和回路机制(cellularandcircuitmechanismsshapingtheperceptualpropertiesoftheprimatefovea).cell2017;168(3):413–426.e12.
40.andersondh,fishersk.灵长类动物中央凹视锥细胞与色素上皮的关系(therelationshipofprimatefovealconestothepigmentepithelium.)j.ultrastruct.res.1979;67(1):23–32.
41.alloccam等人,新型腺相关病毒血清型有效转导鼠类光感受器(noveladeno-associatedvirusserotypesefficientlytransducemurinephotoreceptors.)j.virol.2007;81(20):11372–80.
42.kaycn等人,使用新型衣壳突变的aav载体通过玻璃体内递送靶向光感受器(targetingphotoreceptorsviaintravitrealdeliveryusingnovel,capsid-mutatedaavvectors.)plosone2013;8(4):e62097.
43.jacobsonsg等人,由rpe65突变导致的leber先天性黑蒙症的基因疗法:在15名儿童和成人中随访3年的安全性和有效性(genetherapyforlebercongenitalamaurosiscausedbyrpe65mutations:safetyandefficacyinfifteenchildrenandadultsfolloweduptothreeyears).arch.ophthalmol.2012;130(1):9–24.
44.tenenbauml,lehtonene,monahanpe.与使用基于腺相关病毒的载体有关的风险的评价(evaluationofrisksrelatedtotheuseofadeno-associatedvirus-basedvectors.)curr.genether.2003;3(6):545–65.
45.boydrf等人,在狗中使用玻璃体内施用的aav载体的光感受器靶向基因递送(photoreceptor-targetedgenedeliveryusingintravitreallyadministeredaavvectorsindogs.)genether.2016;23(2):223–230.
46.yeg-j等人,raav2tyf-pr1.7-hcngb3,一种用于治疗全色盲的重组aav载体,在食蟹猕猴中的安全性和生物分布评价(safetyandbiodistributionevaluationincynomolgusmacaquesofraav2tyf-pr1.7-hcngb3,arecombinantaavvectorfortreatmentofachromatopsia.)hum.genether.clin.dev.2016;27(1):hum.2015.164.
47.maguiream等人,基因转移对leber先天性黑蒙症的安全性和有效性(safetyandefficacyofgenetransferforleber’scongenitalamaurosis.)n.engl.j.med.2008;358(21):2240–8.
48.gernouxg,wilsonjm,muellerc.调节性和耗竭性t细胞对aav衣壳的反应(regulatoryandexhaustedtcellresponsestoaavcapsid.)hum.genether.2017;28(4):338–349.
49.choivw,asokana,habermanra,samulskirj.重组腺相关病毒载体的产生(productionofrecombinantadeno-associatedviralvectors.)curr.protoc.hum.genet.2007;chapter12:unit12.9.
50.aurnhammerc等人,用于检测和定量腺相关病毒血清型2衍生的反向末端重复序列的通用实时pcr(universalreal-timepcrforthedetectionandquantificationofadeno-associatedvirusserotype2-derivedinvertedterminalrepeatsequences.)hum.genether.methods2012;23(1):18–28.
51.delyferm-n等人,人类视网膜脱离的转录组学分析揭示炎症反应和光感受器死亡。(transcriptomicanalysisofhumanretinaldetachmentrevealsbothinflammatoryresponseandphotoreceptordeath.)plosone2011;6(12):e28791.
52.reichmans等人,同源框基因chx10/vsx2调节内视网膜中的rdcvf启动子活性(thehomeoboxgenechx10/vsx2regulatesrdcvfpromoteractivityintheinnerretina.)hum.mol.genet.2010;19(2):250–61.
序列表
<110>法国国家卫生及研究医学协会(inserm)
索邦大学(sorbonneuniversite)
<120>包括视网膜下递送治疗有效量的重组aav9衍生载体的在对象的视锥细胞光感受器中表达目的多核苷酸的方法
<130>b2763pc00
<150>ep17306430
<151>2017-10-20
<160>15
<170>patentinversion3.5
<210>1
<211>7
<212>prt
<213>人工序列
<220>
<223>没有间隔子的7m8肽
<400>1
leuglygluthrthrargpro
15
<210>2
<211>7
<212>prt
<213>人工序列
<220>
<223>插入肽
<400>2
asngluthrilethrargpro
15
<210>3
<211>7
<212>prt
<213>人工序列
<220>
<223>插入肽
<400>3
lysalaglyglnalaasnasn
15
<210>4
<211>7
<212>prt
<213>人工序列
<220>
<223>插入肽
<400>4
lysaspprolysthrthrasn
15
<210>5
<211>7
<212>prt
<213>人工序列
<220>
<223>插入肽
<400>5
lysaspthraspthrthrarg
15
<210>6
<211>7
<212>prt
<213>人工序列
<220>
<223>插入肽
<400>6
argalaglyglyservalgly
15
<210>7
<211>7
<212>prt
<213>人工序列
<220>
<223>插入肽
<400>7
alavalaspthrthrlysphe
15
<210>8
<211>7
<212>prt
<213>人工序列
<220>
<223>插入肽
<400>8
serthrglylysvalproasn
15
<210>9
<211>10
<212>prt
<213>人工序列
<220>
<223>7m8肽
<400>9
alaalaleuglygluthrthrargproala
1510
<210>10
<211>733
<212>prt
<213>腺相关病毒9
<400>10
metalaalaaspglytyrleuproasptrpleugluaspasnleuser
151015
gluglyileargglutrptrpalaleulysproglyalaproglnpro
202530
lysalaasnglnglnhisglnaspasnalaargglyleuvalleupro
354045
glytyrlystyrleuglyproglyasnglyleuasplysglyglupro
505560
valasnalaalaaspalaalaalaleugluhisasplysalatyrasp
65707580
glnglnleulysalaglyaspasnprotyrleulystyrasnhisala
859095
aspalaglupheglngluargleulysgluaspthrserpheglygly
100105110
asnleuglyargalavalpheglnalalyslysargleuleuglupro
115120125
leuglyleuvalgluglualaalalysthralaproglylyslysarg
130135140
provalgluglnserproglngluproaspserseralaglyilegly
145150155160
lysserglyalaglnproalalyslysargleuasnpheglyglnthr
165170175
glyaspthrgluservalproaspproglnproileglyglupropro
180185190
alaalaproserglyvalglyserleuthrmetalaserglyglygly
195200205
alaprovalalaaspasnasngluglyalaaspglyvalglyserser
210215220
serglyasntrphiscysaspserglntrpleuglyaspargvalile
225230235240
thrthrserthrargthrtrpalaleuprothrtyrasnasnhisleu
245250255
tyrlysglnileserasnserthrserglyglyserserasnaspasn
260265270
alatyrpheglytyrserthrprotrpglytyrpheasppheasnarg
275280285
phehiscyshispheserproargasptrpglnargleuileasnasn
290295300
asntrpglypheargprolysargleuasnphelysleupheasnile
305310315320
glnvallysgluvalthraspasnasnglyvallysthrilealaasn
325330335
asnleuthrserthrvalglnvalphethraspserasptyrglnleu
340345350
protyrvalleuglyseralahisgluglycysleuproprophepro
355360365
alaaspvalphemetileproglntyrglytyrleuthrleuasnasp
370375380
glyserglnalavalglyargserserphetyrcysleuglutyrphe
385390395400
proserglnmetleuargthrglyasnasnpheglnphesertyrglu
405410415
phegluasnvalprophehissersertyralahisserglnserleu
420425430
aspargleumetasnproleuileaspglntyrleutyrtyrleuser
435440445
lysthrileasnglyserglyglnasnglnglnthrleulyspheser
450455460
valalaglyproserasnmetalavalglnglyargasntyrilepro
465470475480
glyprosertyrargglnglnargvalserthrthrvalthrglnasn
485490495
asnasnsergluphealatrpproglyalasersertrpalaleuasn
500505510
glyargasnserleumetasnproglyproalametalaserhislys
515520525
gluglygluaspargphepheproleuserglyserleuilephegly
530535540
lysglnglythrglyargaspasnvalaspalaasplysvalmetile
545550555560
thrasngluglugluilelysthrthrasnprovalalathrgluser
565570575
tyrglyglnvalalathrasnhisglnseralaglnglnalaglnthr
580585590
glytrpvalglnasnglnglyileleuproglymetvaltrpglnasp
595600605
argaspvaltyrleuglnglyproiletrpalalysileprohisthr
610615620
aspglyasnphehisproserproleumetglyglypheglymetlys
625630635640
hisproproproglnileleuilelysasnthrprovalproalaasp
645650655
proprothralapheasnlysasplysleuasnserpheilethrgln
660665670
tyrserthrglyglnvalservalgluileglutrpgluleuglnlys
675680685
gluasnserlysargtrpasnprogluileglntyrthrserasntyr
690695700
tyrlysserasnasnvalgluphealavalasnthrgluglyvaltyr
705710715720
sergluproargproileglythrargtyrleuthrarg
725730
<210>11
<211>743
<212>prt
<213>人工序列
<220>
<223>重组aav9衍生载体的vp1衣壳
<400>11
metalaalaaspglytyrleuproasptrpleugluaspasnleuser
151015
gluglyileargglutrptrpalaleulysproglyalaproglnpro
202530
lysalaasnglnglnhisglnaspasnalaargglyleuvalleupro
354045
glytyrlystyrleuglyproglyasnglyleuasplysglyglupro
505560
valasnalaalaaspalaalaalaleugluhisasplysalatyrasp
65707580
glnglnleulysalaglyaspasnprotyrleulystyrasnhisala
859095
aspalaglupheglngluargleulysgluaspthrserpheglygly
100105110
asnleuglyargalavalpheglnalalyslysargleuleuglupro
115120125
leuglyleuvalgluglualaalalysthralaproglylyslysarg
130135140
provalgluglnserproglngluproaspserseralaglyilegly
145150155160
lysserglyalaglnproalalyslysargleuasnpheglyglnthr
165170175
glyaspthrgluservalproaspproglnproileglyglupropro
180185190
alaalaproserglyvalglyserleuthrmetalaserglyglygly
195200205
alaprovalalaaspasnasngluglyalaaspglyvalglyserser
210215220
serglyasntrphiscysaspserglntrpleuglyaspargvalile
225230235240
thrthrserthrargthrtrpalaleuprothrtyrasnasnhisleu
245250255
tyrlysglnileserasnserthrserglyglyserserasnaspasn
260265270
alatyrpheglytyrserthrprotrpglytyrpheasppheasnarg
275280285
phehiscyshispheserproargasptrpglnargleuileasnasn
290295300
asntrpglypheargprolysargleuasnphelysleupheasnile
305310315320
glnvallysgluvalthraspasnasnglyvallysthrilealaasn
325330335
asnleuthrserthrvalglnvalphethraspserasptyrglnleu
340345350
protyrvalleuglyseralahisgluglycysleuproprophepro
355360365
alaaspvalphemetileproglntyrglytyrleuthrleuasnasp
370375380
glyserglnalavalglyargserserphetyrcysleuglutyrphe
385390395400
proserglnmetleuargthrglyasnasnpheglnphesertyrglu
405410415
phegluasnvalprophehissersertyralahisserglnserleu
420425430
aspargleumetasnproleuileaspglntyrleutyrtyrleuser
435440445
lysthrileasnglyserglyglnasnglnglnthrleulyspheser
450455460
valalaglyproserasnmetalavalglnglyargasntyrilepro
465470475480
glyprosertyrargglnglnargvalserthrthrvalthrglnasn
485490495
asnasnsergluphealatrpproglyalasersertrpalaleuasn
500505510
glyargasnserleumetasnproglyproalametalaserhislys
515520525
gluglygluaspargphepheproleuserglyserleuilephegly
530535540
lysglnglythrglyargaspasnvalaspalaasplysvalmetile
545550555560
thrasngluglugluilelysthrthrasnprovalalathrgluser
565570575
tyrglyglnvalalathrasnhisglnseralaglnalaalaleugly
580585590
gluthrthrargproalaglnalaglnthrglytrpvalglnasngln
595600605
glyileleuproglymetvaltrpglnaspargaspvaltyrleugln
610615620
glyproiletrpalalysileprohisthraspglyasnphehispro
625630635640
serproleumetglyglypheglymetlyshisproproproglnile
645650655
leuilelysasnthrprovalproalaaspproprothralapheasn
660665670
lysasplysleuasnserpheilethrglntyrserthrglyglnval
675680685
servalgluileglutrpgluleuglnlysgluasnserlysargtrp
690695700
asnprogluileglntyrthrserasntyrtyrlysserasnasnval
705710715720
gluphealavalasnthrgluglyvaltyrsergluproargproile
725730735
glythrargtyrleuthrarg
740
<210>12
<211>1724
<212>dna
<213>人工序列
<220>
<223>pr1.7启动子
<400>12
ggaggctgaggggtggggaaagggcatgggtgtttcatgaggacagagcttccgtttcat60
gcaatgaaaagagtttggagacggatggtggtgactggactatacacttacacacggtag120
cgatggtacactttgtattatgtatattttaccacgatctttttaaagtgtcaaaggcaa180
atggccaaatggttccttgtcctatagctgtagcagccatcggctgttagtgacaaagcc240
cctgagtcaagatgacagcagcccccataactcctaatcggctctcccgcgtggagtcat300
ttaggagtagtcgcattagagacaagtccaacatctaatcttccaccctggccagggccc360
cagctggcagcgagggtgggagactccgggcagagcagagggcgctgacattggggcccg420
gcctggcttgggtccctctggcctttccccaggggccctctttccttggggctttcttgg480
gccgccactgctcccgctcctctccccccatcccaccccctcaccccctcgttcttcata540
tccttctctagtgctccctccactttcatccacccttctgcaagagtgtgggaccacaaa600
tgagttttcacctggcctggggacacacgtgcccccacaggtgctgagtgactttctagg660
acagtaatctgctttaggctaaaatgggacttgatcttctgttagccctaatcatcaatt720
agcagagccggtgaaggtgcagaacctaccgcctttccaggcctcctcccacctctgcca780
cctccactctccttcctgggatgtgggggctggcacacgtgtggcccagggcattggtgg840
gattgcactgagctgggtcattagcgtaatcctggacaagggcagacagggcgagcggag900
ggccagctccggggctcaggcaaggctgggggcttcccccagacaccccactcctcctct960
gctggacccccacttcatagggcacttcgtgttctcaaagggcttccaaatagcatggtg1020
gccttggatgcccagggaagcctcagagttgcttatctccctctagacagaaggggaatc1080
tcggtcaagagggagaggtcgccctgttcaaggccacccagccagctcatggcggtaatg1140
ggacaaggctggccagccatcccaccctcagaagggacccggtggggcaggtgatctcag1200
aggaggctcacttctgggtctcacattcttggatccggttccaggcctcggccctaaata1260
gtctccctgggctttcaagagaaccacatgagaaaggaggattcgggctctgagcagttt1320
caccacccaccccccagtctgcaaatcctgacccgtgggtccacctgccccaaaggcgga1380
cgcaggacagtagaagggaacagagaacacataaacacagagagggccacagcggctccc1440
acagtcaccgccaccttcctggcggggatgggtggggcgtctgagtttggttcccagcaa1500
atccctctgagccgcccttgcgggctcgcctcaggagcaggggagcaagaggtgggagga1560
ggaggtctaagtcccaggcccaattaagagatcaggtagtgtagggtttgggagctttta1620
aggtgaagaggcccgggctgatcccacaggccagtataaagcgccgtgaccctcaggtga1680
tgcgccagggccggctgccgtcggggacagggctttccatagcc1724
<210>13
<211>552
<212>prt
<213>人工序列
<220>
<223>jaws-gfp=halo57+2个突变+kgc+gfp+er2
<400>13
metthralavalserthrthralathrthrvalleuglnalathrgln
151015
seraspvalleuglngluileglnserasnpheleuleuasnserser
202530
iletrpvalasnilealaleualaglyvalvalileleuleupheval
354045
alametglyargaspleugluserproargalalysleuiletrpval
505560
alathrmetleuvalproleuvalserilesersertyralaglyleu
65707580
alaserglyleuthrvalglypheleuglnmetproproglyhisala
859095
leualaglyglngluvalleuserprotrpglyargtyrleuthrtrp
100105110
thrpheserthrprometileleuleualaleuglyleuleualaasp
115120125
thraspilealaserleuphethralailethrmetaspileglymet
130135140
cysvalthrglyleualaalaalaleuilethrserserhisleuleu
145150155160
argtrpvalphetyrglyilesercysalaphephevalalavalleu
165170175
tyrvalleuleuvalglntrpproalaaspalaglualaalaglythr
180185190
sergluilepheglythrleuargileleuthrvalvalleutrpleu
195200205
glytyrproileleuphealaleuglysergluglyvalalaleuleu
210215220
servalglyvalthrsertrpglytyrserglyleuaspileleuala
225230235240
lystyrvalphealapheleuleuleuargtrpvalalaalaasnglu
245250255
glythrvalserglyserglymetglyileglyserglyglyalaala
260265270
proalaaspaspargprovalvallysserargilethrserglugly
275280285
glutyrileproleuaspglnileaspileasnvalalaproalagly
290295300
alavalserlysglyglugluleuphethrglyvalvalproileleu
305310315320
valgluleuaspglyaspvalasnglyhislyspheservalsergly
325330335
gluglygluglyaspalathrtyrglylysleuthrleulyspheile
340345350
cysthrthrglylysleuprovalprotrpprothrleuvalthrthr
355360365
leuthrtyrglyvalglncyspheserargtyrproasphismetlys
370375380
glnhisaspphephelysseralametprogluglytyrvalglnglu
385390395400
argthrilephephelysaspaspglyasntyrlysthrargalaglu
405410415
vallysphegluglyaspthrleuvalasnargilegluleulysgly
420425430
ileaspphelysgluaspglyasnileleuglyhislysleuglutyr
435440445
asntyrasnserhisasnvaltyrilemetalaasplysglnlysasn
450455460
glyilelysvalasnphelysilearghisasnilegluaspglyser
465470475480
valglnleualaasphistyrglnglnasnthrproileglyaspgly
485490495
provalleuleuproaspasnhistyrleuserthrglnseralaleu
500505510
serlysaspproasnglulysargasphismetvalleuleugluphe
515520525
valthralaalaglyilethrleuglymetaspgluleutyrlysval
530535540
alaphecystyrgluasngluval
545550
<210>14
<211>300
<212>prt
<213>人工序列
<220>
<223>jaws=halo57+2个突变+kgc+er2
<400>14
metthralavalserthrthralathrthrvalleuglnalathrgln
151015
seraspvalleuglngluileglnserasnpheleuleuasnserser
202530
iletrpvalasnilealaleualaglyvalvalileleuleupheval
354045
alametglyargaspleugluserproargalalysleuiletrpval
505560
alathrmetleuvalproleuvalserilesersertyralaglyleu
65707580
alaserglyleuthrvalglypheleuglnmetproproglyhisala
859095
leualaglyglngluvalleuserprotrpglyargtyrleuthrtrp
100105110
thrpheserthrprometileleuleualaleuglyleuleualaasp
115120125
thraspilealaserleuphethralailethrmetaspileglymet
130135140
cysvalthrglyleualaalaalaleuilethrserserhisleuleu
145150155160
argtrpvalphetyrglyilesercysalaphephevalalavalleu
165170175
tyrvalleuleuvalglntrpproalaaspalaglualaalaglythr
180185190
sergluilepheglythrleuargileleuthrvalvalleutrpleu
195200205
glytyrproileleuphealaleuglysergluglyvalalaleuleu
210215220
servalglyvalthrsertrpglytyrserglyleuaspileleuala
225230235240
lystyrvalphealapheleuleuleuargtrpvalalaalaasnglu
245250255
glythrvalserglyserglymetglyileglyserglyglyalaala
260265270
proalaaspaspargprovalvallysserargilethrserglugly
275280285
glutyrileproleuaspglnileaspileasnval
290295300
<210>15
<211>300
<212>prt
<213>人工序列
<220>
<223>halo57+2个突变+kgc
<400>15
metthralavalserthrthralathrthrvalleuglnalathrgln
151015
seraspvalleuglngluileglnserasnpheleuleuasnserser
202530
iletrpvalasnilealaleualaglyvalvalileleuleupheval
354045
alametglyargaspleugluserproargalalysleuiletrpval
505560
alathrmetleuvalproleuvalserilesersertyralaglyleu
65707580
alaserglyleuthrvalglypheleuglnmetproproglyhisala
859095
leualaglyglngluvalleuserprotrpglyargtyrleuthrtrp
100105110
thrpheserthrprometileleuleualaleuglyleuleualaasp
115120125
thraspilealaserleuphethralailethrmetaspileglymet
130135140
cysvalthrglyleualaalaalaleuilethrserserhisleuleu
145150155160
argtrpvalphetyrglyilesercysalaphephevalalavalleu
165170175
tyrvalleuleuvalglntrpproalaaspalaglualaalaglythr
180185190
sergluilepheglythrleuargileleuthrvalvalleutrpleu
195200205
glytyrproileleuphealaleuglysergluglyvalalaleuleu
210215220
servalglyvalthrsertrpglytyrserglyleuaspileleuala
225230235240
lystyrvalphealapheleuleuleuargtrpvalalaalaasnglu
245250255
glythrvalserglyserglymetglyileglyserglyglyalaala
260265270
proalaaspaspargprovalvallysserargilethrserglugly
275280285
glutyrileproleuaspglnileaspileasnval
290295300
- 还没有人留言评论。精彩留言会获得点赞!