一种稳定性好的醋酸奥曲肽注射液及其制备方法和其应用与流程
1.本发明属于药物制剂技术领域,具体涉及一种稳定性好的醋酸奥曲肽注射液及其制备方法和其应用。
背景技术:
2.奥曲肽(octreotide)由8个氨基酸组成的环状多肽化合物,生长抑素类似物,具有对抗生长激素和胰高血糖素的活性,通过减少内脏血流量,减轻与胃肠肿瘤相关的潮红和腹泻,但作用持续时间更长。临床主要将醋酸奥曲肽注射液用于治疗肢端肥大症、胃肠胰内分泌肿瘤、预防胰腺手术后并发症和食管-胃静脉曲张出血等。
3.醋酸奥曲肽注射液存在如下缺陷:一是乳酸甘露醇缓冲液采用活性炭吸附热原、杂质和色素,延长生产周期且造成物料损耗;二是滤芯影响生产周期且增加微生物感染风险,影响药品质量和安全有效性;三是注射液置于2-8℃避光保存,在光照、高温下稳定性较差,长期存放易导致单杂、总杂含量超标,影响安全性。为此,有必要开发一种稳定性好的醋酸奥曲肽注射液,保障临床用药的安全有效性。
技术实现要素:
4.本发明的目的在于提供一种醋酸奥曲肽注射液,所述注射液由0.001-0.05%(w/v)的醋酸奥曲肽、渗透压调节剂、ph调节剂和注射用水组成,注射液ph4.0-4.5,注射液的渗透压为285-320mosmol/kg。
5.本发明优选的技术方案,所述注射液中醋酸奥曲肽含量为0.005-0.04%,优选为0.005%、0.01%、0.03%的任一种。
6.本发明优选的技术方案,所述ph调节剂选自磷酸、磷酸氢二钠、磷酸二氢钠、碳酸氢钠、碳酸钠、氢氧化钠、乳酸的任一种或其组合。
7.本发明优选的技术方案,所述注射液中的磷酸含量为0.01-1%(w/v),优选为0.04-0.08%(w/v)。
8.本发明优选的技术方案,注射液中的渗透压调节剂为甘露醇,注射液中的甘露醇含量为1-10%(w/v),优选为4.5-6%(w/v)。
9.本发明优选的技术方案,按重量/体积百分比计,醋酸奥曲肽注射液中含有0.005%醋酸奥曲肽、0.08%磷酸、4.5%甘露醇,氢氧化钠调ph4.0-4.5。
10.本发明优选的技术方案,按重量/体积百分比计,醋酸奥曲肽注射液中含有0.01%醋酸奥曲肽,0.08%磷酸,4.5%甘露醇,氢氧化钠调ph4.0-4.5。
11.本发明优选的技术方案,按重量/体积百分比计,醋酸奥曲肽注射液中含有0.03%醋酸奥曲肽,0.08%磷酸,4.5%甘露醇,氢氧化钠调ph4.0-4.5。
12.本发明的优选技术方案中,注射液中的脱苏氨醇8奥曲肽含量≤0.5%,其他单杂含量≤0.5%,总杂含量≤2.0%。
13.本发明的优选技术方案中,注射液中,每1mg醋酸奥曲肽中含细菌内毒素≤100eu。
14.本发明的优选技术方案中,注射液中,微生物含量≤10cfu/100ml。
15.本发明的优选技术方案中,注射液在加速6个月条件下单杂含量≤0.5%,总杂含量≤2%。
16.本发明的优选技术方案中,注射液在光照10天条件下单杂含量≤0.5%,总杂含量≤2%。
17.本发明的优选技术方案中,所述注射液与0.9%的生理盐水或5%葡萄糖配伍使用,效期末单杂含量≤0.5%,总杂含量≤2%。
18.本发明的另一目的在于提供一种醋酸奥曲肽注射液的制备方法,所述注射液由0.001-0.05%(w/v)的醋酸奥曲肽、渗透压调节剂、ph调节剂和注射用水组成,所述注射液ph4.0-4.5,注射液的渗透压为285-320mosmol/kg,所述注射液的制备方法包括如下步骤:
19.(1)在搅拌条件下,将所需量的磷酸和甘露醇加入到注射用水中至完全溶解,用氢氧化钠溶液调节ph4.0-4.5,再加入所需量的醋酸奥曲肽,制得药液;
20.(2)将制得药液经0.22μm的聚醚砜滤芯两级过滤,即得。
21.本发明的优选技术方案中,所述搅拌转速为30-50hz,优选为38-42hz。
22.本发明的优选技术方案中,过滤压力为0.1mpa。
23.本发明优选的技术方案,所述注射液中醋酸奥曲肽含量为0.005-0.04%,优选为0.005%、0.01%、0.03%的任一种。
24.本发明优选的技术方案,所述ph调节剂选自磷酸、磷酸氢二钠、磷酸二氢钠、碳酸氢钠、碳酸钠、氢氧化钠、乳酸的任一种或其组合。
25.本发明优选的技术方案,所述注射液中的磷酸含量为0.01-1%(w/v),优选为0.04-0.08%(w/v)。
26.本发明优选的技术方案,注射液中的渗透压调节剂为甘露醇,注射液中的甘露醇含量为1-10%(w/v),优选为4.5-6%(w/v)。
27.本发明优选的技术方案,按重量/体积百分比计,醋酸奥曲肽注射液中含有0.005%醋酸奥曲肽、0.08%磷酸、4.5%甘露醇,氢氧化钠调ph4.0-4.5。
28.本发明优选的技术方案,按重量/体积百分比计,醋酸奥曲肽注射液中含有0.01%醋酸奥曲肽,0.08%磷酸,4.5%甘露醇,氢氧化钠调ph4.0-4.5。
29.本发明优选的技术方案,按重量/体积百分比计,醋酸奥曲肽注射液中含有0.03%醋酸奥曲肽,0.08%磷酸,4.5%甘露醇,氢氧化钠调ph4.0-4.5。
30.本发明的优选技术方案中,注射液中的脱苏氨醇8奥曲肽含量≤0.5%,其他单杂含量≤0.5%,总杂含量≤2.0%。
31.本发明的优选技术方案中,注射液中,每1mg醋酸奥曲肽中含细菌内毒素≤100eu。
32.本发明的优选技术方案中,注射液中,微生物含量≤10cfu/100ml。
33.本发明的优选技术方案中,注射液在加速6个月条件下单杂含量≤0.5%,总杂含量≤2%。
34.本发明的优选技术方案中,注射液在光照10天条件下单杂含量≤0.5%,总杂含量≤2%。
35.本发明的优选技术方案中,所述注射液与0.9%的生理盐水或5%葡萄糖配伍使用,效期末单杂含量≤0.5%,总杂含量≤2%。
36.本发明的另一目的在于提供一种醋酸奥曲肽注射液用于制备治疗肢端肥大症、胃肠胰内分泌肿瘤、预防胰腺手术后并发症和食管胃静脉曲张出血药物中的应用。
37.本发明的优选技术方案中,所述注射液采用静脉注射。
38.本发明的优选技术方案中,所述静脉注射时使用生理盐水或5%的葡萄糖的任一种或其组合配伍使用。
39.除非另有说明,本发明涉及液体与液体之间的百分比时,所述的百分比为体积/体积百分比;本发明涉及液体与固体之间的百分比时,所述百分比为体积/重量百分比;本发明涉及固体与液体之间的百分比时,所述百分比为重量/体积百分比;其余为重量/重量百分比。
40.与现有技术相比,本发明具有下述有益效果:
41.1、本发明科学筛选用于制备醋酸奥曲肽注射液的组份及配比,优化制备工艺及参数,显著提高了醋酸奥曲肽注射液的稳定性,显著降低甚至避免了微生物感染风险,显著提高了药品质量,且与生理盐水和5%葡萄糖的任一种或其组合配伍良好,保障临床用药的安全有效性。
42.2、本发明的制备方法操作简便,缩短生产周期,降低物料损耗提高产率,无特殊设备需求、成本更优,适宜工业化生产。
具体实施方式
43.以下参照实施例说明本发明,但本发明不局限于实施例。
44.实施例1醋酸奥曲肽注射液的制备
45.醋酸奥曲肽注射液的配方如下(8万支,规格:0.05mg/ml):
46.名称用量醋酸奥曲肽4g磷酸64g甘露醇3600g氢氧化钠适量注射用水加至80l
47.醋酸奥曲肽注射液的制备包括如下步骤:
48.(1)加入约占全量85%的30℃以下的注射用水至配液罐中,开启搅拌(40
±
2hz),缓缓加入所需量的磷酸和甘露醇,用约占全量2%的注射用水冲洗残留的磷酸至配液罐中,搅拌5~10分钟使甘露醇溶解,用氢氧化钠溶液调节ph4.0-4.5,补加注射用水至全量的99%;
49.(2)将磷酸甘露醇缓冲液冷却至30℃以下,加入所需量的醋酸奥曲肽,用余量的注射用水冲洗盛主药的容器,倒入配液罐,搅拌(40
±
2hz)20分钟,使其完全溶解,检测中间产品的性状、ph值、细菌内毒素、微生物限度及含量,检验合格后,将药液经0.22μm的聚醚砜滤芯两级过滤,滤液,灌装,即得,收率82.9%。
50.实施例2醋酸奥曲肽注射液的制备
51.醋酸奥曲肽注射液的配方如下(8万支,规格:0.1mg/ml):
52.名称用量
醋酸奥曲肽8g磷酸64g甘露醇3600g氢氧化钠适量注射用水加至80l
53.醋酸奥曲肽注射液的制备包括如下步骤:
54.(1)加入约占全量85%的30℃以下的注射用水至配液罐中,开启搅拌(40
±
2hz)缓缓加入所需量的磷酸和甘露醇,用约占全量2%的注射用水冲洗残留的磷酸至配液罐中,搅拌5~10分钟使甘露醇溶解,用氢氧化钠溶液调节ph4.0-4.5,补加注射用水至全量的99%;
55.(2)冷却磷酸甘露醇缓冲液至30℃以下,加入所需量的醋酸奥曲肽,用余量的注射用水冲洗盛主药的容器,倒入配液罐,搅拌(40
±
2hz)20分钟,使其完全溶解,检测中间产品的性状、ph值、细菌内毒素、微生物限度及含量,检验合格后,将药液经0.22μm的聚醚砜滤芯两级过滤,滤液罐装,即得,收率85.7%。
56.实施例3醋酸奥曲肽注射液的制备
57.醋酸奥曲肽注射液的配方如下(8万支,规格:0.3mg/ml):
58.名称用量醋酸奥曲肽24.0g磷酸64g甘露醇3600g氢氧化钠适量注射用水加至80l
59.醋酸奥曲肽注射液的制备包括如下步骤:
60.(1)加入约占全量85%的30℃以下的注射用水至配液罐中,开启搅拌(40
±
2hz)缓缓加入所需量的磷酸和甘露醇,用约占全量2%的注射用水冲洗残留的磷酸至配液罐中,搅拌5~10分钟使甘露醇溶解,用氢氧化钠溶液调节ph4.0-4.5,补加注射用水至全量的99%;
61.(2)冷却磷酸甘露醇缓冲液至30℃以下,加入所需量的醋酸奥曲肽,用余量的注射用水冲洗盛主药的容器,倒入配液罐,搅拌(40
±
2hz)20分钟,使其完全溶解,检测中间产品的性状、ph值、细菌内毒素、微生物限度及含量,检验合格后,将药液经0.22μm的聚醚砜滤芯两级过滤,滤液罐装,即得,收率83.8%。
62.对比例1醋酸奥曲肽注射液的制备
63.醋酸奥曲肽注射液组成(8万支,0.1mg/1ml):
64.[0065][0066]
醋酸奥曲肽注射液的制备方法包括如下步骤:
[0067]
(1)加入约占全量95%的注射用水(温度为80℃)至配液罐中,开启搅拌(40
±
2hz)缓缓加入所需量的乳酸和甘露醇,搅拌5~10分钟使甘露醇溶解,用7.5%碳酸氢钠溶液调节ph值至4.0-4.5,补加注射用水至全量,检查乳酸甘露醇缓冲液的ph值,应在4.0-4.5范围内;
[0068]
(2)加入所需量的醋酸奥曲肽,搅拌(40
±
2hz)20分钟使其完全溶解,进行中间产品测定,检测性状、ph值、细菌内毒素、微生物限度及含量;
[0069]
(3)性状和ph值合格后将药液经0.22μm的聚醚砜滤芯除菌过滤至药液移动接收罐中,罐装,收率77.3%。
[0070]
对比例2本发明醋酸奥曲肽注射液的制备
[0071]
本发明醋酸奥曲肽注射液的配方如下(8万支,0.1mg/1ml):
[0072]
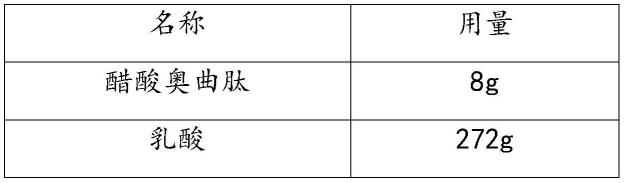
名称用量醋酸奥曲肽8g乳酸272g甘露醇3600g碳酸氢钠适量(约144g)注射用水加至80l
[0073]
本发明醋酸奥曲肽药物组合物的制备方法包括如下步骤:
[0074]
(1)加入约占全量95%的注射用水(温度为80℃)至配液罐中,开启搅拌(40
±
2hz)缓缓加入所需量的乳酸和甘露醇,搅拌5~10分钟使甘露醇溶解,用7.5%碳酸氢钠溶液调节ph值至4.0-4.5,补加注射用水至全量,检查乳酸甘露醇缓冲液的ph值,应在4.0-4.5范围内;
[0075]
(2)加入所需量的醋酸奥曲肽,搅拌(40
±
2hz)20分钟使其完全溶解,进行中间产品测定,检测性状、ph值、细菌内毒素、微生物限度及含量;
[0076]
(3)性状和ph值合格后将药液经0.22μm的聚醚砜滤芯和0.45+0.22μm的复合聚醚砜滤芯过滤除菌至药液移动接收罐中,罐装,收率80.0%。
[0077]
试验例1醋酸奥曲肽注射液的光照稳定性考察研究
[0078]
将实施例1的醋酸奥曲肽注射液与参比制剂(善宁,1ml:0.1mg,生产商:诺华)置于光照4500lx 500lx下光照10天,结果见表1。实施例1的醋酸奥曲肽注射液具有比参比制剂更好的稳定性。
[0079]
表1
[0080][0081]
试验例2醋酸奥曲肽注射液的稳定性考察研究
[0082]
将实施例2制得的醋酸奥曲肽注射液置于25
±
2℃、rh60
±
10%条件下放置6个月,结果见表2。实施例2的醋酸奥曲肽注射液具有比参比制剂更好的稳定性。
[0083]
表2
[0084][0085]
试验例3醋酸奥曲肽注射液的稳定性研究
[0086]
将实施例1的醋酸奥曲肽注射液和参比试剂分别与5%葡萄糖注射液配伍,考察有关物质。结果见表3。实施例1的醋酸奥曲肽注射液与葡萄糖注射液的配伍稳定性比参比制剂更优。
[0087]
表3
[0088][0089]
以上对本发明具体实施方式的描述并不限制本发明,本领域技术人员可以根据本发明作出各种改变或变形,只要不脱离本发明的精神,均应属于本发明权利要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1