一种基于多重HRM分析的氯吡格雷耐药基因检测方法与流程
本发明涉及分子生物学技术领域,具体地说,是一种基于多重HRM分析的氯吡格雷耐药基因检测方法。
背景技术:
氯吡格雷用于治疗冠心病患者经皮冠状动脉介入术(percutaneous coronary intervention,PCI)后预防血栓事件。临床应用时4%~30%患者在常规剂量治疗中达不到预期的抗血小板作用,严重者会导致再次心梗、血栓、死亡等心血管不良事件,这种现象称为氯吡格雷抵抗(clopidogrel resistance,CR)。氯吡格雷是一种前体药物,在体外无活性,通过酶促反应衍生成硫醇代谢物而发挥临床疗效。影响药物转化的相关基因主要包括影响药物吸收的ABCB1和影响代谢过程的肝药酶代谢酶基因。在氯吡格雷的代谢过程中CYP2C19发挥至关重要的作用,CYP2C19基因存在多态性,其中慢代谢型以CYP2C19*2(rs4244285)、CYP2C19*3(rs4986893)变异为主,分别导致了酶失去催化活性和活性降低;CYP2C19*17(rs12248560)突变则显著升高了2C19的转录活性,是一种超快速代谢的基因表型。PON1酶是氯吡格雷代谢过程中的关键酶,控制着2-O-氯吡格雷生成活性产物,PON1Q192R(rs662)基因多态性可能影响血小板的聚集。编码小肠多耐药P-糖蛋白的ABCB1基因多态性会影响氯吡格雷的生物利用度,ABCB13435C>T(rs1045642)与十二指肠P-gp高表达以及P-gp底物生物利用度降低有关。因此,建议在使用氯吡格雷前进行CYP2C19、PON1和ABCB1基因检测,依据患者基因型确定合适给药方案。
高分辨熔解曲线(high-resolution melt,HRM)分析技术是近几年来在国外兴起的一种用于突变扫描和基因分型的最新遗传学分析方法。它是一种高效稳健的PCR技术,不受突变碱基位点与类型的局限,无需序列特异性探针,在PCR结束后直接运行高分辨熔解,即可完成对样品基因型的分析。
中国专利文献CN104450935A公开了一种HRM技术检测氯吡格雷用药相关基因多态性的方法。中国专利文献CN105018583A公开了一种华法林与氯吡格雷个体化用药相关基因多态性检测试剂盒及其应用,可用于鉴别氯吡格雷耐药性相关基因的多态性位点。中国专利文献CN105671165A公开了一种基于Sequenom Mass ARRAY分型系统的检测与氯吡格雷药物抵抗反应相关的基因位点高效分型的试剂盒。但是临床医疗检测的准确性至关重要,而基于HRM技术的高通量检测由于同一反应体系中引物较多,外加其他反应成分,往往检测准确率较低,因此提供一种能同时检测多个位点并且准确率很高的氯吡格雷耐药基因检测引物及方法十分必要。
技术实现要素:
本发明的目的是针对现有技术中的不足,提供一种用于HRM分析法检测氯吡格雷耐药基因的引物组合。
本发明的再一的目的是,提供一种基于多重HRM分析的氯吡格雷耐药基因检测方法。
本发明的另一的目的是,提供氯吡格雷耐药基因检测的引物组合的应用。
为实现上述目的,本发明采取的技术方案是:一种用于HRM分析法检测氯吡格雷耐药基因的引物组合,其用于检测rs4244285、rs4986893、rs12248560三个位点,rs4244285位点的上游引物序列如SEQ ID NO:1所示,rs4244285位点的下游引物序列如SEQ ID NO:2所示;rs4986893位点的上游引物序列如SEQ ID NO:3所示,rs4986893位点的下游引物序列如SEQ ID NO:4所示;rs12248560位点的上游引物序列如SEQ ID NO:5所示,rs12248560位点的下游引物序列如SEQ ID NO:6所示。
一种用于HRM分析法检测氯吡格雷耐药基因的引物组合,其用于检测rs662、rs1045642两个位点,rs662位点的上游引物序列如SEQ ID NO:7所示,rs662位点的下游引物序列如SEQ ID NO:8所示;rs1045642位点的上游引物序列如SEQ ID NO:9所示,rs1045642位点的下游引物序列如SEQ ID NO:10所示。
一种用于HRM分析法检测氯吡格雷耐药基因的引物组合,其用于检测rs4244285、rs4986893、rs12248560、rs662、rs1045642位点,rs4244285位点的上游引物序列如SEQ ID NO:1所示,rs4244285位点的下游引物序列如SEQ ID NO:2所示;rs4986893位点的上游引物序列如SEQ ID NO:3所示,rs4986893位点的下游引物序列如SEQ ID NO:4所示;rs12248560位点的上游引物序列如SEQ ID NO:5所示,rs12248560位点的下游引物序列如SEQ ID NO:6所示;rs662位点的上游引物序列如SEQ ID NO:7所示,rs662位点的下游引物序列如SEQ ID NO:8所示;rs1045642位点的上游引物序列如SEQ ID NO:9所示,rs1045642位点的下游引物序列如SEQ ID NO:10所示。
为实现上述第二个目的,本发明采取的技术方案是:一种检测氯吡格雷耐药基因的HRM分析方法,所述的方法包括以下步骤:对DNA样品进行PCR扩增,PCR反应结束后,对反应体系缓慢程序升温,升温过程中记录荧光信号,获得高分辨率熔解曲线。
优选地,PCR扩增反应在荧光定量PCR分析仪内进行,PCR扩增的条件为:95℃预变性3min,然后进行35个反应循环,每个循环包括95℃、15s的变性,和30s的退火延伸,检测rs4244285、rs4986893、rs12248560三个位点的退火延伸温度为60℃,检测rs662和rs1045642两个位点的退火延伸温度为62℃。
优选地,在荧光定量PCR分析仪内对反应体系进行缓慢程序升温,温度每上升0.2℃记录一次荧光信号。
为实现上述第三个目的,本发明采取的技术方案是:所述的引物组合在制备多重HRM分析的试剂或试剂盒中的应用。
所述的试剂或试剂盒用于检测氯吡格雷耐药基因。
一种基于多重HRM分析的氯吡格雷耐药基因检测的试剂盒,所述的试剂盒包含镁离子、dNTP、rTaq酶、Syto9染料、碱基序列如SEQ ID NO:1、SEQ ID NO:2、SEQ ID NO:3、SEQ ID NO:4、SEQ ID NO:5、SEQ ID NO:6、SEQ ID NO:7、SEQ ID NO:8、SEQ ID NO:9、SEQ ID NO:10所示的引物,前六种引物与后四种引物分开设置。
本发明优点在于:
1、本发明的检测方法是针对多个SNP位点的HRM分型方法,用以分析与氯吡格雷精准用药相关的5个SNP位点rs4244285、rs4986893、rs12248560、rs662和rs1045642。
2、本发明的检测方法可以在同一个反应体系中检测rs4244285、rs4986893、rs12248560三个位点,和/或rs1045642、rs662两个位点,减少了试剂用量,缩短了检测时间。
3、本发明的检测方法对316个经皮冠状动脉介入造影手术的病人的样本进行检测,并用Sanger测序方法进行验证,rs4244285、rs4986893、rs12248560、rs1045642和rs662五个位点的检测正确率分别为100%、99.37%、99.37%、100%、100%,准确率高。
附图说明
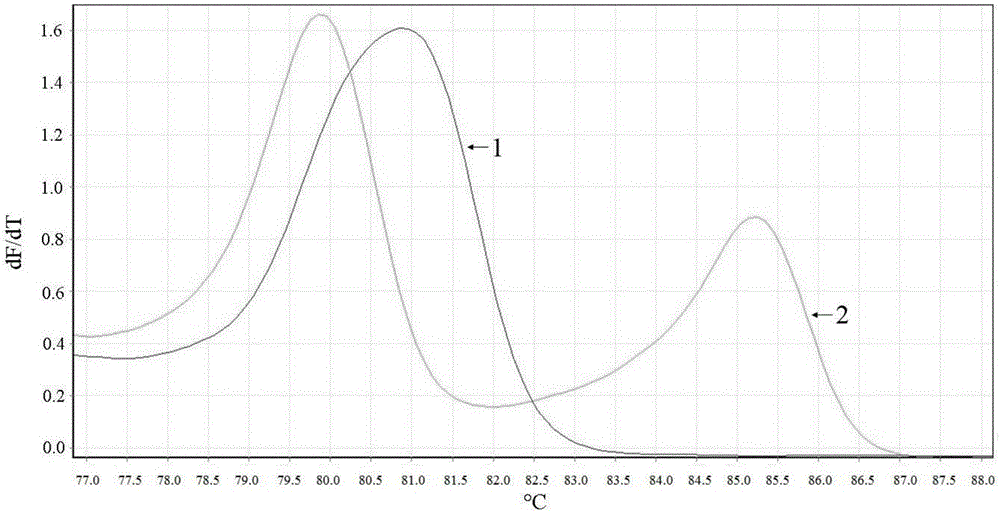
附图1:rs4986893、rs12248560片段多重PCR反应产物的高分辨率熔解曲线负导数图。曲线1中rs4986893引物不含额外的GC序列,可以看到rs4986893的熔解峰与rs12248560的熔解峰重合并相互干扰。曲线2中rs4986893引物添加了GC序列,熔解峰(右)和rs12248560的熔解峰(左)可以很好的分开。
具体实施方式
下面结合实施例对本发明提供的具体实施方式作详细说明。
实施例1本发明的氯吡格雷耐药基因检测方法
材料
Rotor-Gene Q实时荧光定量PCR分析仪(qiagen),rTaq酶(Takara),Syto9荧光染料(Invitrogen),引物(上海生工生物),人基因组DNA样本(提取自经皮冠状动脉介入造影手术的病人)。
方法
1、引物设计:针对五个与氯吡格雷耐药有关的SNP位点:rs4244285、rs4986893、rs12248560、rs1045642和rs662,设计五对PCR扩增引物,使每一对引物产生的扩增子中包含相应的SNP位点。其中,为了提高rs4986893扩增子的Tm值,使其与rs12248560扩增子的熔解峰在HRM曲线上分开,在rs4986893引物的5’端增加一段GC序列(划线部分)。引物序列见表1。
2、PCR扩增体系:扩增反应体积为20μL,包括镁离子1.5mM,dNTP 200μM,rTaq酶0.5U,Syto9染料50pmol,以及1μL基因组DNA样品。用来检测rs4244285、rs4986893、rs12248560三个位点的反应体系中还包括:rs4244285的F、R引物各0.35μM,rs4986893的F、R引物各0.1μM,rs12248560的F、R引物各0.35μM。用来检测rs662和rs1045642的反应体系中还包括rs662的F、R引物各0.15μM,rs1045642的F、R引物各0.35μM。
3、PCR扩增条件:95℃预变性3min,然后进行35个反应循环,每个循环包括95℃、15s的变性,和30s的退火延伸(检测rs4244285、rs4986893、rs12248560三个位点温度为60℃,rs662和rs1045642两个位点为62℃),扩增反应在荧光定量PCR分析仪内进行。
4、HRM分析:PCR反应结束后,在荧光定量PCR分析仪内对反应体系进行缓慢程序升温,温度每上升0.2℃记录一次荧光信号,荧光信号随温度的变化即形成高分辨率熔解曲线。同一个体系中不同的扩增子由于Tm值的不同,熔解峰分布在不同的温度区间。利用HRM分析软件对不同的温度区间进行分析,就可以得到相应SNP位点的基因型。不同SNP的扩增子熔解峰分布区间见表2。
结果
本研究建立了一种针对多个SNP位点的HRM分型方法,用以分析与氯吡格雷精准用药相关的5个SNP位点rs4244285、rs4986893、rs12248560、rs662和rs1045642。引物5’端GC序列的加入使不同SNP位点的考察区间更好的分布在不同的温度范围内(图1)。
表1:针对不同SNP位点的引物序列
表2:不同SNP的扩增子熔解峰分布区间
实施例2本发明的氯吡格雷耐药基因检测方法的准确率验证
使用本发明的氯吡格雷耐药基因检测方法对316个未知基因型的样本进行检测。所有样本均来自仁济医院2015年4月至12月胸闷胸痛入院行经皮冠状动脉介入造影手术,并需要给予阿司匹林+氯吡格雷双联抗血小板治疗的连续病人,其中77个样本为女性,239个样本为男性,年龄范围为35到94岁。检测结果与Sanger测序方法进行比对,rs4244285、rs4986893、rs12248560、rs1045642和rs662五个位点的检测正确率分别为100%、99.37%、99.37%、100%、100%,准确率显著高于常规水平。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!