一种石墨烯负载Fe2Co金属有机骨架材料的制备方法与流程
本发明涉及一种金属有机骨架材料的制备方法。
背景技术:
二十一世纪以来,能源短缺和环境污染成为全世界人们共同面临的问题,新能源的开发也成为了避不开的话题,太阳能,风能等资源被不断的开发、利用,而氢能因其储存量大,产热量高达化石燃料的二倍,清洁无污染等优良的特性而得到人们的关注与研究。氢能的产生途径有很多种,例如:有机废弃物制氢、利用微型藻类持续大量制氢、源于植物原料制氢以及光催化制氢等,其中利用太阳能,将水通过光催化制氢的方法最为常见。利用太阳能来获取氢能的光催化技术,成为了获得氢能的最理想的方法,受到了国内外研究学者的青睐。其中日本学者Fujishima和Honda研究发现当光照n-型半导体TiO2电极时,可导致水分解,使人们认识到利用太阳能光催化制氢的可行性。但因其在光催化制氢的过程中光生电子和空穴复合率高、只能响应紫外光等缺点,限制了其发展。因此开发一种新型的光催化剂迫在眉睫。
金属有机骨架材料是以金属离子或金属簇为中心,与有机配体经配位键自组装而成的配位聚合物。MOFs材料作为一种有机-无机杂化的材料,具有许多传统材料不具有的优良特性,如组分和结构的多样性,较高的比表面积及孔隙率,合成方便等;使得其诸多领域有着广阔的应用前景,如在催化、气体储存、荧光探测等。由于MOFs材料本身具有半导体的性质,最近几年越来越多的研究已经验证了MOFs材料可以吸收太阳光,激发后可产生光生电子,从而可以将其应用于光催化制氢。
金属-有机骨架材料的快速发展是近二十年来无机化学领域的重大突破。MOFs材料是由金属中心或金属簇作为中心点。与有机配体通过配位键自组装连接而成,具有高度周期性的网络结晶配合物,也称为金属配位聚合物[7]。
MOFs这种有机-无机杂化的独特结构特点和它的纳米级别的孔洞尺寸,使它在一个空洞中提供一个或多个催化位点,这是其它材料所不能实现的。因此MOFs材料具有许多诱人的特点:第一,MOFs材料具有组分多样性,通过选择不同的金属离子及不同的配体,就可以合成种类繁多的MOFs材料。第二,MOFs材料的结构具有可调节性能,可以自行设计并合成所想要的结构,并且可以通过功能材料的修饰,来实现MOF材料的功能化。第三,MOFs材料具有大小均匀的多孔结构,较大的比表面积。第四,MOFs材料具 有良好的热稳定性和化学稳定性。第五,合成方法简便、操作简单。
在近三十年的研究中,MOFs材料以惊人的速度发展。在许多化学期刊中,关于MOFs的论文或综述成指数增长,如此快的发展速度也说明了此材料在科学研究领域具有举足轻重的地位。目前为止,研究学者们己经合成了大量的结构新颖、性能良好的MOFs材料,取得众多举世瞩目的科研成效。
在MOFs的蓬勃发展的二十年间,来自世界各国的研究者们投身到这个领域,不断的合成各种各样的结构并拓展其在各个领域的应用。近年来国内的很多研究者们在该领域取得了一定的成就,在国际上也具有深远的影响。
然而现有MOFs材料光解水制氢的效率不高,有待进一步的探究,研制一种光解水制氢效率高的材料。
技术实现要素:
本发明的目的是要解决现有用于光解水制氢的材料制氢效率不高的问题,而提供一种石墨烯负载Fe2Co金属有机骨架材料的制备方法。
本发明的一种石墨烯负载Fe2Co金属有机骨架材料的制备方法是按以下步骤完成的:
一、Fe2Co-MOF材料的制备:向Fe2Co中加入N,N-二甲基甲酰胺Ⅰ和冰醋酸,在超声频率为35KHz~45KHz的条件下超声处理4min~6min,然后加入3,3’,5,5’-偶氮苯四羧酸,在超声频率为35KHz~45KHz的条件下超声处理25min~35min,然后将反应容器放入反应釜中,再将反应釜置于温度为130~150℃的烘箱中反应2h~12h,得到Fe2Co-MOF材料;
步骤一中所述N,N-二甲基甲酰胺Ⅰ与冰醋酸的体积比为2:(0.5~1.5);
步骤一中所述N,N-二甲基甲酰胺Ⅰ的体积与Fe2Co的质量的比为2mL:(10~40)mg;
步骤一中所述Fe2Co与3,3’,5,5’-偶氮苯四羧酸的质量比为1:(1~2)mg;
二、Go/Fe2Co-MOF材料的制备:①将石墨烯溶于N,N-二甲基甲酰胺Ⅱ中,在超声频率为35KHz~45KHz的条件下超声处理50min~70min,得到混合溶液;②将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合后放入反应釜中,再将反应釜置于温度为130~150℃的烘箱中反应3h~5h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料;
步骤二①所述石墨烯的质量与N,N-二甲基甲酰胺Ⅱ的体积的比为(0.2~0.3)mg:2mL;
步骤二②所述步骤二①得到的混合溶液中石墨烯的质量与步骤一得到的Fe2Co-MOF材料的质量比为(0.025~0.25):25。
本发明所述配体3,3’,5,5’-偶氮苯四羧酸按《催化科学与技术,铁(Ⅲ),金属有机框 架作为固体Lewis酸对α-蒎烯易氧化物的异构化,2012》中记载的方法制备。
本发明的有益效果
本发明通过水热(溶剂热)法将配体3,3’,5,5’-偶氮苯四羧酸(3,3’,5,5’-偶氮苯四羧酸,H4abtc)与Fe2Co反应生成Fe2Co-MOF;并采用红外、X-射线单晶衍射对所制得的MOFs材料进行了结构表征,检测结果表明已成功合成了较为纯相的Fe2Co-MOF材料。然后在Fe2Co-MOF材料负载石墨烯,得到不同石墨烯负载量的Go/Fe2Co-MOF材料,通过固体紫外-可见漫反射光谱分析(UV-Vis)测试结果表明:Fe2Co-MOF及0.25%石墨烯负载量的GO/Fe2Co-MOF材料氧化电位-还原电位的能隙值分别为1.65eV、1.55eV;由循环伏安法得到氧化电位能级值为0.42eV,进而可以计算出还原电位能级值为-1.23eV,比氢离子还原氢气的能级值更负,因此具备光催化制氢的能力,采用热重分析(TGA)对本发明制备的Go/Fe2Co-MOF材料的稳定性进行了探究,结果显示本发明制备的Go/Fe2Co-MOF材料在温度低于400℃时具有很好的稳定性。
附图说明
图1为不同石墨烯负载量的Go/Fe2Co-MOF以及配体3,3’,5,5’-偶氮苯四羧酸的红外光谱图;
图2为不同石墨烯负载量的Go/Fe2Co-MOF的X-射线粉末衍射表征结果与其单晶解析模拟图;
图3为试验二制备的Go/Fe2Co-MOF的SEM图;
图4为试验三制备的Go/Fe2Co-MOF的SEM图;
图5为试验四制备的Go/Fe2Co-MOF的SEM图;
图6为试验五制备的Go/Fe2Co-MOF的SEM图;
图7为试验三步骤一制备的Fe2Co-MOF的紫外-可见光吸收谱图;
图8为试验三制备的Go/Fe2Co-MOF的紫外-可见光吸收谱图如;
图9为试验三制备的Go/Fe2Co-MOF的循环伏安法测试图;
图10为试验三制备的Go/Fe2Co-MOF的热失重曲线图;
图11为气相色谱仪制氢实验的标准曲线图;
图12为不同石墨烯负载量的GO/Fe2Co-MOF的产氢量曲线图。
具体实施方式
具体实施方式一:本实施方式的一种石墨烯负载Fe2Co金属有机骨架材料的制备方法是按以下步骤完成的:
一、Fe2Co-MOF材料的制备:向Fe2Co中加入N,N-二甲基甲酰胺Ⅰ和冰醋酸,在超声频率为35KHz~45KHz的条件下超声处理4min~6min,然后加入3,3’,5,5’-偶氮苯四羧酸,在超声频率为35KHz~45KHz的条件下超声处理25min~35min,然后将反应容器放入反应釜中,再将反应釜置于温度为130~150℃的烘箱中反应2h~12h,得到Fe2Co-MOF材料;
步骤一中所述N,N-二甲基甲酰胺Ⅰ与冰醋酸的体积比为2:(0.5~1.5);
步骤一中所述N,N-二甲基甲酰胺Ⅰ的体积与Fe2Co的质量的比为2mL:(10~40)mg;
步骤一中所述Fe2Co与3,3’,5,5’-偶氮苯四羧酸的质量比为1:(1~2)mg;
二、Go/Fe2Co-MOF材料的制备:①将石墨烯溶于N,N-二甲基甲酰胺Ⅱ中,在超声频率为35KHz~45KHz的条件下超声处理50min~70min,得到混合溶液;②将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合后放入反应釜中,再将反应釜置于温度为130~150℃的烘箱中反应3h~5h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料;
步骤二①所述石墨烯的质量与N,N-二甲基甲酰胺Ⅱ的体积的比为(0.2~0.3)mg:2mL;
步骤二②所述步骤二①得到的混合溶液中石墨烯的质量与步骤一得到的Fe2Co-MOF材料的质量比为(0.025~0.25):25。
本实施方式所述配体3,3’,5,5’-偶氮苯四羧酸按《催化科学与技术,铁(Ⅲ),金属有机框架作为固体Lewis酸对α-蒎烯易氧化物的异构化,2012》(Catalysis Science&Technology Iron(III)metal–organic frameworks as solid Lewis acids for the isomerization of a-pinene oxide 2012)中记载的方法制备。
本实施方式通过水热(溶剂热)法将配体3,3’,5,5’-偶氮苯四羧酸(3,3’,5,5’-偶氮苯四羧酸,H4abtc)与Fe2Co反应生成Fe2Co-MOF;并采用红外、X-射线单晶衍射对所制得的MOFs材料进行了结构表征,检测结果表明已成功合成了较为纯相的Fe2Co-MOF材料。然后在Fe2Co-MOF材料负载石墨烯,得到不同石墨烯负载量的Go/Fe2Co-MOF材料,通过固体紫外-可见漫反射光谱分析(UV-Vis)测试结果表明:Fe2Co-MOF及0.25%石墨烯负载量的GO/Fe2Co-MOF材料氧化电位-还原电位的能隙值分别为1.65eV、1.55eV;由循环伏安法得到氧化电位能级值为0.42eV,进而可以计算出还原电位能级值为-1.23eV,比氢离子还原氢气的能级值更负,因此具备光催化制氢的能力,采用热重分析(TGA)对本发明制备的Go/Fe2Co-MOF材料的稳定性进行了探究,结果显示本实施方式制备的Go/Fe2Co-MOF材料在温度低于400℃时具有很好的稳定性。
具体实施方式二:本实施方式与具体实施方式一不同的是:步骤一中所述N,N-二甲 基甲酰胺Ⅰ与冰醋酸的体积比为2:0.9。其他步骤及参数与具体实施方式一相同。
具体实施方式三:本实施方式与具体实施方式一或二不同的是:步骤一中所述N,N-二甲基甲酰胺Ⅰ的体积与Fe2Co的质量的比为2mL:(20~30)mg。其他步骤及参数与具体实施方式一或二相同。
具体实施方式四:本实施方式与具体实施方式一至三之一不同的是:步骤一中所述Fe2Co与3,3’,5,5’-偶氮苯四羧酸的质量的比为1:1.5mg。其他步骤及参数与具体实施方式一至三之一相同。
具体实施方式五:本实施方式与具体实施方式一至四之一不同的是:步骤一中向Fe2Co中加入N,N-二甲基甲酰胺Ⅰ和冰醋酸,在超声频率为40KHz的条件下超声处理5min,然后加入3,3’,5,5’-偶氮苯四羧酸,在超声频率为40KHz的条件下超声处理30min。其他步骤及参数与具体实施方式一至四之一相同。
具体实施方式六:本实施方式与具体实施方式一至五之一不同的是:步骤一中将反应容器放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Fe2Co-MOF材料。其他步骤及参数与具体实施方式一至五之一相同。
具体实施方式七:本实施方式与具体实施方式一至六之一不同的是:步骤二①所述石墨烯的质量与N,N-二甲基甲酰胺Ⅱ的体积的比为0.25mg:2mL。其他步骤及参数与具体实施方式一至六之一相同。
具体实施方式八:本实施方式与具体实施方式一至七之一不同的是:步骤二②所述步骤二①得到的混合溶液中石墨烯的质量与步骤一得到的Fe2Co-MOF材料的质量比为0.0625:25。其他步骤及参数与具体实施方式一至七五之一相同。
具体实施方式九:本实施方式与具体实施方式一至八之一不同的是:步骤二①中将石墨烯溶于N,N-二甲基甲酰胺Ⅱ中,在超声频率为35KHz~45KHz的条件下超声处理60min,得到混合溶液。其他步骤及参数与具体实施方式一至八之一相同。
具体实施方式十:本实施方式与具体实施方式一至九之一不同的是:步骤二②中将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合后放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料。其他步骤及参数与具体实施方式一至九之一相同。
用以下试验来验证本发明的有益效果
试验一、本实验的一种石墨烯负载Fe2Co金属有机骨架材料的制备方法按以下步骤进行:
一、Fe2Co-MOF材料的制备:向40mg的Fe2Co中加入2mL的N,N-二甲基甲酰胺Ⅰ和0.9mL的冰醋酸,在超声频率为40KHz的条件下超声处理5min,然后加入60mg的3,3’,5,5’-偶氮苯四羧酸,在超声频率为40KHz的条件下超声处理30min,然后将反应容器放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Fe2Co-MOF材料;
二、Go/Fe2Co-MOF材料的制备:①将0.1mg石墨烯溶于2mL的N,N-二甲基甲酰胺Ⅱ中,在超声频率为40KHz的条件下超声处理60min,得到混合溶液;②将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料;
本试验中石墨烯的负载量按质量分数计为0.1%。
本试验所述配体3,3’,5,5’-偶氮苯四羧酸按《催化科学与技术,铁(Ⅲ),金属有机框架作为固体Lewis酸对α-蒎烯易氧化物的异构化,2012》(Catalysis Science&Technology Iron(III)metal–organic frameworks as solid Lewis acids for the isomerization of a-pinene oxide 2012)中记载的方法制备。
试验二、本实验的一种石墨烯负载Fe2Co金属有机骨架材料的制备方法按以下步骤进行:
一、Fe2Co-MOF材料的制备:向40mg的Fe2Co中加入2mL的N,N-二甲基甲酰胺Ⅰ和0.9mL的冰醋酸,在超声频率为40KHz的条件下超声处理5min,然后加入60mg的3,3’,5,5’-偶氮苯四羧酸,在超声频率为40KHz的条件下超声处理30min,然后将反应容器放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Fe2Co-MOF材料;
二、Go/Fe2Co-MOF材料的制备:①将0.2mg石墨烯溶于2mL的N,N-二甲基甲酰胺Ⅱ中,在超声频率为40KHz的条件下超声处理60min,得到混合溶液;②将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料;
本试验中石墨烯的负载量按质量分数计为0.2%。
本试验所述配体3,3’,5,5’-偶氮苯四羧酸按《催化科学与技术,铁(Ⅲ),金属有机框架作为固体Lewis酸对α-蒎烯易氧化物的异构化,2012》(Catalysis Science&Technology Iron(III)metal–organic frameworks as solid Lewis acids for the isomerization of a-pinene oxide 2012)中记载的方法制备。
试验三、本实验的一种石墨烯负载Fe2Co金属有机骨架材料的制备方法按以下步骤进行:
一、Fe2Co-MOF材料的制备:向40mg的Fe2Co中加入2mL的N,N-二甲基甲酰胺Ⅰ和0.9mL的冰醋酸,在超声频率为40KHz的条件下超声处理5min,然后加入60mg的3,3’,5,5’-偶氮苯四羧酸,在超声频率为40KHz的条件下超声处理30min,然后将反应容器放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Fe2Co-MOF材料;
二、Go/Fe2Co-MOF材料的制备:①将0.25mg石墨烯溶于2mL的N,N-二甲基甲酰胺Ⅱ中,在超声频率为40KHz的条件下超声处理60min,得到混合溶液;②将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料;
本试验中石墨烯的负载量按质量分数计为0.25%。
本试验所述配体3,3’,5,5’-偶氮苯四羧酸按《催化科学与技术,铁(Ⅲ),金属有机框架作为固体Lewis酸对α-蒎烯易氧化物的异构化,2012》(Catalysis Science&Technology Iron(III)metal–organic frameworks as solid Lewis acids for the isomerization of a-pinene oxide 2012)中记载的方法制备。
试验四、本实验的一种石墨烯负载Fe2Co金属有机骨架材料的制备方法按以下步骤进行:
一、Fe2Co-MOF材料的制备:向40mg的Fe2Co中加入2mL的N,N-二甲基甲酰胺Ⅰ和0.9mL的冰醋酸,在超声频率为40KHz的条件下超声处理5min,然后加入60mg的3,3’,5,5’-偶氮苯四羧酸,在超声频率为40KHz的条件下超声处理30min,然后将反应容器放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Fe2Co-MOF材料;
二、Go/Fe2Co-MOF材料的制备:①将0.5mg石墨烯溶于2mL的N,N-二甲基甲酰胺Ⅱ中,在超声频率为40KHz的条件下超声处理60min,得到混合溶液;②将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料;
本试验中石墨烯的负载量按质量分数计为0.5%。
本试验所述配体3,3’,5,5’-偶氮苯四羧酸按《催化科学与技术,铁(Ⅲ),金属有机框架作为固体Lewis酸对α-蒎烯易氧化物的异构化,2012》(Catalysis Science&Technology Iron(III)metal–organic frameworks as solid Lewis acids for the isomerization of a-pinene oxide 2012)中记载的方法制备。
试验五、本实验的一种石墨烯负载Fe2Co金属有机骨架材料的制备方法按以下步骤进行:
一、Fe2Co-MOF材料的制备:向40mg的Fe2Co中加入2mL的N,N-二甲基甲酰胺Ⅰ和0.9mL的冰醋酸,在超声频率为40KHz的条件下超声处理5min,然后加入60mg的3,3’,5,5’-偶氮苯四羧酸,在超声频率为40KHz的条件下超声处理30min,然后将反应容器放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Fe2Co-MOF材料;
二、Go/Fe2Co-MOF材料的制备:①将1mg石墨烯溶于2mL的N,N-二甲基甲酰胺Ⅱ中,在超声频率为40KHz的条件下超声处理60min,得到混合溶液;②将步骤二①得到的混合溶液与步骤一得到的Fe2Co-MOF材料混合放入反应釜中,再将反应釜置于温度为140℃的烘箱中反应4h,得到Go/Fe2Co-MOF材料,即石墨烯负载Fe2Co金属有机骨架材料;
本试验中石墨烯的负载量按质量分数计为1%。
本试验所述配体3,3’,5,5’-偶氮苯四羧酸按《催化科学与技术,铁(Ⅲ),金属有机框架作为固体Lewis酸对α-蒎烯易氧化物的异构化,2012》(Catalysis Science&Technology Iron(III)metal–organic frameworks as solid Lewis acids for the isomerization of a-pinene oxide 2012)中记载的方法制备。
(一)对试验一至试验五得到的Go/Fe2Co-MOF的表征分析:
①红外光谱分析
对试验一、试验三至试验五制备的不同石墨烯负载量的Go/Fe2Co-MOF以及配体3,3’,5,5’-偶氮苯四羧酸进行检测,得到不同石墨烯负载量的Go/Fe2Co-MOF以及配体3,3’,5,5’-偶氮苯四羧酸的红外光谱如图1所示;其中1为石墨烯负载量为0%的Go/Fe2Co-MOF(即Fe2Co-MOF)的曲线,2为石墨烯负载量为0.1%的Go/Fe2Co-MOF的曲线,3为石墨烯负载量为0.25%的Go/Fe2Co-MOF的曲线,4为石墨烯负载量为0.5%的Go/Fe2Co-MOF的曲线,5为石墨烯负载量为1%的Go/Fe2Co-MOF的曲线,6为配体3,3’,5,5’-偶氮苯四羧酸的曲线。由图1可知,Fe2Co-MOF及GO/Fe2Co-MOF材料在1652cm-1处出现羰基的伸缩振动峰,与配体1696cm-1处出现的羰基峰相比发生了明显的位移;而在1696cm-1处未出现羧基的吸收峰,表明配体中的羧基已全部发生质子化反应,并与金属离子配位。由此可判断,Fe2+离子与羰基氧发生了桥连。
②X射线粉末衍射分析
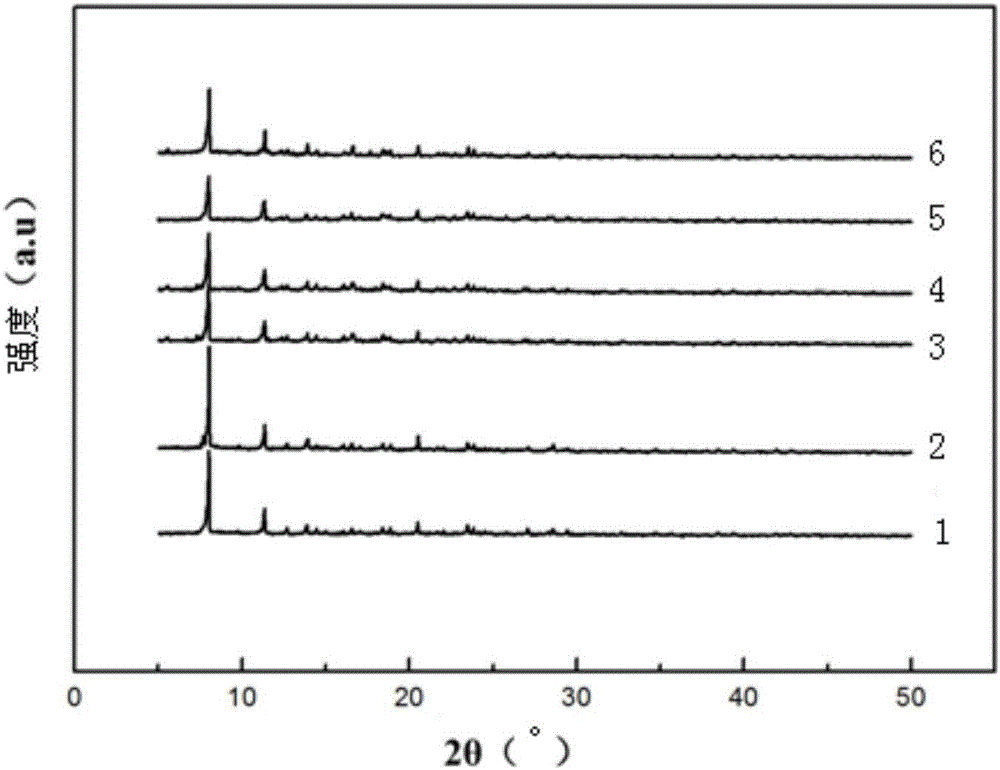
对试验一至试验五制备的不同石墨烯负载量的Go/Fe2Co-MOF进行X-射线检测,以Cu靶(λ=0.15418nm)为X射线源,并设45kV的管电压、8°/min的扫描速率、0.02°的扫描步长、5°~50°的2θ范围。得到试验一至试验五制备的不同石墨烯负载量的Go/Fe2Co-MOF的X-射线粉末衍射表征结果与其单晶解析模拟图如图2所示;其中1为Go/Fe2Co-MOF的模拟曲线,2为石墨烯负载量为0.1%的Go/Fe2Co-MOF的曲线,3为石墨烯负载量为0.2%的Go/Fe2Co-MOF的曲线,4为石墨烯负载量为0.25%的Go/Fe2Co-MOF的曲线,5为石墨烯负载量为0.5%的Go/Fe2Co-MOF的曲线,6为石墨烯负载量为1%的Go/Fe2Co-MOF的曲线。由图2可知,对于不同石墨烯负载量的Go/Fe2Co-MOF来说,这些峰均与样品的标准谱图吻合程度较好,说明均已得到较为纯相的Go/Fe2Co-MOF材料,但是当石墨烯的负载量为0.25%时Go/Fe2Co-MOF的XRD图与标准谱图相比吻合度最好,分别在8.2°、11.3°处出现明显的主特征峰,无论是主特征峰还是杂峰,都能够与模拟图很好的对应,说明的得到了晶型较好而且较纯的Go/Fe2Co-MOF。
③扫描电子显微镜分析
对试验二至试验五制备的不同石墨烯负载量的Go/Fe2Co-MOF进行扫描电子显微镜检测,得到试验二制备的Go/Fe2Co-MOF的SEM图如图3所示,得到试验三制备的Go/Fe2Co-MOF的SEM图如图4所示,得到试验四制备的Go/Fe2Co-MOF的SEM图如图5所示,得到试验五制备的Go/Fe2Co-MOF的SEM图如图6所示,由图3~6可知,负载量过大造成过量的石墨烯覆盖在晶体表面上,并有团聚现象,负载量过小造成晶体上石墨烯覆盖不均匀;当负载量为0.25%(试验三制备的Go/Fe2Co-MOF)时,石墨烯与金属有机骨架材料复合的程度最好。
④紫外-可见吸收光谱分析
对试验三制备的Go/Fe2Co-MOF(石墨烯负载量为0.25%)以及试验三步骤一制备的Fe2Co-MOF进行紫外-可见吸收光谱分析,测试方法:采用的是日本日立公司生产的UV-3010型紫外可见分光光度计,测试的实验条件为:扫描范围在200~800nm之间,扫描间隔为2s,以BaSO4标准白板为参比。得到试验三步骤一制备的Fe2Co-MOF的紫外-可见光吸收谱图如图7所示,得到试验三制备的Go/Fe2Co-MOF的紫外-可见光吸收谱图如图8所示,由图7可以看出,310nm处对光的吸收强度最大,在400-600nm的可见光范围内对光也有较强的吸收,最大吸收波长为750nm;由图8可以看出,GO/Fe2Co-MOF材料测试结果(b)在330nm处对光的吸收强度最大,最大吸收波长为800nm;由此得 出结论两种材料对光的响应能力都比较强,且负载了石墨烯后对光的吸收波长明显增加,同时由光谱图可以计算出氧化电位-还原电位之间的能隙值分别为1.65eV、1.55eV。
⑤循环伏安法分析
对试验三制备的Go/Fe2Co-MOF(石墨烯负载量为0.25%)进行循环伏安检测,测试方法:使用三电极体系,其中包含碳糊工作电极,铂对电极及Ag/AgCl参比电极。采用1mol/L的H2SO4溶液为电解质,0.2~1.0V的扫描范围,50mV/s的扫描速度。
其中制作碳糊电极的方法如下:将石墨与Fe2Co-MOF或GO/Fe2Co-MOF材料混合(质量4/1),在研钵中充分研磨30min,以确保二者混合均匀,再用胶头滴管滴加液体石蜡,置于玻璃管内,插入铜丝,制成碳糊电极。
得到如图9所示的试验三制备的Go/Fe2Co-MOF的循环伏安法测试图。
H+/H2的能级值为零,当金属有机骨架材料的还原电位能级值比零更负时,则可以判定该材料具有光催化制氢性能,相反,则不具有光催化制氢性能。而还原电位能级值可由氧化电位能隙值和氧化电位-还原电位能级值的差值计算得到,所以只需要得到氧化电位能级值就可以计算出还原电位能级值,进而判断是否具有光催化制氢性能。
由图9可以看出,试验三制备的Go/Fe2Co-MOF的氧化电位的能级值为0.42eV,因此可以得到试验三制备的Go/Fe2Co-MOF的还原电位能级值为-1.23eV,比氢离子还原氢气的能级值更负,因此可以判断试验三制备的Go/Fe2Co-MOF具有光催化制氢性能。
⑥热重光谱分析
对试验三制备的Go/Fe2Co-MOF(石墨烯负载量为0.25%)进行热稳定性曲线,得到如图10所示的试验三制备的Go/Fe2Co-MOF的热失重曲线图,从图10可以看出:在30~200℃内,试验三制备的Go/Fe2Co-MOF逐渐失去游离的溶剂分子以及配位的水分子;当温度达到400℃时骨架开始坍塌,600℃以上时,试验三制备的Go/Fe2Co-MOF的骨架完全坍塌。
(二)用试验三制备的Go/Fe2Co-MOF光解水制氢
①标准曲线的制定
分别对不同体积的纯氢气进行了气相色谱分析,得到气相色谱仪制氢实验的标准曲线图如图11所示,标准曲线方程为y=7645.4x-24057,R2=0.996。
②不同石墨烯负载量的GO/Fe2Co-MOF对产氢速率的影响
光解水制氢的实验是在密闭的石英反应器中进行;加入50mg的Fe2Co-MOF或GO/Fe2Co-MOF催化剂、15mL三乙醇胺、85ml蒸馏水;制氢装置经过先抽真空后通 氮气的操作,往复循环三次,以除去溶液中含有的空气和其它杂质气体;在300W氙灯模拟的可见光照射的条件下反应,每隔1h采一次样,共采样7次,并通过气相色谱仪进行氢气含量的测定。
反应条件为:催化剂(试验一至试验五制备的Go/Fe2Co-MOF)的投入量为50mg,15mL三乙醇胺,85mL蒸馏水,在300W的氙灯下进行光催化制氢反应,每1小时采一次样,共测7次,并通过气相色谱仪进行氢气含量的测定。
采用色谱色谱仪的测定条件如下:以N2为载气,采用5的分子筛填料、TCD检测器;设定40℃为初温,80℃柱温,80℃检测室温度,80A电流。
得到不同石墨烯负载量的GO/Fe2Co-MOF的产氢量曲线图如图12所示;其中1为石墨烯负载量为0%的Go/Fe2Co-MOF(即Fe2Co-MOF)的曲线,2为石墨烯负载量为0.1%的Go/Fe2Co-MOF的曲线,3为石墨烯负载量为0.2%的Go/Fe2Co-MOF的曲线,4为石墨烯负载量为0.25%的Go/Fe2Co-MOF的曲线,5为石墨烯负载量为0.5%的Go/Fe2Co-MOF的曲线,6为石墨烯负载量为1%的Go/Fe2Co-MOF的曲线。从图12可以看出:Fe2Co-MOF的制氢量随时间的增大呈现先增后减的趋势,负载石墨烯的Fe2Co-MOF与单独的Fe2Co-MOF相比,制氢量相对增大;不同石墨烯负载量的Fe2Co-MOF相比,石墨烯负载量为0.25%时,制氢量达到最大16μL/(g·h)。
- 还没有人留言评论。精彩留言会获得点赞!