一种鸡蛋粉中氟虫腈砜残留分析标准物质候选物及其制备方法
1.本发明涉及食品检测、加工领域,尤其涉及一种鸡蛋粉中氟虫腈砜残留分析标准物质候选物及其制备方法。
背景技术:
2.氟虫腈是一种苯基吡唑类杀虫剂,曾被广泛应用于农业、兽医等领域。但由于反复使用,氟虫腈容易积累于水体、土壤和农作物中,对一些非靶标生物(蜜蜂、禽类、水生生物等)造成毒害作用,并通过食物链对人体造成影响。研究发现,蛋鸡摄入氟虫腈污染的饲料后,大部分氟虫腈转化成氟虫腈砜,排泄至鸡蛋中。氟虫腈砜是氟虫腈在蛋鸡体内的主要代谢产物,也是氟虫腈在鸡蛋中的残留标示物。
3.gb 2763-2019《食品安全国家标准食品中农药最大残留限量》中规定氟虫腈的残留物为:氟虫腈、氟甲腈、氟虫腈砜、氟虫腈亚砜,以总和计,用氟虫腈表示;鸡蛋中氟虫腈的最大残留限量为20μg/kg。通过药代动力学实验发现,鸡蛋中很少检出氟甲腈和氟虫腈亚砜;氟虫腈即使有检出,但是含量大都低于氟虫腈砜;而且,当鸡蛋中检测不到氟虫腈时,仍有可能存在较高残留的氟虫腈砜。
4.氟虫腈砜的毒性远高于氟虫腈,大量摄入会损害人体的肝脏、甲状腺、肾脏以及生殖系统和神经系统。它的化学性质与氟虫腈相近,易溶于乙腈、丙酮等有机溶剂,容易带负电,分子式为c
12
h4cl2f6n4o2s,化学结构式如下所示:
[0005][0006]
有效的安全评价体系有利于确保农产品及食品安全。标准物质是以特性量值的均匀性、稳定性和准确性等为主要特征的实物形式的计量标准,是保障分析检测体系准确可靠的重要支撑。基体标准物质是具有实际样品特性的标准物质,主要用于分析方法评价、操作人员水平考核以及检测过程质量监控等,是检测机构能力验证考核评价的基准材料。标准物质候选物是为了满足标准物质均匀性、稳定性的特性需求和实际检测工作的需要,经特殊生产加工工艺制备的未赋予标准值和不确定度的产品形态,是标准物质市场流通的实体。规范化的标准物质候选物制备方法有利于确保标准物质产品的持续稳定供应,从而有效满足检测质控的需求。
[0007]
经检索,国内外尚无经动物实验获得特性原料、再经特殊加工工艺制备鸡蛋粉中氟虫腈砜残留分析标准物质候选物的方法体系和技术规程。
技术实现要素:
[0008]
本发明提供了一种鸡蛋粉中氟虫腈砜残留分析标准物质候选物。
[0009]
本发明特别提供了一种鸡蛋粉中氟虫腈砜残留分析标准物质候选物的制备方法,包括以下步骤:
[0010]
(1)动物实验:以鸡蛋中氟虫腈及其代谢物残留限量20μg/kg为目标,通过氟虫腈在蛋鸡体内的药代动力学试验,筛检含15~25μg/kg氟虫腈砜的鸡蛋液原料;
[0011]
(2)原料匀浆:将筛检获得的鸡蛋液原料搅拌均匀;
[0012]
(3)冷冻干燥:将搅拌均匀的鸡蛋液原料通过预冻、分批真空冷冻干燥至恒重;
[0013]
(4)磨粉过筛:将冷冻干燥后的样品粉碎、过筛至鸡蛋粉粒径不大于40目;
[0014]
(5)干粉混匀:收集的所有过筛后的鸡蛋粉混合、搅拌、混匀;
[0015]
(6)干粉初检:将混匀的鸡蛋粉进行均匀性初检;
[0016]
(7)产品包装:将均匀性初检合格的鸡蛋粉分装至样品瓶中,然后进行抽真空包装;
[0017]
(8)辐照灭菌:将包装好的产品进行灭菌处理,获得鸡蛋粉中氟虫腈砜残留分析标准物质候选物,低温保存。
[0018]
具体采用的技术方案如下:
[0019]
一种鸡蛋粉中氟虫腈砜残留分析标准物质候选物的制备方法,包括以下步骤:
[0020]
(1)动物实验。以鸡蛋中氟虫腈及其代谢物残留限量(20μg/kg)为目标,通过氟虫腈在蛋鸡体内的药代动力学试验,筛检含15~25μg/kg氟虫腈砜的鸡蛋液原料。在目标含量附近筛检原料,有利于后期加工的均匀化处理,降低最小取样量,使最终产品更符合天然样品。
[0021]
所述的药代动力学试验,是将氟虫腈按所需剂量装入药用胶囊内,使蛋鸡口服胶囊,一次性给药,给药剂量为0.005~2mg/只,试验周期为28d。每天采集鸡蛋,测定每天每组鸡蛋液中氟虫腈砜含量,绘制残留消除曲线。根据不同剂量给药后各个时间点的氟虫腈砜残留情况,筛选较接近目标含量20μg/kg的鸡蛋液样品。
[0022]
作为优选,针对健康24周龄、平均体重为1.46kg的“大午金凤”蛋鸡,氟虫腈给药剂量分别为:0.005、0.01、0.1mg/只。当剂量为1mg/只或2mg/只时,给药后第2天至第28天,鸡蛋液中氟虫腈砜含量均始终远高于25μg/kg。
[0023]
作为优选,针对含15~25μg/kg氟虫腈砜的鸡蛋液原料,当剂量为0.005mg/只时,鸡蛋采集时间为给药后第6、7天;当剂量为0.01mg/只时,鸡蛋采集时间为给药后第4~10天;当剂量为0.1mg/只时,鸡蛋采集时间为给药后第2天和第17~22天。通过多个剂量多天采集的模式可减少蛋鸡的使用量,降低原料成本。
[0024]
(2)原料匀浆。将步骤(1)中筛检获得的鸡蛋液原料置于洁净的不锈钢圆桶中,用商用电动打蛋机以固定转速搅拌均匀。
[0025]
作为优选,所述的商用电动打蛋机的参数为:双轴,容量为15l,功率为200w,转速为467r/min。
[0026]
所述的搅拌均匀,即从不锈钢圆桶的上、中、下三个部位分别抽取3份鸡蛋液样品检测,氟虫腈砜含量在17.0~20.5μg/kg之间,判断原料已基本混匀。
[0027]
作为优选,原料匀浆在环境温度20
±
2℃、湿度40
±
10%rh条件下,通过搅拌-冷却
消泡-搅拌的方式进行。每搅拌30min置于-80℃冰箱中冷却消泡30min,累计搅拌2h。由于鸡蛋液营养丰富,搅拌时间过长,蛋白容易变性。另外,搅拌过程容易起泡,增大体积,不利于冷冻干燥。经-80℃冰箱冷冻处理30min,不仅可以消泡,还可以降低鸡蛋液的微生物污染。
[0028]
(3)冷冻干燥。将步骤(2)中搅拌均匀的鸡蛋液原料分装于洁净的不锈钢圆盘中,上面用带小孔的铝箔纸包封,置于-80℃冰箱预冻。再分批放入冷冻干燥机中,-80℃真空冷冻干燥至恒重。每批鸡蛋液干燥至恒重用时6d。鸡蛋液原料经冷冻干燥,平均脱水率为75%,即1.25g鸡蛋粉,加入3.75g水,可复原成5g鸡蛋液,直接用于国标法(gb23200.115-2018)检测质控。
[0029]
作为优选,所述的冷冻干燥机的参数为:捕水能力为6kg/24h,功率为950w,冻干面积为0.18~0.27m2,真空度为《10pa。
[0030]
所述的恒重,是指冷冻干燥至6d时,对样品连盘称重,继续冷冻干燥过夜(16h),再次称重,前后两次重量相差小于0.1%,视为恒重。
[0031]
作为优选,采用真空冷冻干燥技术除去鸡蛋液中的水分,脱水率要求达到75%,最终鸡蛋粉产品含水量不高于1.5%,这样的产品在密封状态下始终处于松散状态,不会结块。真空冷冻干燥技术能够保持产品的基本形态,保证其营养物质和维生素等不被破坏,加水复原后,其颜色、味道、物料结构等与之前新鲜的基本相同。同时,这种技术可使产品水分含量很低,抑制微生物的生长和增殖,提高产品的稳定性。
[0032]
作为优选,鸡蛋液的复原,即准确称取鸡蛋粉,以1:3(w/w)准确加入纯净水,涡旋振荡1min,超声10min,30℃避光水浴1h,复原成均质后的鸡蛋液。产品中氟虫腈砜含量最终以鸡蛋粉计。纯净水加入量为鸡蛋粉的3倍,使复原后的鸡蛋液与实际样品几乎无差异。每份鸡蛋粉的取样量建议为1.25g,取样量过大会给样品提取和净化增加负担,影响结果的重复性。水浴有利于鸡蛋液充分复原,但水浴时间不得超过2h,因为氟虫腈及其代谢物在水溶液中光照下有缓慢降解的风险。
[0033]
(4)磨粉过筛。将步骤(3)中冷冻干燥后的蜂窝状鸡蛋样品置于大型粉碎机中,高速粉碎30s。粉碎后的样品过40目筛后收集。未能过筛的样品倒入小型粉碎机中再次粉粹30s,重新过40目筛,再次收集。磨粉过筛损失控制在2%以内。最终产品颗粒大小不大于40目。
[0034]
作为优选,所述的大型粉碎机参数为:容量为4500g,额定功率为550w,频率为50hz。所述的小型粉碎机的参数为:容量为500g,额定功率为500w,频率为50hz。
[0035]
作为优选,磨粉过筛时要求环境温度为20
±
2℃、湿度小于30%rh,以免产品吸潮变质。
[0036]
(5)干粉混匀。将步骤(4)中收集的所有过筛后的鸡蛋粉全部倒入混合机中,混合搅拌16h,充分混匀。
[0037]
作为优选,所述的混合机的参数为:容量为8kg,混合桶转速为0~26r/min,搅拌轴转速为0~100r/min,混合桶功率为40w,搅拌轴功率为25w,工作方式为v型对流混合,自动循环正反转。
[0038]
作为优选,设置混合桶转速为18r/min,搅拌轴转速为36r/min,采用正转1h逆转1h的模式。
[0039]
作为优选,混匀过程要求环境温度为20
±
2℃、湿度小于30%rh,以免产品吸潮变
质。
[0040]
(6)干粉初检。将步骤(5)中混匀的鸡蛋粉,于上下两个取样层,按三分法取样,共取样品6份,进行均匀性初检。初检合格,方能进行产品分装。
[0041]
所述的初检合格,即对抽取的6份样品进行氟虫腈砜含量检测,每份平行检测3次。采用单因素方差分析法(f-检验法),对检测结果进行统计学分析。由f﹤f
α
,p-value﹥0.05,判定该标准物质候选物均匀性初检合格。
[0042]
作为优选,均匀性初检的取样量为1.25g。在最小取样量试验中,0.50~1.50g的取样量均能满足检测方法的重复性要求,说明产品是充分均匀的。但为了复原至5g鸡蛋液,满足国标法检测质控需求,该标准物质候选物的最小取样量设定为1.25g。最终由候选物形成的鸡蛋粉中氟虫腈砜残留分析标准物质产品,其标准值和不确定度均为最小取样量下获得的结果。
[0043]
(7)产品包装。将步骤(6)中均匀性初检合格的鸡蛋粉倒入洁净的电脑智能分装机中,通过振动和红外感应自动分装至样品瓶中。然后用真空包装机进行抽真空包装。
[0044]
所述的智能分装机的参数为:额定功率为180w,分装速度为4~8s/瓶,称重范围为1~30g,误差范围为0.1~0.2g。
[0045]
所述的真空包装机的参数为:包装速度为1~3包/min,功率为120w,真空室尺寸为330
×
275
×
50mm。
[0046]
作为优选,系统设置10.5g规格进行智能分装,使每瓶鸡蛋粉净重大于10g。以每份待测样品1.25g计,每瓶产品大约可称取8份样品用于检测质控。
[0047]
所用样品瓶需经检验密封性能好,其材质对产品无影响。
[0048]
作为优选,所用样品瓶为亚克力瓶,容积为60ml,内胆呈银色,完全避光,每瓶自带压敏垫片,密封性良好。经检验该包装瓶对氟虫腈砜无吸附或降解作用;可置于-20℃冰箱长期保存,不存在冻裂现象。
[0049]
作为优选,真空包装时,样品瓶瓶口向内装入铝箔袋中,通过抽真空除去瓶内空气,并且反向抽真空还可以进一步压紧垫片,避免空气渗入,从而提高了产品的稳定性。
[0050]
(8)辐照灭菌。将步骤(7)中包装好的产品进行灭菌处理,获得鸡蛋粉中氟虫腈砜残留分析标准物质候选物,置于-20℃冰箱长期保存。鸡蛋营养丰富,在生产和加工过程容易污染微生物。灭菌处理是为了彻底消除因微生物污染所引起的鸡蛋粉变质,从而延长产品的保质期。
[0051]
作为优选,采用
60
co辐照进行灭菌处理。相对于其它灭菌工艺,
60
co辐照灭菌更彻底,无需拆封,穿透力较强,经济性较高,处理方式可靠、高效,加工确认简单,一定剂量下无有害物质残留,无需作灭菌后置处理,方便、快捷。
[0052]
所述的
60
co辐照,辐照剂量为500~2000gy,辐照剂量过低,灭菌不彻底;辐照剂量过高,产品容易变质。辐照时环境温度为22℃
±
2℃,湿度小于37%rh。
[0053]
作为优选,
60
co辐照剂量为1000gy,实测值为959~1009gy。
[0054]
与现有产品和技术相比,本发明的有益效果在于:
[0055]
(1)本发明提供的鸡蛋粉中氟虫腈砜残留分析标准物质候选物是目前国内唯一的鸡蛋粉中氟虫腈砜残留分析标准物质的产品形态,由此形成的标准物质产品最终经均匀性检验、稳定性检验和6家实验室联合定值,确定了标准值和不确定度,符合国家标准物质评
审要求。
[0056]
(2)本发明提供的鸡蛋粉中氟虫腈砜残留分析标准物质候选物,涉及的氟虫腈砜是氟虫腈经蛋鸡体内代谢残留于鸡蛋中的代谢物,它与鸡蛋内容物基质紧密结合,所获得的含氟虫腈砜的鸡蛋液原料属于天然样品,完全有别于人为的加标样品;通过加水复原过程,该基体标准物质候选物可还原成含有氟虫腈砜的鸡蛋液,与天然样品基本一致,用于练兵考核、能力验证和实验室间比对时更能反映相关检测技术的准确性和可比性。
[0057]
(3)本发明提供的鸡蛋粉中氟虫腈砜残留分析标准物质候选物的制备方法,包括整套技术流程和相关技术参数,可用于大量生产鸡蛋粉中氟虫腈砜残留分析标准物质产品;针对残留限量有目标的开展动物实验和获取阳性样品,围绕标准物质的均匀性和稳定性要求开展产品加工,解决了检测质控过程中阳性样品获取不可控、均匀性和稳定性较难保证等问题。
[0058]
(4)本发明在基体标准物质候选物加工过程的关键控制点上具有技术特殊性,在规范工艺流程和产品结果上具有创新性,在其他动物源性基体标准物质产品研制生产中具有指导意义和应用前景。特别是对一些尚无标准参照物的代谢物,依据本发明的技术路线可获得接近实际样品的质控样,重点解决了基体标准物质研制领域的卡脖子问题。
附图说明
[0059]
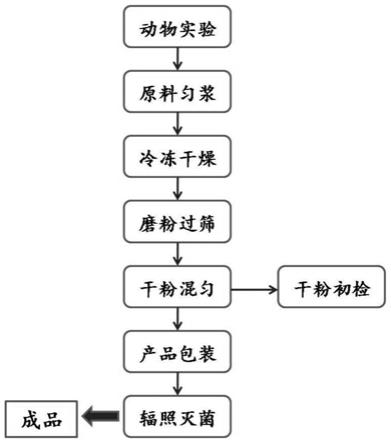
图1为鸡蛋粉中氟虫腈砜残留分析标准物质候选物的制备流程图。
[0060]
图2为不同剂量氟虫腈给药后鸡蛋液中氟虫腈砜的残留消除曲线,其中a图给药量分别为0.005、0.01、0.1mg/只,b图给药量分别为1、2mg/只。
[0061]
图3为氟虫腈砜稳定同位素内标化学结构式。
具体实施方式
[0062]
下面结合附图与实施例,进一步阐明本发明。应理解,这些实施例仅用于说明本发明,而不用于限制本发明的范围。
[0063]
实施例1基体标准物质候选物的制备
[0064]
1.1鸡蛋液原料的获取
[0065]
从杭州的农贸市场、超市随机抽取53份鸡蛋样品,相关信息见表1。按gb 23200.115-2018《食品安全国家标准鸡蛋中氟虫腈及其代谢物残留量的测定液相色谱-质谱联用法》检测,所有样品均不含氟虫腈及其代谢物(氟虫腈砜、氟虫腈亚砜、氟甲腈)。由此可见,以抽样方式获取阳性鸡蛋样品,可控性较差,阳性样品的数量和目标含量经常不能满足一批产品制备规模和检测质控的需求。
[0066]
表1市场抽检鸡蛋来源信息
[0067][0068]
本发明采用动物的药代动力学实验获取含目标分析物的阳性样品,并由此建立了生产技术规范,有利于动物源性基体标准物质产品的持续稳定供应。
[0069]
如图1所示,本发明提供的鸡蛋粉中氟虫腈砜残留分析标准物质候选物的制备方法,技术路线包含:动物实验、原料匀浆、冷冻干燥、磨粉过筛、干粉混匀、干粉初检、产品包装、辐照灭菌。
[0070]
本实施例以残留限量为筛检目标,通过药代动力学实验获得氟虫腈砜含量接近20μg/kg的鸡蛋液原料。
[0071]
具体的方法为:选择健康24周龄、体质量相近的“大午金凤”蛋鸡60只,平均体重为1.46kg,采用3层全阶梯笼养,随机分成3组,每组20只;将氟虫腈按所需剂量装入药用胶囊内,使蛋鸡口服药用胶囊。每组给药剂量分别为:0.005、0.01、0.1、1、2mg/只,试验周期为28d;每天采集鸡蛋,洗净、擦干,分组打蛋,用洁净的食品级塑料样品瓶装,置于-20℃冰箱中保存;使用前恢复至室温,充分均质,同步测定每天每组鸡蛋液中氟虫腈砜含量,绘制得到如图2所示的残留消除曲线。当剂量为1mg/只或2mg/只时,给药后第2天至第28天,鸡蛋液中氟虫腈砜含量均始终远高于25μg/kg。
[0072]
在有效的给药剂量(0.005、0.01、0.1mg/只)下,在特定的采集时间可获得含15~25μg/kg氟虫腈砜的鸡蛋液原料。由表2可见,当剂量为0.005mg/只时,鸡蛋采集时间为给药后第6、7天;当剂量为0.01mg/只时,鸡蛋采集时间为给药后第4~10天;当剂量为0.1mg/只时,鸡蛋采集时间为给药后第2天和第17~22天。通过动物实验可了解代谢物的残留消除规律,采用多个剂量多天采集的模式可在使用较少蛋鸡的情况下获得足够量的各种目标残留
量的鸡蛋液原料。
[0073]
表2动物实验确定的给药剂量、采集时间及对应含量
[0074][0075]
1.2鸡蛋粉复原方式的确定
[0076]
为了方便保存,延长有效期,采用真空冷冻干燥均匀化技术,除去鸡蛋液中游离的水分,制备成鸡蛋粉。具体操作如下:将均质后的鸡蛋液原料分装于洁净的不锈钢圆盘中,上面用带小孔的铝箔纸包封,置于-80℃冰箱预冻。然后分批放入creatrust冻干机中,进行-80℃真空冷冻干燥。在本实施例中,每批鸡蛋液干燥至恒重用时6d。干燥前后称重,脱水率见表3。计算可得,平均脱水率为75%。该产品使用时,准确称取1.25g试样,准确加入3.75g纯净水,涡旋振荡1min,超声10min,30℃避光水浴1h,即可复原成5g鸡蛋液,与均质后的自然样品基本一致。
[0077]
表3鸡蛋液真空冷冻干燥脱水率检测结果
[0078][0079]
本实施例于鸡蛋粉加水后,辅助振荡、超声和水浴的方式,促进鸡蛋液的复原。比较了6份样品超声后30℃避光水浴1h立即提取和室温放置0~2h内随机提取的差异。复原后的鸡蛋液按gb 23200.115-2018检测,对所有测定值进行组间t检验,p值大于0.05,说明复原时水浴操作和不水浴处理对鸡蛋粉中氟虫腈砜的残留检测不存在显著性差异。但增加水浴操作可能更好地促进了鸡蛋粉的复溶,检测结果的重复性相对较好。故本发明采用加水振荡、超声后再30℃避光水浴1h的方式,使鸡蛋粉充分复原成鸡蛋液,然后用于检测质控。
[0080]
1.3关键控制点的分析
[0081]
鸡蛋液经筛检、匀浆、冷冻干燥、磨粉过筛获得鸡蛋粉,再次混匀后,开展均匀性初检。只有通过均匀性初检的鸡蛋粉原料才能进行产品包装,若未通过初检,则需要继续混匀。具体操作如下:在混合机容器的上下两个取样层,按三分法取样,共取样品6份,每份样品取样量为1.25g,按gb 23200.115-2018平行检测3次。本实施例的检测结果见表4。采用单因素方差分析法(f-检验法),对检测结果进行统计学分析。由表5可见,f﹤f
α
,p-value﹥0.05,判定鸡蛋粉原料均匀性初检合格。
[0082]
表4鸡蛋粉原料均匀性初检结果
[0083][0084]
表5鸡蛋粉原料均匀性评估-单因素方差分析
[0085][0086]
备注:ss是离均差平方和,ms是均方,df是自由度,f是统计量,f
α
是在α水平上的临界统计量,p-value是表征显著性的值。
[0087]
当取样量过小时,物质的特征量容易出现不均匀的现象;当取样量过大时,会造成样品的浪费,同时对提取和后续净化造成负担。
[0088]
本实施例开展了最小取样量试验,具体操作是:以不同的取样量各取6份鸡蛋粉样品,按gb 23200.115-2018检测,结果见表6。对所有测定值进行组间t检验,p值均大于0.05,说明0.50g~1.50g的取样量对氟虫腈砜检测结果影响不显著。从测定值的重复性上反应,分别以1g和1.25g的取样量进行检测,rsd值相差极小且均小于2%,说明以这两种取样量开展实验能够获得相对较小的不确定度。而国标法(gb 23200.115-2018)中鸡蛋液的取样量为5g。为了满足国标法检测质控需求,该标准物质候选物的最小取样量设定为1.25g。最终由候选物形成的鸡蛋粉中氟虫腈砜残留分析标准物质产品,其标准值和不确定度均为最小取样量下获得的结果。
[0089]
表6不同取样量下鸡蛋粉原料氟虫腈砜检测结果
[0090][0091]
鸡蛋营养丰富,在生产和加工过程容易污染微生物。本发明采用
60
co辐照灭菌,以
避免产品在保存和运输过程发生变质。
[0092]
本实施例比较了辐照剂量对鸡蛋粉的影响。具体操作如下:随机抽取12瓶产品,其中9瓶平均分成3组,作为辐照组,分别在500gy、1000gy、2000gy剂量下进行辐照灭菌,另外3瓶作为对照组。按gb 4789.2-2016测定菌落总数。在无菌操作下称取1g样品,用10ml生理盐水稀释,取0.1ml涂布pca平板,37℃培养2d,观察并计数。结果发现,不辐照时,产品平均含菌量达2.25
×
104cfu/g;用500gy辐照处理后,产品平均含菌量为200cfu/g,与对照组比明显减少,但灭菌不彻底;分别用1000gy和2000gy辐照处理后,产品均呈无菌状态。每组从样品瓶的上、下层共抽取6份样品,按gb 23200.115-2018检测氟虫腈砜含量。对辐照组与对照组的测定值进行组间t检验,p值均大于0.05,说明上述剂量辐照对鸡蛋粉中氟虫腈砜的量值无显著影响。但是,2000gy处理可能对鸡蛋粉的营养品质有影响,因为该剂量辐照后产品的黄色变浅,而且略微散发出一种臭鸡蛋味道。因此,优先选择辐照剂量为1000gy,实测值为959~1009gy,辐照环境温度为22℃,湿度为37%rh。辐照后的产品置于-20℃冰箱长期保存。
[0093]
考虑到真空冷冻干燥至恒重时鸡蛋粉中仍可能存在少量水分,后续加工过程也可能吸潮,本实施例进一步对最终产品的水分进行检测:随机抽取6份真空包装后的鸡蛋粉,采用gb5009.3-2016中的直接干燥法检测。检测得到,鸡蛋粉的平均含水量为1.5%,相对标准偏差rsd值为1.62%。即在相应的状态下,鸡蛋粉呈松散的粉状,真空包装后于-20℃冰箱冷冻保存,鸡蛋粉不会结块,不会影响产品的检测。
[0094]
由于鸡蛋粉在室温下暴露于空气中容易吸潮和受微生物污染,建议产品开启后一次性使用。每瓶产品使用前应恢复至室温。一次称取6份鸡蛋粉测试样(每份1.25g)置于洁净的50ml离心管中,密封后立即置于-20℃冰箱避光保存,分别于0天、3天、7天各取2份样品检测,3次检测的平均值差异较小,6份样品的rsd值小于2%,说明开封后的鸡蛋粉用上述方法保存,一周内检测,量值稳定。
[0095]
1.4检测方法的选择
[0096]
本发明均采用国标法进行样品检测,所述的国标法是在gb23200.115-2018的基础上适当修改后的稳定同位素稀释液相色谱质谱联用法(id-lc-ms/ms)。id-lc-ms/ms很少受到各种物理和化学因素的干扰,可以克服基质效应的影响。它是以同样分子结构的稳定同位素标记的有机化合物为内标,通过对内标和目标物进行同位素丰度的精确质谱测量,转化获得待测样品中目标物的准确含量。在实验过程中,id-lc-ms/ms法测量的不是浓度而是样品中待测物与内标的摩尔数量的比值,因而测量可以直接追溯到基本单位。氟虫腈砜参考物质为国家有证标准物质(gbw(e)084271),由浙江省农业科学院研制生产。同位素内标为氟虫腈砜-13
c6,由上海安谱提供,化学结构式见图3。
[0097]
本实施例对国标法的仪器条件和前处理方式进行了适当优化,结果如下:
[0098]
(1)样品前处理
[0099]
鸡蛋液复原:将产品从冰箱中取出,恢复至室温。准确称取1.25g鸡蛋粉(精确至0.0001g)置于50ml塑料离心管中,准确加入3.75g水,涡旋振荡1min,超声10min,30℃避光水浴1h。
[0100]
提取:准确加入50μl氟虫腈砜-13
c6标准品和20ml乙腈于装有待测鸡蛋液的50ml塑料离心管中,涡旋振荡1min,超声30min。继续加入2g氯化钠和6g无水硫酸钠,涡旋振荡
1min,5000r/min离心5min,上清液待净化。
[0101]
净化:准确吸取2ml上清液于预先装有100mg psa粉末、100mg c
18
粉末和300mg无水硫酸镁的10ml塑料离心管中,涡旋振荡1min,5000r/min离心5min,上清液过0.22μm微孔滤膜,待上机测定。
[0102]
(2)lc-ms/ms检测
[0103]
液相色谱条件:
[0104]
仪器型号:thermo fisher ultimate 3000高效液相色谱仪;
[0105]
色谱柱:ace excel 2c
18
柱(2.1mm
×
100mm,2μm);
[0106]
柱温:35℃;
[0107]
流动相:a相为水,b相为甲醇,梯度洗脱,洗脱程序见表7;
[0108]
流速:0.25ml/min;
[0109]
进样量:5μl。
[0110]
表7流动相梯度洗脱程序
[0111][0112]
质谱条件:
[0113]
仪器型号:thermo fisher tsq quantum discovery三重四极杆质谱仪;
[0114]
扫描方式:负离子扫描(esi
-
);
[0115]
毛细管电压:3 800v;
[0116]
离子源温度:320℃;
[0117]
鞘气:25arb;
[0118]
辅助气:4arb;
[0119]
碰撞气:2mtorr;
[0120]
监测模式:选择反应监测(srm),监测条件见表8。
[0121]
表8被测物及其内标物的质谱信息
[0122][0123]
最终建立的上述检测方法,其准确度、精密度、灵敏度均能满足国标法以及相关标准物质研制需求。
[0124]
实施例2基体标准物质候选物的应用
[0125]
按jjf 1343-2012《标准物质定值的通用原则及统计学原理》的随机数表抽取样品,进行均匀性检验。采用单因素方差分析法(f-检验法),对检测结果进行统计学分析,由p-value﹥0.05,判定该候选物的均匀性良好。
[0126]
按jjf 1343-2012分别考察长期保存的稳定性和短期运输的稳定性。以先密后疏原则在不同时间点抽取样品检测,均采用趋势分析法(t-检验法)对检测结果进行统计学分析,由p-value﹥0.05,判定该候选物的稳定性良好。
[0127]
按jjf 1343-2012,采用上述的稳定同位素稀释液相色谱质谱联用法(id-lc-ms/ms),由6家实验室对该候选物进行联合定值。对每家实验室提供的检测数据分别用狄克逊(dixon)准则检验,检查是否存在界外值。用科克伦法(cochran)检查各组数据之间是否等精度。将6家实验室所测数据的平均值视为单次测量值构成一组新的测量数据,再次用狄克逊准则检验,判断是否存在异常值。采用达戈斯提诺法(d’agostino)检验6家实验室所有检测数据的正态性。经统计学分析,6家实验室提供的所有检测数据均有效,最终获得鸡蛋粉中氟虫腈砜残留分析标准物质的含量标准值为:77μg/kg。
[0128]
按jjf 1343-2012,对均匀性引入的不确定度、稳定性引入的不确定度、联合定值过程引入的不确定度进行统计学分析。数值修约规则按gb8170-2008《数值修约规则与极限数值的表示和判定》和jjf 1059.1-2012《测量不确定度评定与表示》进行。最终获得鸡蛋粉中氟虫腈砜残留分析标准物质的扩展不确定度为:6μg/kg(k=2)。
[0129]
本发明提供的鸡蛋粉中氟虫腈砜残留分析标准物质候选物,均匀性和稳定性均能满足标准物质要求,通过后续的分析获得了标准值和不确定度,由此形成了具有量值溯源性的标准物质产品,可用于鸡蛋中氟虫腈砜检测过程质量监控、分析方法评价以及操作人员水平考核等。
[0130]
以上所述的实施例对本发明的技术方案进行了详细说明,应理解的是以上所述的仅为本发明的具体实施例,并不用于限制本发明,凡在本发明的原则范围内所做的任何修改、补充或类似方式替代等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1