一种黑果枸杞花色苷复合物及调色方法
1.本发明涉及植物提取物的领域,具体涉及一种黑果枸杞花色苷复合物及调色 方法。
背景技术:
2.在植物界,蓝色的花朵和果实极其少见,而蓝色所对应的最大吸收波长较高, 吸收蓝色波长段的光需要大量的共轭发色团,而植物中需要耗费更多的合成步骤 及能量才能完成蓝色素的合成,但蓝色并不能给植物在吸引传粉媒介上带来优势, 因此在植物中很少有蓝色,可食用的蓝色素则更加稀少。
3.食品工业主要依靠两种人工蓝色素制造蓝色糖果、谷物和饮料:亮蓝和靛蓝, 但随着食品安全意识的提高,人们对人造染料对健康的潜在影响以及它们生产的 可持续性提出了质疑。
4.因此,若能利用自然界中的植物提取物得到一种天然的蓝色素,将对食品安 全的保障具有重要意义。
技术实现要素:
5.本发明的目的在于提供一种黑果枸杞花色苷复合物及调色方法,提供的黑果 枸杞花色苷复合物在中性条件下对黑果枸杞花色苷的蓝颜色具有较好的改善作 用,具有潜在的蓝色食品着色剂的使用价值。
6.为了实现上述目的,本发明采用如下方案:
7.本发明提供了一种黑果枸杞花色苷复合物,所述黑果枸杞花色苷复合物是由 黑果枸杞花色苷与羟丙基四氢吡喃三醇、四氢甲基嘧啶羧酸、甘草酸二钾中的任 意一种或几种化合物形成的。
8.本发明还提供了一种黑果枸杞花色苷的调色方法,所述调色方法包括:将所 述黑果枸杞花色苷与羟丙基四氢吡喃三醇、四氢甲基嘧啶羧酸、甘草酸二钾中的 任意一种或几种化合物形成复合物,用于提升黑果枸杞花色苷的蓝色。
9.本发明首先从选取了10种化合物探究其色差影响情况,最终得到3类有助 于花色苷溶液产生蓝色调的化合物:羟丙基四氢吡喃三醇(px)是一种小分子的 木糖类衍生物;四氢甲基嘧啶羧酸(ect)是芳香酸类化合物,具有嘧啶吡咯环 的平面结构;甘草酸二钾(dg)是五环三萜类皂苷类化合物,分子量较大。
10.进一步地,所述黑果枸杞花色苷的浓度为0.2~0.6mg/ml。
11.发明人在实验过程中发现,黑果枸杞花色苷溶液(acns)的浓度对色差有一 定的影响,acns处于0.2~0.6mg/ml的色差与其他浓度范围相比有着显著性差 异,而黑果枸杞花色苷溶液浓度为0.4mg/ml下的色差值相较于0.2mg/ml和 0.6mg/ml更低;因此,在本发明的一个实施方式中,所述黑果枸杞花色苷的浓 度为0.4mg/ml。
12.在0.4mg/ml的acns浓度下,随着化合物的浓度的升高,花色苷趋向于向 蓝色、绿
色的色调移动。
13.进一步地,所述化合物的浓度为0~180mg/ml,更进一步为0~90mg/ml。
14.进一步地,所述复合物的溶液的酸碱性为中性。
15.羟丙基四氢吡喃三醇、四氢甲基嘧啶羧酸、甘草酸二钾的假如可以增强蓝色 区域波长吸光值的表达,进一步地,所述复合物的最大吸收波长为550~570nm。
16.本发明黑果枸杞花色苷复合物在中性条件下对黑果枸杞花色苷的蓝颜色具 有较好的改善作用。
17.所述复合物的制备方法具有如下步骤:
18.a.制备黑果枸杞花色苷溶液,所述黑果枸杞花色苷溶液为的浓度为0.2~0.6 mg/ml;
19.b.添加羟丙基四氢吡喃三醇、四氢甲基嘧啶羧酸、甘草酸二钾中的任意一种 或几种化合物并且混合,以制备所述复合物;
20.所述化合物的浓度为0~180mg/ml;
21.所述复合物的溶液的酸碱性为中性。
22.进一步地,所述黑果枸杞花色苷的浓度为0.4mg/ml;
23.所述混合的时间为0~20min;所述化合物的浓度为0~90mg/ml;黑果枸杞花 色苷溶液的浓度随着反应时间的增加,色差值同样也呈现了先下降后上升的趋势, 黑果枸杞花色苷溶液处于10~30min时的色差与其他反应时间下有着显著性差异, 因20min下的色差值相较于10min和30min更低,因此,本发明的一个实施 例中,混合的时间为20min。
24.进一步地,所述羟丙基四氢吡喃三醇的浓度为0~20mg/ml;
25.进一步地,所述黑果枸杞花色苷溶液与所述化合物的体积比为1:10~10:1。
26.有益效果
27.本发明利用羟丙基四氢吡喃三醇(px)、四氢甲基嘧啶羧酸(ect)或甘草酸 二钾(dg)与黑果枸杞花色苷形成复合物体系,有利于改善黑果枸杞花色苷的颜 色,羟丙基四氢吡喃三醇(px)、四氢甲基嘧啶羧酸(ect)、甘草酸二钾(dg) 三种复合物能使单一的黑果枸杞花色苷颜色向蓝色调发生转移,其中以acns-px 的复合物最接近蓝色;本发明黑果枸杞花色苷复合物可以提升黑果枸杞花色苷的 蓝色,具有潜在的蓝色食品着色剂的使用价值,可用于食品加工及贮藏中。
附图说明
28.图1为化合物3的谱图;
29.图2为花色苷浓度对色差的影响;
30.图3为花色苷反应时间对色差的影响;
31.图4为化合物浓度对花色苷溶液色差影响,a:acns+px;b:acns+ect;c: acns+ntm;d:acns+alt;e:acns+egt;f:acns+α-abt;g:acns+β-abt;h: acns+dg;i:acns+ist;j:acns+crm;
32.图5为羟丙基四氢吡喃三醇浓度对花色苷颜色的影响;
33.图6为四氢甲基嘧啶羧酸浓度对花色苷颜色的影响;
34.图7为甘草酸二钾浓度对花色苷颜色的影响;
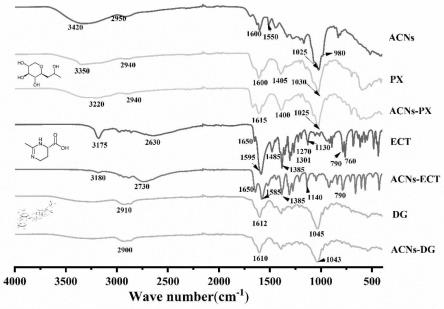
35.图8为花色苷复合物的傅里叶红外光谱;
36.图9为花色苷复合物的吸收波长光谱图;
37.图10为花色苷单体二元复合物的1h核磁共振波谱,a:3-px;b:3-ect;c: 3-dg;
38.图11为花色苷单体二元复合物的原子力扫描显微镜图谱,a:3的三维图; b:3-px的三维图;c:3-ect的三维图;d:3-dg的三维图;e:3的二维图;f: 3-px的二维图;g:3-ect的二维图;h:3-dg的二维图。
39.图2、3中,不同字母代表组间差异显著,p<0.05;相同字母代表组间差异 不显著,p>0.05;
40.图4中,*代表与对照组0mg/ml相比,*p<0.05说明具有统计学意义, **p<0.01说明具有极显著的统计学意义。
具体实施方式
41.下面对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是 本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域 普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于 本发明保护的范围。
42.在本发明的描述中,需要说明的是,除非另有明确的规定和限定,本发明中 的试剂均为常规市售能够得到。
43.实施例1
44.1.材料与试剂
45.本发明所用的黑果枸杞花色苷提取物制备方法为:称取3.0kg黑果枸杞粉 末置于提取桶中,按料液比(1:10,g/ml)加入70%乙醇,静置浸泡5h。微波 萃取仪50℃循环提取1h,收集提取液。使用管式离心机(12000rpm)除去提 取液中的不溶物及杂质,澄清液于旋转蒸发仪50℃真空浓缩除去液体中的乙醇, 收集无醇的黑果枸杞提取液。
46.(2)黑果枸杞花色苷的富集
47.以大孔树脂ab-8作为吸附材料,将无醇的黑果枸杞提取液与树脂进行动态 吸附,吸附后用5倍柱体积的纯水洗脱,以除去多糖、蛋白质。用4倍柱体积的 75%乙醇为流动相对大孔树脂上吸附的色素进行洗脱。洗脱液于旋转蒸发仪50℃ 真空浓缩干燥,得到黑色颗粒状的黑果枸杞花色苷提取物195.8g,并对颗粒状 提取物进行超微粉碎,得到粉末状黑果枸杞花色苷提取物。
48.化合物3的制备:化合物3是黑果枸杞花色苷的主要成分,通过液相色谱制 备得到:
49.(1)样品溶液的配制
50.称取10.0g黑果枸杞花色苷提取物粉末,将提取物超声溶解于100.0ml 的0.1%盐酸-甲醇溶液中,使其终浓度为10.0mg/ml,过0.22μm滤膜后置于 4℃冰箱避光保存。
51.(2)一维色谱条件
52.色谱柱:dac-50动态轴向压缩柱(c18-ods-a,300mm
×
50mm,5μm,ymc), 流动相:a为0.6%三氟乙酸水溶液(v/v),b为乙腈。色谱洗脱条件如下所示, 色谱进样量20.0ml,流速80.0ml/min,色谱柱温30℃,检测波长为280nm。 得到fr1-fr7馏分,如图1-a。
53.(3)化合物3的制备条件
54.色谱柱为xaqua c18(250mm
×
20mm,5μm,acchrom),流动相:a为0.6% 三氟乙酸水溶液(v/v),b为乙腈。等度洗脱条件:17%b,流速18.0,洗脱后得 到化合物3。
55.经过1h nmr和13c nmr结构鉴定,化合物3是 petunidin-3-o-trans-p-coumaroylrutinoside-5-o-glucoside.结构鉴定参考 文献:high-performanceliquid chromatography separation of cis
–
transanthocyanini somers from wild lycium ruthenicum murr.employing amixed-mode reversed-phase/strong anion-exchange stationary phase。
56.化合物3的氢谱如如图1-b所示,碳谱如如图1-c所示。
57.试剂
58.分析纯羟丙基四氢吡喃三醇(pro-xylane,px)、四氢甲基嘧啶羧酸(ectoin, ect)、巯基组氨酸三甲基内盐(ergothioneine,egt)、α-熊果苷(α-arbutin, α-abt)、β-熊果苷(β-arbutin,β-abt)、甘草酸二钾(dipotassiumglycyrrhizinate,dg)、烟酰胺(nicotinamide,ntm)、神经酰胺(ceramide, crm)、尿囊素(allantoin,alt)、肌醇(inositol,ist)购买自西安超邦生物 科技有限公司,色谱级氘代水购买自阿拉丁试剂有限公司,其他试剂均为分析纯。
59.2实验方法
60.2.1储备溶液的配制
61.黑果枸杞花色苷储备溶液的配制:称取2.0g的黑果枸杞花色苷提取物,超 纯水定容至200ml并摇匀至充分溶解,使其终浓度为10.0mg/ml。
62.px储备溶液的配制:称取2.0g的羟丙基四氢吡喃三醇粉末,超纯水定容 至100ml并摇匀至充分溶解,使其终浓度为10mg/ml。
63.ect、egt、α-abt、β-abt、dg、ntm、crm、alt、ist储备溶液的配制: 称取10.0g的化合物粉末,超纯水定容至100ml并摇匀至充分溶解,使其终浓 度为100mg/ml。
64.2.2单因素优化条件
65.花色苷浓度优化实验:将黑果枸杞花色苷储备溶液用超纯水稀释为0.05、 0.10、0.20、0.40、0.60、0.80、1.00、2.00、3.00、4.00mg/ml,避光静置 20min后使用分光测色仪检测色差。
66.花色苷反应时间优化实验:将黑果枸杞花色苷储备溶液用超纯水稀释至 0.40mg/ml,避光静置0、10、20、30、40、50、60、70、80、90min后使用分 光测色仪检测色差。
67.2.3花色苷复合物的颜色改善条件
68.将px储备溶液以0、1、2、3、4、5、6、7、8、9mg/ml的浓度稀释于0.40 mg/ml黑果枸杞花色苷溶液,将ect、egt、α-abt、β-abt、dg、ntm、crm、alt、 ist储备溶液以0、10、20、30、40、50、60、70、80、90mg/ml的浓度稀释于 0.40mg/ml黑果枸杞花色苷溶液,花色苷复合物溶液避光静置20min后使用分 光测色仪检测色差。
69.2.4傅里叶红外分析条件
70.将px储备溶液以12mg/ml的浓度稀释于0.40mg/ml黑果枸杞花色苷溶液, ect、dg储备溶液以120mg/ml的浓度稀释于0.40mg/ml黑果枸杞花色苷溶液, 花色苷复合物冻干后检测,扫描范围4000~500cm-1
,分辨率8cm-1
,共扫描64 次。
71.2.5 1
h核磁共振波谱分析条件
72.分别将px、ect以及dg与前期所制备的化合物3(50μm)以摩尔浓度比 20:1、10:1、5:1、2:1混合并冻干,核磁溶剂为氘代水,复溶后静置20min, 核磁600mhz检测1h波谱。
73.2.6原子力显微镜分析条件
74.分别将px、ect以及dg与前期所制备的化合物3(50μm)以摩尔浓度比 10:1混合并冻干,超纯水复溶后吸取1μl样品置于干净的云母片上,室温下 挥干溶液后上机检测;扫描频率1hz,扫描模式为非接触扫描,对表面粗糙度 以及形貌进行记录。所有实验均在恒温恒湿环境条件下进行(温度25℃,相对 湿度25%),并使用相同的探针进行分析。
75.2.7相互作用力分析条件
76.使用chemdraw对花色苷以及化合物的结构进行构建,并利用chem3d中的 mm2模块对所有结构进行能量最小化以及几何优化。使用molcus对二元复合物 的初始构象进行搜索,并在mopac2016的pm6-dh3半经验量子力学水平上进行优 化;在对最低能量的构象进一步基于b3ylp/6-31g(d)的全电子dft优化,利 用bsse进行校正后对相互作用能进行计算;对二元复合物的共价及非共价作用 研究使用multiwfn(lut,chenf.multiwfn:a multifunctional wavefunctionanalyzer[j].journal of computational chemistry,2012,33(5):580-92.) 的hirshfeld的独立梯度模型(independent gradient model based onhirshfeldpartition,igmh)。
[0077]
igmh分析是可视化研究分子间相互作用的一种常用方法。该分析方法基于 研究系统的电子电荷密度ρ的拓扑学特性,并计算与电荷密度相关的的一阶导 数和二阶导数。分析方法通过整个分子系统与分子间电荷密度的一阶导数之差从 而计算出δg
inter
:
[0078][0079]
δg
inter
大于0则表示弱相互作用的存在,并表示其相互作用的强度。igmh 专注于单独研究分子间和分子内的相互作用,避免了其他研究方法下的相互干扰, 而相互作用区δg函数的值则直接反映了相互作用的强度。
[0080]
2.8数据处理及分析
[0081]
数据使用graphpad prism 8.0(graphpad software inc.,usa)和origin 2018(originlab corporation,usa)进行处理和统计学分析。多组数据之间的 均数比较的相互比较采用单因素方差分析(one-way anova),统计数据以平均值
ꢀ±
标准差(x
±
s)表示,不同字母代表组间差异显著(p<0.05),相同字母代表 组间差异不显著(p>0.05)。*或者#代表p<0.05说明具有统计学意义,**或者 ##代表p<0.01说明具有极显著的统计学意义。
[0082]
3实验结果
[0083]
3.1单因素优化结果分析
[0084]
设置优化的目标颜色为蓝紫色、紫色、紫红色,三种标准色的rgb值分别为 (112,0,144)、(128,0,128)、(144,0,112);通过检测待测样品与三种标 准色之间的色差值变化,确定最接近目标颜色的单因素条件。
[0085]
黑果枸杞花色苷溶液(acns)浓度对色差的影响如图2所示。由图2可知, acns随着浓度的升高,色差值呈现了先下降后上升的趋势,且与三种标准色的 色差值的变化规律基本一致。acns处于0.2~0.6mg/ml的色差与其他浓度范围 有着显著性差异,因0.4mg/ml下的色差值相较于0.2mg/ml和0.6mg/ml更低, 因此选择0.4mg/ml作为acns的改善颜色下的浓度条件。
[0086]
acns反应时间对色差的影响如图3所示。由图3可知,acns随着反应时间 的增加,色差值同样也呈现了先下降后上升的趋势,且三种标准色的色差值的变 化规律也基本一致。此外,acns处于10-30min时的色差与其他反应时间下有 着显著性差异,因20min下的色差值相较于10min和30min更低,如与紫色 相比,20min色差值(43.81
±
0.02)略小于10min(46.17
±
0.04)和30min (44.06
±
0.06),因此我们选择20min作为acns的改善颜色下的反应时间。
[0087]
综上所述,acns的颜色改善条件优化为:提取物浓度0.4mg/ml,反应时间 20min。
[0088]
3.2花色苷复合物颜色的改善
[0089]
确定优化反应条件之后,对acns的颜色做进一步优化。在自然界中,天然 的食用蓝色素资源十分稀缺,仅有栀子蓝、藻蓝蛋白和靛蓝,因此通过二元复合 物使黑果枸杞花色苷呈现蓝色或蓝紫色对其应用具有十分重要的意义。
[0090]
本发明从一些常见辅料中选择了px、ect、egt、α-abt、β-abt、dg、ntm、 crm、alt、ist,并根据黑果枸杞花色苷在中性溶液中的颜色特点,设置目标颜 色oxford blue,rgb值为(0,33,71),lab值为(12.88,5.81,-27.03), 探究化合物的浓度对acns色差的影响。
[0091]
化合物浓度对acns色差影响如图4所示。图e-g和图i-j中,相较于对照 组,色差值并未随着化合物浓度的升高而出现显著的变化,且色差值并未有缩小 的趋势,表明egt、α-abt、β-abt、ist和crm在0-90mg/ml的浓度范围无法 使acns产生蓝色调;图a-d及图h的色差值随着化合物浓度的升高发生显著变 化,其中图a代表的px组、图b代表的ect组以及图c代表的dg组随其浓度的 增加色差值出现了显著的下降,如px组相较于对照组,于90mg/ml浓度时降至 13.10
±
0.15,ect组从0mg/ml的21.19
±
0.18下降至90mg/ml的14.72
±
0.12, dg组相较于对照组的色差值(20.38
±
0.12)最低降至了11.89
±
0.08;0000000 图c代表ntm组,其色差值也随着浓度的上升而下降,但颜色稳定性较差;图d 代表alt组,其色差值出现了先下降在上升的趋势,从对照组浓度的20.38
±
0.03 降至40mg/ml的17.35
±
0.05,但幅度较小,因此烟酰胺和尿囊素也不纳入研 究对象。
[0092]
因此,px、ect以及dg在和acns的复合物可以明显缩小与目标蓝色调的色 差值。
[0093]
本发明进一步探究px、ect以及dg的浓度对acns颜色的影响,并通过lab 颜色空间反映变化。
[0094]
结果如图5~图7所示,在0.4mg/ml的acns浓度下,随着化合物的浓度的 升高,花色苷溶液的颜色在颜色坐标轴上出现了向-a和-b轴移动的现象,这表 明随着化合物浓度的升高,花色苷趋向于向蓝色、绿色的色调移动。
[0095]
从表1可知,随着px浓度的增加,acns-px的lab值均出现一定程度的下 降,亮度l值从31.55
±
1.83持续下降到18mg/ml浓度下的16.61
±
0.73,同 时红绿值a从53.64
±
3.23下降到26.12
±
1.56,黄蓝值b从-35.52
±
1.45下降 至-52.03
±
1.32,结果表明随着浓度的提升,颜色朝绿色和蓝色靠近,亮度降低。
[0096]
从表2可知,ect对acns颜色参数的影响,140mg/ml浓度下的亮度值降至 最低20.84
±
1.32。随着ect浓度增加,其黄蓝值下降加剧,这导致了花色苷对 蓝色的表达增加。
[0097]
从表3可知,化合物dg对acns颜色参数的影响,20mg/ml的dg即可提升 溶液的亮度值l,从空白组29.88
±
2.14到47.36
±
3.91,随着化合物浓度的提 高而降低,浓度的增加对黄蓝值b影响不大,随着浓度的增加,红绿值a从 37.57
±
2.16减少至30.21
±
0.02,dg浓度
的增加对提高了acns亮度,并使红 绿值减少。
[0098]
综上所述,px能显著影响花色苷的各项比色参数,使颜色向深蓝色靠近且 和浓度相关;ect浓度的增加可以减少花色苷的亮度和黄蓝值;而低浓度下的dg 即可发生颜色的改变并随着浓度的增加减小亮度值。
[0099]
表1羟丙基四氢吡喃三醇浓度对花色苷比色参数的影响
[0100][0101]
注:不同字母代表组间差异显著,p<0.05;相同字母代表组间差异不显著,p>0.05。
[0102]
表2四氢甲基嘧啶羧酸浓度对花色苷比色参数的影响
[0103][0104]
注:不同字母代表组间差异显著,p<0.05;相同字母代表组间差异不显著,p>0.05。
[0105]
表3甘草酸二钾浓度对花色苷比色参数的影响
[0106][0107][0108]
注:不同字母代表组间差异显著,p<0.05;相同字母代表组间差异不显著,p>0.05。
[0109]
3.3花色苷复合物的红外光谱分析
[0110]
acns、acns-px、acns-ect、acns-dg的红外光谱如图8所示。由图8可知, acns在3420cm-1
处有o-h拉伸振动,2950cm-1
处有c-h拉伸振动,1600cm-1
处的频带与c-o伸缩振动有关,1550cm-1
处的频带归属于芳香烃骨架的c-c伸 缩振动,1025cm-1
和980cm-1
归属于c-o-c的芳香环的弹性振动,这些都是典型 的黄酮类化合物的红外光谱特征。在与px、ect和dg复合后,复合物的红外光 谱相比acns发生了一定的变化,如acns-px复合物的o-h伸缩振动峰从3420cm ‑1、3350cm-1
进一步降低到了3220cm-1
,表明acns与px间形成了分子间的氢键。 此外acns-ect和acns-dg光谱中的1715~1000cm-1
波段的峰强度减小,且复合 物在1100~1000cm-1
波段的峰均发生了较小的偏移,如ect谱图中1130cm-1
的 c-o伸缩振动在acns-ect上偏移到了1140cm-1
,结果说明化合物的羧基与花色 苷的羟基之间存在一定的相互作用。红外光谱分析结果表明,acns与px、ect、 dg的复合之间存在着氢键的相互作用,这些作用在一定程度上改变了花色苷的 光谱学性质。
[0111]
进一步探究acns与px、ect、dg的复合后的波长,结果见图9、表4。
[0112]
表4 acns复合物的波长
[0113][0114]
由图9及表4可以看出,加入px后显著提高了花青素的吸光强度以及蓝色 光谱区域的积分面积,而此区域强度对应光谱的蓝色。此外ect、dg的加入也能 增强蓝色区域波长吸光值的表达。
[0115]
3.4花色苷复合物的1h核磁共振波谱分析
[0116]1h nmr化学位移可以用来描述原子核的周围环境,而原子核周围电子环境的 变
化会对h原子核产生屏蔽或去屏蔽效应,反映到核磁共振波谱上,即h原子的 电子云强度的减小或增大与它在向低场(去屏蔽效应)或高场(屏蔽效应)位移 变化相关。
[0117]
以黑果枸杞花色苷中的主成分化合物3为研究对象,探究化合物浓度对花色 苷的1h核磁波谱影响。3及其复合物的核磁共振波谱分析如图10所示,前面对 3的核磁共振波谱归属表明6-9ppm化学位移内为该化合物的母环和香豆酰基结 构,3的化学位移(6-9ppm)随着化合物浓度的升高而向高场移动,这表明这 些化合物与3之间存在相互作用,进而通过疏水的π-π相互作用力对母环和酰 基上的h原子周边的电子云环境造成屏蔽效。
[0118]
同时我们注意到,随着化合物浓度的提高,化合物的特征化学位移也在向低 场位移,如3-px中,9.09(s)、8.83(d,j=5.8hz)、8.77(dd,j=8.1hz) 以及8.02(dd,j=8.2,5.8hz)分别位移到了8.85(d,j=2.5hz)、8.62(dd, j=5.0,1.8hz)、8.20-8.15(m)和7.52(dd,j=7.9,4.9hz),说明px的h 原子化学位移向低场移动的这一行为,受到了复合物之间相互作用的影响。综上 所述,复合物内存在相互作用力,继而引起了h原子化学位移的改变,花色苷h 原子发生去屏蔽效应,化合物h原子发生屏蔽效应。
[0119]
3.5花色苷复合物的原子力显微镜分析
[0120]
原子力显微镜是能通过测量探针和原子之间相互作用力,从而对微观结构和 表面形态做出表征的一类技术。原子力显微镜的扫描结果如图11所示,其表面 高度如表5所示。图11-a和11-e为化合物3,其表面高度为0.92
±
0.11nm, 在添加px后,表面结构更为均一且高度显著增加至2.13
±
0.14nm,这表明分 子聚合增加,构象升高;在添加ect、dg后,其表面高度分别为1.23
±
0.17nm 和1.42
±
0.04nm,较对照组相比表面高度均有显著增高;表明化合物与花色苷 发生分子间的聚集,但结构不均一。结果说明px、ect和dg均能与花色苷分子 相互结合,产生分子间的作用力。
[0121]
表面粗糙度在研究生物分子相互作用中起着重要作用,原子力扫描显微镜的 粗糙度结果表5所示。3表面相对均匀,平均粗糙度(ra)和均方根粗糙度(rq) 值分别为0.148
±
0.001nm和0.204
±
0.003nm。在3中加入px后,3-px组的 粗糙度参数ra和rq分别增加至0.382
±
0.046nm和0.502
±
0.072nm,相较于其 他两组复合物粗糙度最高;在加入ect后,ra仍维持与3相同的数值,而rq略微 增加到了0.238
±
0.019nm;3-dg粗糙度较3有明显提升,ra和rq值分别为 0.176
±
0.013nm和0.271
±
0.022nm。有研究表明,表面粗糙度的增加原因是 3和化合物分子相互作用,可能发生链的聚集,形成更多的凸起和褶皱从而使粗 糙度增加。
[0122]
表5花色苷单体二元复合物的表面高度和粗糙度
[0123][0124]
注:不同字母代表组间差异显著,p<0.05;相同字母代表组间差异不显著,p>0.05。
[0125]
综上,本发明利用色差法评价了10种不同浓度的辅料对黑果枸杞花色苷溶 液
(acns)颜色的改善效果,从中得到羟丙基四氢吡喃三醇(px)、四氢甲基嘧 啶羧酸(ect)、甘草酸二钾(dg)三种能使acns颜色向蓝色调发生转移的化合 物,其中以acns-px的复合物最接近蓝色。
[0126]
浓度实验发现,px能显著影响acns各项比色参数,使颜色向深蓝色靠近且 和浓度相关;ect浓度的增加可以减少acns的亮度和黄蓝值;而低浓度下的dg 即可发生颜色的改变并随着浓度的增加减小亮度值。
[0127]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言, 可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变 化、修改、替换和变型,本发明的保护范围由所附权利要求及其等同物限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1