1.本发明属于化学医药领域,具体涉及一种预防和/或治疗癌症的药物组合物及其制备方法和用途。
背景技术:2.骨髓来源的抑制细胞(mdscs)是在包括癌症在内的各种病理状况下产生的异质细胞群,是免疫反应的主要调节类群之一。它们具有免疫抑制功能,主要特征是其抑制免疫反应的能力,包括由t细胞、b细胞和自然杀伤(natural killer,nk)细胞介导的免疫反应,几乎所有的肿瘤内mdscs均显示出强大的免疫抑制能力,从而促进肿瘤的发展和转移性扩散。在临床上,mdscs可能是潜在的预后生物标志物,较高的mdscs浸润率与实体瘤患者的总体生存率和无进展生存期有一定的相关性,同时mdscs也是新的治疗策略的潜在靶点。在mdscs向肿瘤的迁移和浸润过程中趋化因子受体cxcr1和cxcr2及其配体趋化因子cxcl1和cxcl2扮演了重要的角色,肿瘤细胞分泌cxcl1和cxcl2,通过cxcr1和cxcr2信号传导调节mdscs,可以增加mdscs对肿瘤组织的浸润,并且降低免疫治疗的效果或产生对免疫治疗药物的耐药。因此使用抗体中和或化合物抑制这些趋化因子的作用可减少肿瘤对mdscs的招募,进而减少mdscs在肿瘤微环境中发挥的免疫抑制作用。
3.有报道信号转导子和转录激活子1(stat1)在cxcl1和cxcl2转录过程中起到了重要作用,丝氨酸磷酸化的stat1可与cxcl1和cxcl2基因的启动子结合促进其表达;同时mdscs的病理激活是由肿瘤基质细胞产生的炎性细胞因子和与损伤相关的分子模式介导的,stat1也是该过程中一个主要的调节因子。因此抑制stat1磷酸化有望抑制cxcl1、cxcl2表达以及抑制mdscs的病理激活,从而治疗癌症。
4.丝裂原活化蛋白激酶(mapks)是将细胞外刺激转化为多种细胞反应信号的重要组成部分。p38 mapk是mapk家族的成员之一,会受环境和遗传毒性胁迫激活,在炎症和组织稳态中发挥关键作用,控制细胞增殖、分化、迁移和凋亡,而肿瘤细胞可以破坏这些通路来促进其增殖、生长和侵袭。p38mapk可调控下游众多的靶基因来实现复杂的生物功能,转录因子stat1为其中之一,p38激酶可以促进stat1的磷酸化,进而调节细胞功能。因此p38激酶抑制剂可以实现抑制stat1的磷酸化的功效。
5.近几十年来小分子激酶抑制剂的开发一直是一个极具潜力的研究领域,发展速度较快。帕纳替尼(ponatinib)是一种第三代酪氨酸激酶抑制剂,受众主要为对其他bcr-ab1激酶抑制剂有原发性或获得性耐药性的病人,2012年在美国注册,已在30多个国家批准用于难治性慢性髓性白血病(cml)和费城染色体阳性急性淋巴细胞白血病(ph+all)等疾病。但目前对于激酶的研究主要是基于酪氨酸激酶间及其在肿瘤中的作用展开的,针对小分子激酶抑制剂对肿瘤微环境的作用以及对肿瘤免疫方面影响的相关研究相对较少,而扩展和发现小分子激酶抑制剂治疗肿瘤的新机制不仅有利于其在肿瘤治疗方面潜力最大程度的挖掘,也有利于其向其他疾病治疗领域的突破,充分扩大其临床应用。
6.此外,小分子激酶抑制剂和免疫检查点抑制剂都存在长期服用产生耐药性的情
况。解决耐药性问题也有重要意义。
技术实现要素:7.本发明的目的是提供一种预防和/或治疗癌症的药物组合物及其制备方法和用途。
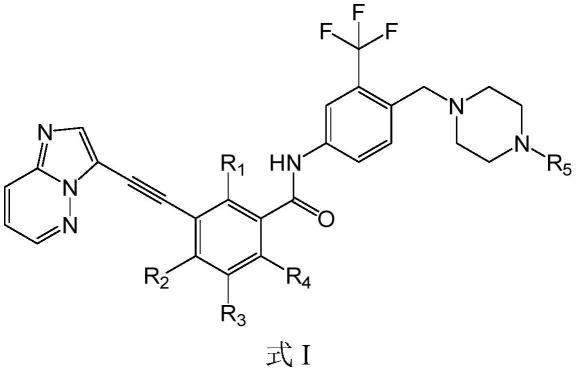
8.本发明提供了式i所示的化合物、或其盐、或其异构体在制备p38激酶抑制剂中的用途:
[0009][0010]
其中,
[0011]
r1、r2、r3、r4、r5分别独立选自氢、c1~c6烷基。
[0012]
进一步地,所述化合物为帕纳替尼,其结构如下:
[0013][0014]
进一步地,所述p38激酶抑制剂为预防和/或治疗癌症,和/或抑制肿瘤细胞增殖、生长、迁移、转移、浸润、侵袭的药物;
[0015]
优选地,所述癌症为结肠癌、乳腺癌、肺癌、肝癌、白血病、肾癌、前列腺癌、胰腺癌、淋巴癌、胃癌。
[0016]
进一步地,所述p38激酶抑制剂为抑制mdscs迁移、浸润的药物。
[0017]
进一步地,所述p38激酶抑制剂为抑制肿瘤细胞p38 mapk信号通路及下游基因表达的药物;
[0018]
优选地,所述药物为抑制stat1磷酸化的药物;
[0019]
和/或,所述药物为抑制cxcl1、cxcl2基因表达的药物;
[0020]
更优选地,所述药物为抑制stat1 ser727位点磷酸化的药物。
[0021]
本发明还提供了一种预防和/或治疗癌症的药物组合物,它是由前述的化合物、或
其盐、或其异构体和肿瘤免疫治疗药物组成。
[0022]
进一步地,所述肿瘤免疫治疗药物为阻断pd-1/pd-l1免疫检查点的阻断剂;
[0023]
优选地,所述阻断pd-1/pd-l1免疫检查点的阻断剂为抗pd-1抗体和/或抗pd-l1抗体;
[0024]
更优选地,所述阻断pd-1/pd-l1免疫检查点的阻断剂为派姆单抗、纳武单抗、阿特朱单抗、巴文西亚单抗、德瓦鲁单抗中的一种或多种。
[0025]
进一步地,前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物的重量比为2:1~400:1;
[0026]
优选地,前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物的重量比为200:1~400:1或3:1~6:1。
[0027]
本发明还提供了一种前述的药物组合物的制备方法,它包括如下步骤:按照重量比取前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物,混合,即可。
[0028]
本发明还提供了前述的药物组合物在制备p38激酶抑制剂中的用途;
[0029]
优选地,所述p38激酶抑制剂为预防和/或治疗癌症,和/或抑制肿瘤细胞增殖、生长、迁移、转移、浸润、侵袭的药物;
[0030]
更优选地,所述癌症为结肠癌、乳腺癌、肺癌、肝癌、白血病、肾癌、前列腺癌、胰腺癌、淋巴癌、胃癌。
[0031]
进一步地,所述p38激酶抑制剂为抑制mdscs迁移、浸润的药物。
[0032]
进一步地,所述p38激酶抑制剂为抑制肿瘤细胞p38 mapk信号通路及下游基因表达的药物;
[0033]
优选地,所述药物为抑制stat1磷酸化的药物;
[0034]
和/或,所述药物为抑制cxcl1、cxcl2基因表达的药物;
[0035]
更优选地,所述药物为抑制stat1 ser727位点磷酸化的药物。
[0036]
本发明还提供了一种预防和/或治疗癌症的药物制剂,它是由前述的药物组合物为活性成分,加上药学上可接受的辅料或者辅助性成分制备而成的制剂。
[0037]
本发明还提供了一种预防和/或治疗癌症的联合用药物,它含有相同或者不同规格的同时或者分别给药的前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物,以及药学上可接受的载体。
[0038]
进一步地,所述肿瘤免疫治疗药物为阻断pd-1/pd-l1免疫检查点的阻断剂;
[0039]
优选地,所述阻断pd-1/pd-l1免疫检查点的阻断剂为抗pd-1抗体和/或抗pd-l1抗体;
[0040]
更优选地,所述阻断pd-1/pd-l1免疫检查点的阻断剂为派姆单抗、纳武单抗、阿特朱单抗、巴文西亚单抗、德瓦鲁单抗中的一种或多种。
[0041]
进一步地,前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物的重量比为2:1~400:1;
[0042]
优选地,前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物的重量比为200:1~400:1或3:1~6:1。
[0043]
本发明还提供了前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物联用在制备p38激酶抑制剂中的用途;
[0044]
优选地,所述p38激酶抑制剂为预防和/或治疗癌症,和/或抑制肿瘤细胞增殖、生长、迁移、转移、浸润、侵袭的药物;
[0045]
更优选地,所述癌症为结肠癌、乳腺癌、肺癌、肝癌、白血病、肾癌、前列腺癌、胰腺癌、淋巴癌、胃癌。
[0046]
进一步地,所述p38激酶抑制剂为抑制mdscs迁移、浸润的药物。
[0047]
进一步地,所述p38激酶抑制剂为抑制肿瘤细胞p38 mapk信号通路及下游基因表达的药物;
[0048]
优选地,所述药物为抑制stat1磷酸化的药物;
[0049]
和/或,所述药物为抑制cxcl1、cxcl2基因表达的药物;
[0050]
更优选地,所述药物为抑制stat1 ser727位点磷酸化的药物。
[0051]
进一步地,所述肿瘤免疫治疗药物为阻断pd-1/pd-l1免疫检查点的阻断剂;
[0052]
优选地,所述阻断pd-1/pd-l1免疫检查点的阻断剂为抗pd-1抗体和/或抗pd-l1抗体;
[0053]
更优选地,所述阻断pd-1/pd-l1免疫检查点的阻断剂为派姆单抗、纳武单抗、阿特朱单抗、巴文西亚单抗、德瓦鲁单抗中的一种或多种。
[0054]
进一步地,前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物的重量比为2:1~400:1;
[0055]
优选地,前述的化合物、或其盐、或其异构体和肿瘤免疫治疗药物的重量比为200:1~400:1或3:1~6:1。
[0056]
本发明研究发现帕纳替尼能够在细胞水平上与p38α激酶相互作用,降低p38α激酶活性,进而抑制其对下游stat1的磷酸化过程,显著降低stat1的磷酸化水平,从而降低p-stat1对cxcl1和cxcl2基因表达的促进,降低肿瘤细胞表达cxcl1和cxcl2,减少了mdscs向肿瘤部位的迁移和浸润,减弱其对肿瘤微环境的免疫抑制作用,最终抑制肿瘤细胞生长和迁移,发挥预防或治疗癌症的功效。此外,帕纳替尼与阻断pd-1/pd-l1免疫检查点的抗体药联合使用具有优异的效果,对于抗肿瘤有协同增效的作用,具有良好的应用前景。
[0057]
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
[0058]
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
[0059]
图1为帕纳替尼体外抑制p38α激酶活性的结果。
[0060]
图2为帕纳替尼抑制mda-mb-231细胞和4t1细胞中stat1 ser727位点的磷酸化水平的结果:a为mda-mb-231细胞;b为4t1细胞。
[0061]
图3为ponatinib对各细胞中趋化因子cxcl1和cxcl2的mrna水平的影响:a为mda-mb-231细胞中的趋化因子cxcl1;b为mda-mb-231细胞中的趋化因子cxcl2;c为4t1细胞中的趋化因子cxcl1;d为4t1细胞中的趋化因子cxcl2;e为mc38细胞中的趋化因子cxcl1;f为mc38细胞中的趋化因子cxcl2。
[0062]
图4为ponatinib对mdscs的迁移的影响结果。
[0063]
图5为ponatinib对mdscs浸润肿瘤组织的影响结果。
[0064]
图6为ponatinib联合抗pd-l1抗体的抗肿瘤效果。
具体实施方式
[0065]
本发明具体实施方式中使用的原料、设备均为已知产品,通过购买市售产品获得。
[0066]
实施例1、帕纳替尼(ponatinib)对p38α酶活性的抑制作用
[0067]
1、实验方法
[0068]
采用p38 alpha kinase enzyme system(promega,#v9591)试剂盒,根据说明书检测帕纳替尼(ponatinib)对p38α酶活性的抑制作用,具体方法如下:
[0069]
(1)96孔板中,在25μl反应缓冲液中加入40ng p38α、1μg底物、1
×
buffer a、50μm atp和50μm dtt,空白组不加入p38α,实验组加入相应浓度ponatinib(以dmso作为溶剂,等ponatinib体积dmso作为对照),室温反应1h。每组三个生物学平行。
[0070]
(2)加入25μl adp-glo试剂,室温反应40min。
[0071]
(3)加入50μl激酶检测试剂,室温反应30min。
[0072]
(4)使用cytation 5细胞成像多模式读板仪检测化学发光读值。
[0073]
(5)以dmso作为对照,通过计算得到p38α激酶活性随着ponatinib浓度变化的曲线。
[0074]
2、实验结果
[0075]
如图1所示,p38α激酶活性随着ponatinib浓度升高而降低,ic50为61.42nm。
[0076]
3、实验结论
[0077]
帕纳替尼(ponatinib)可抑制p38α激酶活性。
[0078]
实施例2、western blot检测ponatinib对stat1磷酸化的抑制作用
[0079]
1、实验方法
[0080]
(1)制备蛋白样品:总蛋白提取,将1μm ponatinib或等体积dmso对照处理24h的乳腺癌细胞系mda-mb-231和4t1样品使用胰酶消化,离心收集细胞,使用pbs洗涤一次,加入适量ripa裂解液,冰上裂解30min,4℃、12000g离心20分钟。收集上清液至新的1.5ml离心管中,即为蛋白样品。
[0081]
(2)蛋白浓度测定:利用bca法进行蛋白浓度测定。制备bsa梯度浓度标准液及工作液。将1μl蛋白溶液加入至20μl工作液中,37℃孵箱中孵育30min。使用nanodrop2000测定标准溶液与待测溶液od值。x轴为bsa标准蛋白浓度(mg/ml),y轴为各标准管对应的od562值。绘制标准曲线。利用标准曲线计算得出待测样品的蛋白浓度。
[0082]
(3)用于电泳上样的蛋白样品的制备:取适量体积的蛋白样品,加入其四分之一体积的5
×
上样缓冲液,涡旋震荡后95℃高温变性5-10min。放入-80℃冰箱保存备用。
[0083]
(4)样品经8%sds-page胶电泳后,转膜至pvdf膜上,5%bsa溶液室温封闭1h。
[0084]
(5)4℃摇床一抗孵育过夜。
[0085]
(6)洗涤:去除封闭液并使用pbst洗涤5次,每次5min。
[0086]
(7)二抗室温摇晃孵育1h。
[0087]
(8)洗涤:去除封闭液并使用pbst洗涤5次,每次5min。
[0088]
(9)ecl发光检测:将ecl发光液的a液与b液等体积混合。将条带放在发光液中稍孵育。使用tanon凝胶成像仪成像。使用image j处理成像条带。
[0089]
2、实验结果
[0090]
如图2所示,加药24h后,ponatinib可显著抑制乳腺癌细胞系mda-mb-231和4t1中stat1 ser727位点的磷酸化水平,但是对stat1tyr701位点无明显抑制作用。
[0091]
3、实验结论
[0092]
ponatinib可显著抑制stat1 ser727位点的磷酸化水平。
[0093]
实施例3、ponatinib对肿瘤分泌cxcl1和cxcl2的抑制作用
[0094]
1、实验方法
[0095]
采用乳腺癌细胞系mda-mb-231和4t1,以及结直肠癌细胞系mc38作为实验用细胞。
[0096]
(1)提前一天铺细胞于6孔板中,待细胞密度长到70%左右,加入稀释好浓度的ponatinib,以等体积dmso作为对照,每个药物浓度选择3个生物平行。
[0097]
(2)孵育24h后将细胞去除培养基加上trizol裂解液提取rna。
[0098]
(3)通过rt-qpcr方法检测cxcl1和cxcl2的表达量,以gapdh作为内参。
[0099]
2、实验结果
[0100]
如图3所示,ponatinib在乳腺癌细胞系mda-mb-231和4t1,以及结直肠癌细胞系mc38中均能降低cxcl1和cxcl2的mrna水平。且cxcl1和cxcl2的mrna水平随着ponatinib的浓度升高而降低。
[0101]
3、实验结论
[0102]
ponatinib可显著抑制cxcl1和cxcl2的基因表达。
[0103]
实施例4、ponatinib对mdscs的迁移的影响
[0104]
1、实验方法
[0105]
mdscs的体外迁移实验是通过transwell可通透的小室来完成的,具体操作步骤如下:
[0106]
(1)条件性培养基的收集:提前一天在10cm培养皿中铺上4t1细胞,待细胞密度生长至70%左右,添加1μm ponatinib或等体积dmso对照,48h后,收集细胞上清液并进行过滤。
[0107]
(2)通过美天旎磁珠分选试剂盒(miltenyi biotec,#130-094-538)体外分离纯化得到小鼠骨髓来源的抑制性细胞(mdscs,经流式分析纯度》90%),细胞计数,按106细胞/ml浓度稀释到rpmi1640培养基中。
[0108]
(3)将提前收集过滤的条件性培养基,即步骤(1)得到的细胞上清液,每孔600μl体积加入到transwell下室中。
[0109]
(4)小心在transwell上室中加入100μl稀释的mdscs。
[0110]
(5)37℃细胞培养箱孵育6h。
[0111]
(6)小心去除transwell上室,收集下室的培养基,按等体积流式上机计数,计算可得mdscs迁移到下室的数量。
[0112]
2、实验结果
[0113]
如图4所示,ponatinib处理的4t1细胞上清液招募的mdscs数量明显减少。
[0114]
3、实验结论
[0115]
ponatinib可显著抑制mdscs的迁移。
[0116]
实施例5、ponatinib对mdscs浸润肿瘤组织的影响
[0117]
1、实验方法
[0118]
将4t1细胞使用胰酶消化,并用pbs洗涤两次,无血清rpmi1640培养基重悬,细胞计数,将4t1细胞稀释到1.25
×
106细胞/ml的浓度,使用胰岛素针向balb/c野生型小鼠第四对乳房垫注射4t1细胞悬液40μl。一周后每周两次监测小鼠肿瘤体积,待瘤体增长到100-200mm3后随即分组并进行给药处理。给药时间为每周灌胃ponatinib或溶剂对照4天,每天给药30mg/kg,连续给药3周。ponatinib的溶剂对照是25mm ph2.75的柠檬酸盐溶液(nc)。肿瘤体积按最长边乘以最短边的平方的一半计算得到。给药3周后将小鼠安乐死并解剖取出肿瘤,加肿瘤解离试剂研磨成单细胞悬液,经过70μm细胞网筛过滤,4℃,300g离心10min,去除上清。再使用40%percoll重悬,2000rpm室温离心20min,去除上清。之后冰上裂解细胞10min,加入预冷的pbs洗涤一次,4℃,300g离心10min。弃上清,使用预冷的pbs洗涤一次,并用细胞计数仪计数,将肿瘤单细胞悬液稀释到107/ml的浓度。取100μl,4℃,400g离心5min。小心去除上清,加入50μl的fcr封闭抗体4度封闭10min。将所需用到的流式抗体依次根据合适比例稀释到50μl/样品的pbs流式染色溶液中。4℃避光孵育40-60min。加入预冷的pbs洗涤一次,4℃,400g离心5min。去除上清,使用预冷的pbs重悬细胞,并用40μm细胞网筛过滤。将过滤好的细胞悬液进行流式上机分析染色结果。使用flowjo v10分析数据。
[0119]
2、实验结果
[0120]
如图5所示,ponatinib给药组小鼠肿瘤内mdscs比例明显低于对照组。
[0121]
3、实验结论
[0122]
ponatinib可显著抑制肿瘤内mdscs的浸润。
[0123]
实施例6、ponatinib与抗pd-l1抗体联用对肿瘤组织的影响
[0124]
1、实验方法
[0125]
将4t1细胞使用胰酶消化,并用pbs洗涤两次,无血清rpmi1640培养基重悬,细胞计数,将4t1细胞稀释到1.25
×
106细胞/ml的浓度,使用胰岛素针向balb/c野生型小鼠第四对乳房垫注射4t1细胞悬液40μl。一周后每周两次监测小鼠肿瘤体积,待瘤体增长到100-200mm3后随即分组并进行给药处理。给药时间为每周灌胃ponatinib或等体积溶剂对照(25mm ph2.75的柠檬酸盐溶液)4天,每天给药30mg/kg,部分小鼠给药ponatinib的同时,每周腹腔注射小鼠抗pd-l1抗体(购买自bioxcell公司)两次,每次200μg/只,连续给药2周。
[0126]
实验共分为4各组:(1)nc组:只灌胃溶剂对照,并注射抗igg抗体,抗igg抗体是抗pd-l1抗体的同型对照,在nc组注射抗igg抗体是为了排除其他非抗pd-l1因素对肿瘤生长的影响;(2)anti-pd-l1组:只注射小鼠抗pd-l1抗体;(3)ponatinib组:只灌胃给药ponatinib;(4)ponatinib+anti-pd-l1组:不仅灌胃给药ponatinib,并注射抗pd-l1抗体。
[0127]
2、实验结果
[0128]
结果如图6所示,ponatinib与抗pd-l1抗体联合使用,可显著抑制肿瘤的生长,抑制效果明显优于单独使用ponatinib或抗pd-l1抗体。说明与单独使用ponatinib或抗pd-l1抗体相比,ponatinib与抗pd-l1抗体联用发挥了协同增效作用。本发明ponatinib与抗pd-l1抗体联合使用时单剂量给药的质量比为3:1。
[0129]
3、实验结论
[0130]
ponatinib与抗pd-l1抗体联合用药对于抗肿瘤、抑制肿瘤生长具有协同增效作用。
[0131]
综上,本发明研究发现帕纳替尼能够在细胞水平上与p38α激酶相互作用,降低p38α激酶活性,进而抑制其对下游stat1的磷酸化过程,显著降低stat1的磷酸化水平,从而降低p-stat1对cxcl1和cxcl2基因表达的促进,降低肿瘤细胞表达cxcl1和cxcl2,减少了mdscs向肿瘤部位的迁移和浸润,减弱其对肿瘤微环境的免疫抑制作用,最终抑制肿瘤细胞生长和迁移,发挥预防或治疗癌症的功效。此外,帕纳替尼与阻断pd-1/pd-l1免疫检查点的抗体药联合使用具有优异的效果,对于抗肿瘤有协同增效的作用,具有良好的应用前景。
