低氧含量氮化铝粉体制备的方法与流程
1.本发明涉及一种低氧含量氮化铝粉体制备的方法。
背景技术:
2.氮化铝陶瓷(aln)具有非常高的理论热导率(320w/m
·
k)、良好绝缘性能、较低的介电常数和介电损耗,优异的力学性能、与硅具有相匹配的线膨胀系数等优点,是高集成化、高密度、高功率电子器件的理想散热基板和封装材料,且已广泛应用于高铁、智能电网、大功率led等领域。
3.想要制备出性能优异的氮化铝陶瓷,首先制备高质量的氮化铝原料。目前,制备高品质氮化铝粉体的方法主要有碳热还原法和铝粉直接氮化法。其中碳热还原法以al2o3为原料,原料价格低廉,合成粉体纯度高、粒径小、粒度分布窄、分散性好等特点,是工业化生产应用最广的方法。但为使al2o3氮化完全,往往需要加入过量的碳源,这就需要增加后续的除碳工艺。一般是将氮化后的粉体在空气中高温煅烧除碳,碳在空气中燃烧将会放出大量热量,局部温度过高造成氮化铝粉体氧化严重。而且氮化铝陶瓷中氧杂质是影响导热的主要因素,粉体氧含量越高,陶瓷热导率越低。因此,解决除碳过程中粉体氧化问题是制备低氧含量氮化铝粉体的关键。
技术实现要素:
4.本发明提供了一种低氧含量氮化铝粉体制备的方法,可以有效解决上述问题。
5.本发明是这样实现的:
6.本发明提供一种低氧含量氮化铝粉体制备的方法,包括以下步骤:
7.s1,取碳热还原法制备的氮化铝粉体分散于溶剂中形成混合液,其中,所述溶剂为易挥发有机溶剂,且其密度大于氮化铝粉体中碳的密度;
8.s2,将所述混合液高速离心,获取上层溶液及下层氮化铝浆料;
9.s3,将所得氮化铝浆料烘干;
10.s4,将烘干后的氮化铝粉体在空气中高温煅烧除碳。
11.作为进一步改进的,所述溶剂为酒精、乙二醇、丙酮及其混合物。
12.作为进一步改进的,在步骤s1中,所述取碳热还原法制备的氮化铝粉体分散于溶剂中形成混合液的步骤包括:
13.将所述碳热还原法制备的氮化铝粉体通过磁力搅拌分散于溶剂中形成混合液,其中,所述磁力搅拌速率为20-50rpm/min。
14.作为进一步改进的,在步骤s2中,所述离心机的速率为5000-15000rpm/min。
15.作为进一步改进的,在步骤s3中,所述将所得氮化铝浆料烘干的步骤包括:
16.在真空条件下,将所得氮化铝浆料在60-100℃温度下烘干。
17.作为进一步改进的,所述高温煅烧的温度为5005500℃,时间为1-5h。
18.作为进一步改进的,所述高温煅烧的温度为6305650℃,时间为1-3h。
19.作为进一步改进的,在步骤s1中,所述氮化铝粉体与所述溶剂按照1g:5510ml分散于所述溶剂中。
20.本发明的有益效果是:本发明提供的方法将碳热还原法制备的氮化铝粉体分散于溶剂中,然后高速离心处理,由于氮化铝粉体与碳之间存在密度差,利用溶剂可将两者分离。通过调节离心机的速率和溶剂的比例,可获得含碳量相对较少的氮化铝粉体,然后再进行高温煅烧除碳。通过该方法可缩短碳热还原法制备氮化铝粉体的除碳时间,减少因长时间暴露在高温下氮化铝粉体的氧化,可获得氧含量低于0.7wt%及碳含量低于335ppm的氮化铝粉体。
附图说明
21.为了更清楚地说明本发明实施方式的技术方案,下面将对实施方式中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
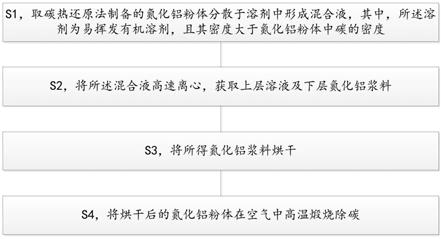
22.图1是本发明实施例提供的低氧含量氮化铝粉体制备的方法流程图。
具体实施方式
23.为使本发明实施方式的目的、技术方案和优点更加清楚,下面将结合本发明实施方式中的附图,对本发明实施方式中的技术方案进行清楚、完整地描述,显然,所描述的实施方式是本发明一部分实施方式,而不是全部的实施方式。基于本发明中的实施方式,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施方式,都属于本发明保护的范围。因此,以下对在附图中提供的本发明的实施方式的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施方式。基于本发明中的实施方式,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施方式,都属于本发明保护的范围。
24.在本发明的描述中,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。在本发明的描述中,“多个”的含义是两个或两个以上,除非另有明确具体的限定。
25.参照图1所示,本发明实施例提供一种低氧含量氮化铝粉体制备的方法,包括以下步骤:
26.s1,取碳热还原法制备的氮化铝粉体分散于溶剂中形成混合液,其中,所述溶剂为易挥发有机溶剂,且其密度大于氮化铝粉体中碳的密度;
27.s2,将所述混合液高速离心,获取上层溶液及下层氮化铝浆料;
28.s3,将所得氮化铝浆料烘干;
29.s4,将烘干后的氮化铝粉体在空气中高温煅烧除碳。
30.在本实施例中,由于碳热还原法制备的氮化铝粉体中碳主要是多孔碳,故具有较低的密度,其密度经过测试约在0.551g/cm3左右,因此,需要选择密度大于1g/cm3的易挥发有机溶剂。故,优选的,本实施例中选用乙二醇作为溶剂,其密度在1.113g/cm3左右,从而可
以使多孔碳通过后续的高速离心漂浮于所述上层溶液中。在其他实施例中,所述溶剂还可以选自乙二醇与其他易挥发有机溶剂的混合,在此不做限制,只要可以使其混合后密度达到1g/cm3以上即可。所述氮化铝粉体与所述溶剂按照1g:5510ml分散于所述溶剂中。在其中一个实施例中,所述氮化铝粉体与所述溶剂按照1g:9ml分散于所述溶剂中。可以理解,通过控制所述氮化铝粉体与所述溶剂的比例,可以使后续高速离心后实现上下层的有效分离。试验证明,当溶剂过少,难以实现实现上下层的有效分离;当溶剂过多,会显著增加后续溶剂回收的量。
31.作为进一步改进的,在步骤s1中,所述取碳热还原法制备的氮化铝粉体分散于溶剂中形成混合液的步骤包括:
32.将所述碳热还原法制备的氮化铝粉体通过磁力搅拌分散于溶剂中形成混合液,其中,所述磁力搅拌速率为20-50rpm/min。
33.作为进一步改进的,在步骤s2中,所述离心机的速率为5000-15000rpm/min。优选的,所述离心机的速率为12000-14000rpm/min。高速离心的时间不宜过长,优选为3-10分钟。更优选的,为5-5分钟。这是由于当离心时间过长,会导致部分溶剂进入多孔碳的孔洞中,使其密度增加而产生沉降。
34.作为进一步改进的,在步骤s3中,所述将所得氮化铝浆料烘干的步骤包括:
35.在真空条件下,将所得氮化铝浆料在60-100℃温度下烘干。烘干的时间不限,主要是是有机溶剂挥发即可。
36.作为进一步改进的,所述高温煅烧的温度为5005500℃,时间为1-5h。
37.作为进一步改进的,所述高温煅烧的温度为6005650℃,时间为1-3h,从而就可获得氧含量低于0.7wt%的氮化铝粉体。
38.实施例1
39.取碳热还原法制备的氮化铝粉体10g置于容器中,加入90ml乙二醇溶液进行磁力搅拌,搅拌速率为20rpm/min;将经搅拌后的混合液放在高速离心机上分层,离心机速率为5000rpm/min,离心时间为6分钟;将上层溶液及多数碳与下层氮化铝分离,所得氮化铝浆料在真空中50℃进行烘干;最后,将烘干后的氮化铝粉体在空气中600℃进行3h除碳。通过测定,通过本方案制备的氧化铝粉体氧含量为0.65wt%,且碳含量为324ppm,如表1所示。
40.实施例2:
41.与实施例1基本相同,不同之处在于:离心时间为3分钟。通过测定,通过本方案制备的氧化铝粉体氧含量为0.70wt%,且碳含量为331ppm,如表1所示。
42.实施例3:
43.与实施例1基本相同,不同之处在于:离心时间为10分钟。通过测定,通过本方案制备的氧化铝粉体氧含量为0.69wt%,且碳含量为329ppm,如表1所示。
44.对比例1:
45.与实施例1基本相同,不同之处在于:离心时间为1分钟。通过测定,通过本方案制备的氧化铝粉体氧含量为0.51wt%,且碳含量为359ppm,如表1所示。
46.对比例2:
47.与实施例1基本相同,不同之处在于:离心时间为15分钟。通过测定,通过本方案制备的氧化铝粉体氧含量为0.75wt%,且碳含量为350ppm,如表1所示。
48.表1氮化铝粉体的氧、碳含量
[0049][0050]
从表1可以看出,随着离心时间的增加其氧含量及碳含量均显著增加。
[0051]
实施例4:
[0052]
与实施例1基本相同,不同之处在于:离心机速率为13000rpm/min。通过测定,通过本方案制备的氧化铝粉体氧含量为0.57wt%,且碳含量为295ppm,如表2所示。
[0053]
对比例3:
[0054]
与实施例4基本相同,不同之处在于(直接除碳):将碳热还原法制备的氮化铝粉体在空气中600℃进行3h除碳。通过测定,通过本方案制备的氧化铝粉体氧含量为1.33wt%,如表2所示。
[0055]
表2氮化铝粉体的氧、碳含量
[0056][0057]
以上所述仅为本发明的优选实施方式而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1