一种维拉卡肽的合成方法与流程
本发明涉及生物多肽制药技术领域,特别涉及几种通过简单高效的在液相中的氧化方法形成分子间二硫键来制备多肽的方法。
技术背景
维拉卡肽,英文名velcalcetide、etelcalcetide、amg416,其化学结构式如式i所示。
velcalcetide是一种新颖的拟钙剂(calcimimeticagent),该药通过静脉给药,开发用于正接受血液透析治疗的慢性肾脏病(ckd)患者。amg416结合并激活对甲状旁腺上的钙敏感受体,从而导致实现甲状旁腺激素(pth)水平的降低。在有效治疗继发性甲状旁腺功能亢进症的新型药物方面显示了广阔的前景。
fda批准新型拟钙剂velcalcetide用于血液透析成年患者继发性甲状旁腺功能亢进的治疗,是12年来首个获批用于治疗透析患者继发性甲状旁腺功能亢进的药物。中重度甲状旁腺功能亢进血液透析患者接受velcalcetide治疗后,pth水平显著降低。而且velcalcetide的疗效优于安慰剂、不低于西那卡塞。由于之前深圳翰宇药业报道(cn105504012a)中使用fmoc-l-cys(npys)-oh、boc-l-cys(npys)-oh、h-l-cys(npys)-oh等特殊的保护型氨基酸,由于其本身成本昂贵,在固相树脂上形成二硫键的方式存在用量过大、不易控制等不利因素,故本发明采用了价格低廉的h-l-cys-oh作为最后形成分子间二硫键的合成原料,采取几种简单的在液相中的氧化方法得到纯度较高的维拉卡肽粗肽溶液。不仅反应是在均相中完成,而且用量上得到了大大的减少与控制。考虑到可能存在的二硫键错配的因素,于是在实验过程中通过hplc监测是否有二聚产物,通过hplc图谱显示出二聚物的含量可忽略不计,不影响最终产物的高收率。因此,这种在液相中氧化形成分子间二硫键的方法大大降低了企业生产成本,对于制备维拉卡肽的工业化生产具有应用前景和可观的经济实用价值。
技术实现要素:
本发明主要是将从固相树脂依次偶联得到的多肽主链切割下来之后,与h-l-cys-oh采用hplc实时监测、环保温和、价格低廉的在液相中氧化形成velcalcetide反应液,经过后续的纯化方法得到固体纯品velcalcetide,方法操作简单,得到的产品纯度高,收率高。有利于企业的大规模生产与应用。
为实现上述目的,本发明采取了以下技术方案:
本发明提供了一种维拉卡肽的合成制备方法,包括以下步骤:
步骤1:按维拉卡肽的序列,取fmoc-d-arg-oh与树脂偶联制得fmoc-d-arg-树脂;
步骤2:在fmoc-d-arg-树脂的载体上,依次从碳端向氮端逐一偶联ala、arg、arg、arg、ala、cys(x)后,将cys(x)的氮端乙酰化后制备得到维拉卡肽主链的线性肽树脂,其中cys的侧链保护基团是trt或mmt、stbu,arg的侧链保护基是cbz、boc、pbf;
步骤3:将步骤2中合成得维拉卡肽主链肽树脂切割下来并脱除cys(x)中的侧链保护基x后,经过冰无水乙醚沉降后得到纯度较高的维拉卡肽主链肽;
具体的,本发明提供的多肽合成制备方法中,维拉卡肽主链肽树脂结构式ii为
其中z为侧链保护基团(trt或mmt、stbu)
具体的,本发明提供的多肽合成制备方法中,维拉卡肽主链肽结构式iii为
步骤4是将步骤3中得到的固体维拉卡肽主链肽与h-l-cys-oh采用在液相中氧化,方法有:dmso氧化方法、h2o2氧化方法,形成分子间二硫键,整个氧化反应可以通过hplc实时监测二硫键形成的反应程度,以便控制反应的进行,同时通过hplc监测情况反映几乎不存在分子间错配、二聚物的产生情况。得到纯度较高,收率较高的velcalcetide反应液,进一步经过分离纯化方法,冻干得到固体纯品维拉卡肽。
其中,上述步骤1中的fmoc-d-arg-树脂为从上海吉尔生化公司购置的fmoc-d-arg(pbf)-oh和rinkamideresin,但是所选的氨基树脂还可以包括rinkamide-mbharesin或者rinkamide-amresin。
步骤1中fmoc-d-arg-树脂的替代度为0.2mmol/g-1.0mmol/g,作为优选fmoc-d-arg-树脂的替代度为0.4mmol/g-0.6mmol/g。
步骤2中的cys(x),作为优选,选择fmoc-d-cys(trt)-oh,同样是从上海吉尔生化公司购置。作为优选,保护氨基酸与fmoc-d-arg-树脂的用量比为(1.5-1.8)∶1。采用hobt/dic作为偶联试剂,用量优选(1g∶1.2ml)。脱fmoc试剂:哌啶∶dmf=1∶4(v∶v)。封闭试剂:优选吡啶∶乙酸酐=1∶1.1(v∶v),封闭时间8-12h。氮端乙酰化,作为优选,n-甲基吗啉∶乙酸酐=1∶1(v∶v),乙酰化时间为1.5-2.5h。
步骤3中的裂解试剂优选,92∶3∶2∶2∶1的tfa/phsme/edt/tis/h2o,裂解试剂的用量∶肽树脂的用量=(10-15∶1)(ml∶g)。裂解时间优选2.5h-3h。优选裂解液∶沉降试剂=(1∶10)(v∶v),其中沉降试剂为冰无水乙醚/石油醚或冰无水乙醚/环己烷、甲基叔丁基醚,优选冰无水乙醚/石油醚,更优选冰无水乙醚。
本技术发明中,步骤4采用了h-l-cys-oh这一无任何侧链保护基团的氨基酸作为原料,与之前报道使用fmoc-l-cys(npys)-oh、boc-l-cys(npys)-oh、h-l-cys(npys)-oh作为原料,大大降低了生产成本,解决了用量可控的问题。而且采用在液相中氧化方法有:碘氧化、空气氧化、dmso氧化、h2o2氧化,优选5%dmso溶液和30%h2o2水溶液的氧化条件。反应通过hplc实时监测二硫键形成情况,清洁快速,操作方便,节约成本,对企业大规模生产具有可观的参考价值。
维拉卡肽粗肽经过半制备型高效液相色谱仪分离纯化后,经过冻干即可获得固体维拉卡肽纯品。
此外,本发明中涉及到与多肽合成制备相关的氨基酸和试剂的缩写或英文、中文名称如下:
缩写或英文中文名称
dicn,n’-二异丙基碳二酰亚胺
hobt1-羟基苯并三氮唑
tfa三氟乙酸
phsme甲基苯基硫醚
edt1,2-乙二硫醇
tis三异丙基硅烷
dmf二甲基甲酰胺
dcm二氯甲烷
h2o2双氧水
dmso二甲基亚砜
trt三苯甲基
pbf(2,3-二氢-2,2,4,6,7-五甲基苯并呋喃-5-基)磺酰基
mmt4-甲氧基三苯甲基
stbu叔丁巯基
phenol苯酚
anisole苯甲醚
fmoc9-芴甲氧羰基
d右旋体(相对构型,多用于糖类和氨基酸)
l左旋体(相对构型,多用于糖类和氨基酸)
h时间单位/小时
说明书附图
图1所示为维拉卡肽主链粗肽的质谱;
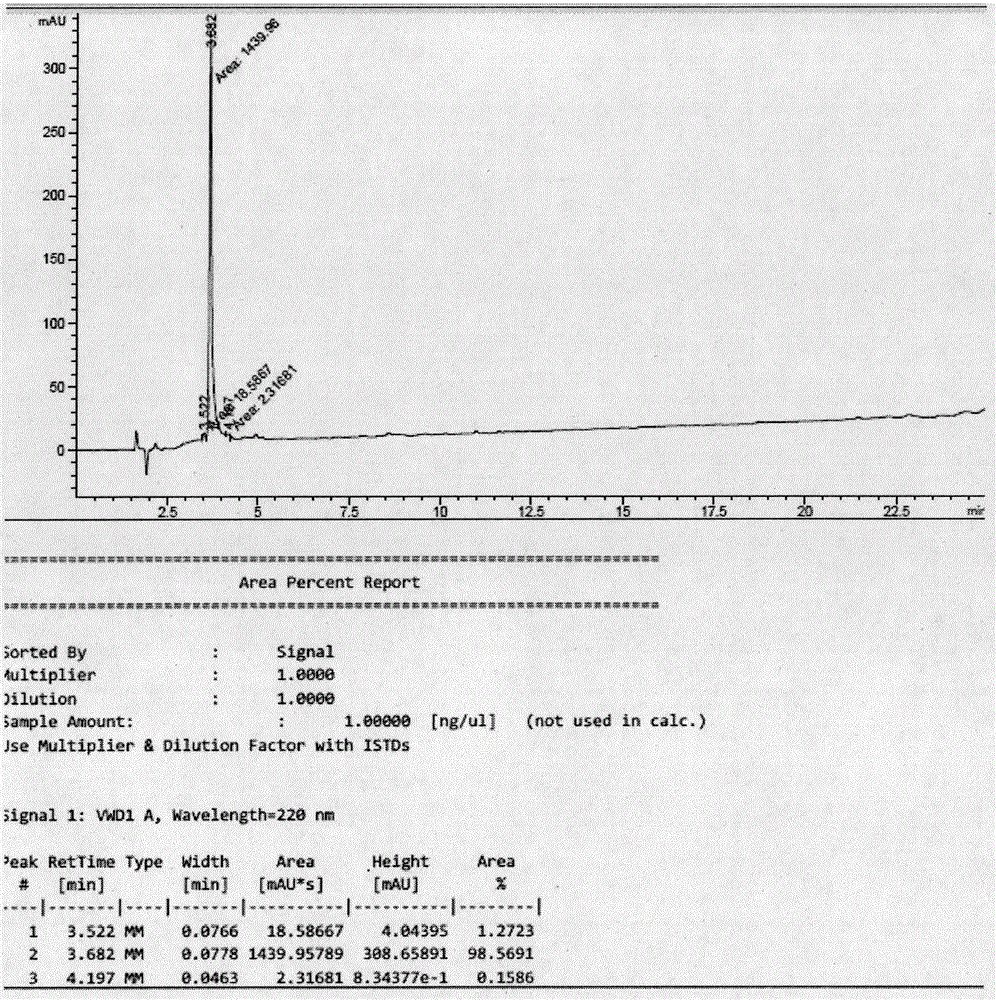
图2所示为冻干后维拉卡肽纯品hplc图谱;
图3所示为冻干后维拉卡肽纯品质谱。
具体实施方法
本发明公开了一种多肽的合成与制备方法,以下实例用于代表性的说明本发明,由于本发明涉及的相关反应条件的各项具体参数体现在实施例中,因此本领域的技术人员在不脱离本发明内容的基础上适当调整工艺方式均可以实现和应用。说明书中给出的各反应条件均能实现本发明。
实施例1
称取替代度0.728mmol/g的rinkamideresin10g加入到固相反应器中,用dmf洗涤2次,dcm溶胀树脂20min。抽干溶剂,加入哌啶∶dmf=1∶4(v∶v)到反应器中,空气鼓泡,采用(5+15min)反应时间体系,充分脱除fmoc后,抽干溶剂,然后用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次。依次称取9.5gfmoc-d-arg(pbf)-oh(14.6mmol)、2.37ghobt(17.5mmol)、2.73mldic(17.5mmol)溶于dmf中活化5min后加入到固相反应器中,将摇床温度调节到室温25℃,充分震荡反应30min。取出反应器,抽滤掉反应液,用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次后。加入60ml(25ml吡啶+25ml乙酸酐+10mldmf)封闭8h。抽滤掉封闭液,用dmf、dcm、dmf、甲醇依次清洗树脂2、1、1、3次,抽干,得到fmoc-d-arg-nh2-树脂。用常规固相替代度测定方法检测到替代度为0.428mmol/g。
以实施例1中0.428mmol/g的fmoc-d-arg-nh2-树脂为原料来合成维拉卡肽主链肽树脂。将抽干得到的12.5g0.428mmol/g的fmoc-d-arg-nh2-树脂加入固相反应器中,用dmf洗涤2次,用dcm溶胀树脂20min,加入哌啶∶dmf=1∶4(v∶v)到反应器反应中,空气鼓泡,采用(5+15min)反应时间体系,充分脱除fmoc后,抽干溶剂,然后用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次。称取3.3g(10.7mmol)fmoc-d-ala-oh、1.73g(12.8mmol)hobt、1.9ml(12.8mmol)dic加入到dmf中预先活化5min后加入到固相反应器中,放入摇床中震荡反应,室温下反应2h,取出固相反应器,抽滤掉反应液,然后用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次。根据标准的多肽固相合成方法,依次偶联剩余的fmoc-d-ala-oh、fmoc-d-arg(pbf)-oh、fmoc-d-arg(pbf)-oh、fmoc-d-arg(pbf)-oh、fmoc-d-ala-oh、fmoc-d-cys(trt)-oh。用茚检试剂来判断偶联反应终点情况:包含溶液a、b、c。其中,溶液a为:5%茚三酮无水乙醇溶液;溶液b:80%苯酚无水乙醇溶液;溶液c:0.01mol/lkcn重蒸吡啶溶液。茚检时,每个溶液各取2滴。当树脂显透明无色表示偶联完全反应结束,如果树脂显色则说明偶联不完全,需要进行补投相应的氨基酸、缩合试剂继续反应直到树脂无色透明。
上述过程偶联到最后一个fmoc-d-cys(trt)-oh后,用上述方法脱除fmoc保护后,氮端乙酰化,选择n-甲基吗啉∶乙酸酐=1∶1(v∶v),乙酰化时间为2.5h。抽干,用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次,甲醇抽干后,称重,得到维拉卡肽主链肽树脂24.3g。
向制备得到的维拉卡肽主链肽树脂中加入体积比为92∶3∶2∶2∶1的tfa/phsme/edt/tis/h2o,裂解试剂的用量∶肽树脂的用量=(10-15∶1)(ml∶g)。常温下反应3h。抽滤,用tfa洗涤树脂以保证多肽残留量降到最低,旋蒸出tfa,收集滤液,加入到沉降试剂中,静置10min后用离心机分离出白色固体,收集,室温真空干燥,收集得到7.5g固体,此为维拉卡肽主链粗肽。
用沉降出的维拉卡肽主链粗肽溶解在纯水中,加入一定量的30%h2o2水溶液和h-l-cys-oh,通过hplc监测,反应1h可完全转化成维拉卡肽粗肽溶液。
将得到的维拉卡肽粗肽溶液,经过滤膜过滤不溶性杂质后,采用半制备型高效液相色谱仪器分离,纯化,波长220nm,层析柱填料:sinochromods-bp
尺寸:10.0mm*200mm。流动相是水和乙腈,以梯度洗脱方式,收集目标多肽的吸收峰组分,合并后,旋蒸出绝大部分的乙腈后,冻干机冻干,获得固体维拉卡肽纯品。
实施例2
称取替代度0.728mmol/g的rinkamideresin10g加入到固相反应器中,用dmf洗涤2次,dcm溶胀树脂20min。抽干溶剂,加入哌啶∶dmf=1∶4(v∶v)到反应器中,空气鼓泡,采用(5+15min)反应时间体系,充分脱除fmoc后,抽干溶剂,然后用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次。依次称取9.5gfmoc-d-arg(pbf)-oh(14.6mmol)、2.37ghobt(17.5mmol)、2.73mldic(17.5mmol)溶于dmf中活化5min后加入到固相反应器中,将摇床温度调节到室温25℃,充分震荡反应45min。取出反应器,抽滤掉反应液,用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次后。加入60ml(25ml吡啶+25ml乙酸酐+10mldmf)封闭8h。抽滤掉封闭液,用dmf、dcm、dmf、甲醇依次清洗树脂2、1、1、3次,抽干,得到fmoc-d-arg-nh2-树脂。用常规固相替代度测定方法检测到替代度为0.588mmol/g。
以实施例2中0.588mmol/g的fmoc-d-arg-nh2-树脂为原料来合成维拉卡肽主链肽树脂。将抽干得到的14.2g0.588mmol/g的fmoc-d-arg-nh2-树脂加入固相反应器中,用dmf洗涤2次,用dcm溶胀树脂20min,加入哌啶∶dmf=1∶4(v∶v)到反应器反应中,空气鼓泡,采用(5+15min)反应时间体系,充分脱除fmoc后,抽干溶剂,然后用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次。称取5.19g(16.7mmol)fmoc-d-ala-oh、2.7g(20mmol)hobt、3.1ml(20mmol)dic加入到dmf中预先活化5min后加入到固相反应器中,放入摇床中震荡反应,室温下反应2h,取出固相反应器,抽滤掉反应液,然后用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次。根据标准的多肽固相合成方法,依次偶联剩余的fmoc-d-ala-oh、fmoc-d-arg(pbf)-oh、fmoc-d-arg(pbf)-oh、fmoc-d-arg(pbf)-oh、fmoc-d-ala-oh、fmoc-d-cys(trt)-oh。用茚检试剂来判断偶联反应终点情况:包含溶液a、b、c。其中,溶液a为:5%茚三酮无水乙醇溶液;溶液b:80%苯酚无水乙醇溶液;溶液c:0.01mol/lkcn重蒸吡啶溶液。茚检时,每个溶液各取2滴。当树脂显透明无色表示偶联完全反应结束,如果树脂显色则说明偶联不完全,需要进行补投相应的氨基酸、缩合试剂继续反应直到树脂无色透明。
上述过程偶联到最后一个fmoc-d-cys(trt)-oh后,用上述方法脱除fmoc保护后,氮端乙酰化,选择n-甲基吗啉∶乙酸酐=1∶1(v∶v),乙酰化时间为2.5h。抽干,用dmf、甲醇、dcm、dmf依次清洗树脂2、1、1、1次,甲醇抽干后,称重,得到维拉卡肽主链肽树脂34.8g。
向制备得到的维拉卡肽主链肽树脂中加入体积比为92∶3∶2∶2∶1的tfa/phsme/edt/tis/h2o,裂解试剂的用量∶肽树脂的用量=(10-15∶1)(ml∶g)。常温下反应3h。抽滤,用tfa洗涤树脂以保证多肽残留量降到最低,旋蒸出tfa,收集滤液,加入到沉降试剂中,静置10min后用离心机分离出白色固体,收集,室温真空干燥,收集得到16.3g固体,此为维拉卡肽主链粗肽。
用沉降出的维拉卡肽主链粗肽溶解在纯水中,加入一定量5%dmso溶液,和h-l-cys-oh,通过hplc监测,反应2h可完全转化成维拉卡肽粗肽溶液。
将得到的维拉卡肽粗肽溶液,经过滤膜过滤不溶性杂质后,采用半制备型高效液相色谱仪器分离,纯化,波长220nm,层析柱填料:sinochromods-bp
尺寸:10.0mm*200mm。流动相是水和乙腈,以梯度洗脱方式,收集目标多肽的吸收峰组分,合并后,旋蒸出绝大部分的乙腈后,冻干机冻干,获得固体维拉卡肽纯品。
- 还没有人留言评论。精彩留言会获得点赞!