烟草低温早花相关基因NtDUF599及其应用的制作方法
本发明属于烟草基因工程技术领域,具体涉及一个与烟草低温早花相关的ntduf599基因及其应用的专利申请。
背景技术:
烟草(nicotianatabacuml.)是一种喜温不耐寒的叶用经济作物,在烟叶生长过程中时常会发生早花现象。烟草早花指烟草植株未能达到正常栽培条件下所具有的高度和叶数就加速完成发育进程而导致提前现蕾、开花的异常现象。发生早花的烟株过早地从营养生长转入生殖生长,导致烟株生长势弱、叶数少、叶片小而薄、株形小,烟叶的质量和产量严重下降。
国内外烟草生产均存在较为普遍的早花现象。温度、光周期、不当的栽培管理技术及其他一些因素都对对烟草早花的形成产生影响。以温度为例,温度骤降且持续十天以上是引起烟株早花的主要原因,在此过程中,烟草会发生从叶片分化向发芽分化的转换,从而导致早花。因此,为了避免早花的发生,应做好以下几点:选择合适的烟草品种进行栽培、培育壮苗、选择合适时期移栽、有效施肥、做好防寒防旱等措施。
在所有的环境因子中,低温是引起烟草早花的主要原因。有报道显示少叶型品种在营养生长期遭受11-13℃低温时会促进花芽分化,20℃以上温度则抑制花芽发育而促进营养生长。另外,促进花芽分化最适宜的温度为13-18℃。文家仁的研究发现,烟株4叶期之前遇到低温不会出现早花现象;5片真叶时期遭遇低温,早花率达到33%左右;7-8片真叶遇到低温的早花率高达75-100%。韩锦峰等人的研究显示k326对低温敏感时期出现在6片真叶,当处理到7片真叶期时才会稳定低温的诱导作用,且不发生逆转。金磊的研究发现烟株在45-73d的苗龄范围进行12-18℃低温诱导时,温度越低,苗龄越小,早花现象越明显。苏亮等研究了不同叶龄与低温持续时间对烟草花芽分化的影响,发现6叶期吉烟9号遭低温后早花程度最高。综上所述,低温诱导烟草早花应建立在一定的条件基础上,其中诱导时间、温度范围及烟草品种均与早花的形成关系密切。
目前在烟草栽培生产中应对低温早花问题主要是通过农艺措施(如移栽、打顶留杈等)来解决低温胁迫诱导花芽提前分化的问题,但这是比较耗费人力的补救措施。而随着分子生物学技术发展和烟草基因工程开展,利用基因工程手段来改良烟草抵御低温早花在理论和技术上都是一定可行的。但总体上,现有关于烟草低温早花的分子机制研究还停留在较初步的阶段,相关功能基因研究的仍然较为有限。
总之,通过分子生物学层面研究,同时结合相关生理学研究成果,筛选并鉴定烟草低温早花相关基因,并利用基因工程手段改良现有烟草主栽品种,对于培育出耐低温抗早花的烟草新品种具有重要的理论和现实意义。
技术实现要素:
本发明目的在于提供一个与烟草低温早花相关基因ntduf599,从而为烟草及其他植物的抗低温早花分子育种以及优化开花时期基因工程育种培育提供新的策略和路径。
本申请所采取的技术方案详述如下。
烟草低温早花相关基因ntduf599,包括711bp碱基,其碱基序列如seqidno.1所示。
所述烟草低温早花相关基因ntduf599在花期调控中的应用,利用基因沉默技术、或者基因超表达方法,通过调节ntduf599基因表达量,来调节控制逆境条件下的花期,所述逆境条件具体为低温条件。
所述烟草低温早花相关基因ntduf599的pcr扩增制备方法,包括如下步骤:
(1)提取(具体例如以烟草k326叶片为样品)基因组,并反转录为cdna备用;
(2)设计引物用于扩增基因编码区,并进行pcr扩增,具体引物序列设计如下:
f:5'-atggagaaagaaattctgga-3',
r:5'-ctaaactgctactctctctg-3'。
用于沉默所述烟草低温早花相关基因ntduf599的rnai载体,将其命名为:pbwa(v)hs-ntduf599-rnai,通过如下步骤制备获得:
(1)酶切、连接
首先,以ntduf599基因中第121-300位核苷酸作为rnai的引导序列,分别进行正反方向的pcr扩增;
其次,对pbwa(v)hs载体依次采用psti和smai进行单酶切,单酶切后利用infusion连接酶依次将正向和反向rnai引导序列连接到pbwa(v)hs载体;
(2)转化、筛选和鉴定
将步骤(1)中的连接产物转化大肠杆菌dh5α,并进行筛选,挑取阳性克隆质粒进行菌落pcr鉴定和测序鉴定,确保重组构建正确,并将最终构建正确重组干扰表达载体质粒命名为:pbwa(v)hs-ntduf599-rnai。
烟草低温早花相关基因ntduf599所编码蛋白,包括236个氨基酸,氨基酸序列如seqidno.2所示。
所述烟草低温早花相关基因ntduf599所编码蛋白在花期调控中的应用,该蛋白与植物逆境处理条件下开花时间相关,降低该蛋白表达量后,可缩短逆境处理条件下的植物开花时间,或者说,可提前促进植株开花;所述逆境处理条件具体例如为低温胁迫逆境处理。
利用所述烟草低温早花相关基因ntduf599的烟草新品种培育方法,通过转基因技术、瞬时表达技术或基因组编辑技术,构建含有ntduf599基因的病毒诱导沉默载体、rnai干涉载体、超表达载体或基因组编辑载体,转化烟草,筛选获得花期变化的烟草新品种;
具体例如:利用rna干扰沉默技术,干扰ntduf599基因的表达使其沉默,ntduf599基因沉默植株在面临低温胁迫时,筛选获得植株开花时间提前的植物新品种。
换言之,一种培育低温胁迫处理条件早花烟草新品种培育方法,利用rna干扰沉默技术,干扰ntduf599基因的表达使其沉默,ntduf599基因沉默的新烟草品种植株在面临低温胁迫处理时,新品种植株早花现象提前。
基于现有烟草基因工程进展和相关植物表型观察和鉴定,发明人对特定基因ntduf599进行了深入研究,发现其与烟草低温早花现象高度相关。进一步基因功能验证过程中,在将该基因沉默,并对转基因植株进行低温胁迫处理后,转基因植株的开花时间得到了明显提前,表明该基因与植株响应低温胁迫、植株的生殖生长均具有十分密切的关联。而基于此研究结果,可为进一步的烟草新品种培育奠定一定技术基础。
附图说明
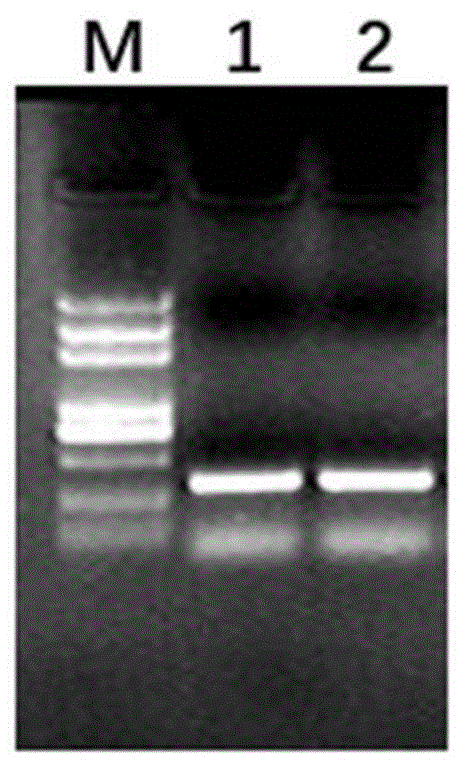
图1ntduf599基因的pcr产物电泳图;m,marker;1,正向序列pcr产物;2,反向序列pcr产物;
图2ntduf599基因植物rnai干扰载体转基因株系基因表达水平;
图3ntduf599-rnai转基因株系与非转基因对照的花期比较。
具体实施方式
下面结合实施例对本申请做进一步解释说明,以使本领域技术人员能够进一步了解本申请的技术方案。
实施例1
本实施例就低温早花相关基因ntduf599的克隆获得过程简要介绍如下。
(一)烟草rna提取及cdna合成
(1)总rna提取
以生长4周左右的烟草k326的幼嫩叶片为样品,经液氮充分研磨成粉状后;
取约100mg粉末状材料置于盛有1.0ml的trizol试剂的1.5ml离心管中,随后加入200μl氯仿,振荡混匀、离心,小心将上层水相转入另一离心管中;
加入500μl异丙醇,沉淀、离心分离出rna,再经75%酒精洗涤,室温微干后,加入适当体积的rnasefree的水,充分溶解;
最后对所提取的总rna经dnasei处理,以便后续cdna制备,dnasei消化处理时,10μ:l反应体系参考如下:
所提取总rna,1μg;
10×reactionbufferwithmgcl2,1μl;
dnasei(rnase-free),1μl(1u);
depc-treatedwater加至10μl;
37℃水浴中放置30min。
(2)cdna合成
在无菌0.2ml离心管中配置模板rna/引物混合液,70℃保温10min后迅速在冰上急冷2min以上,离心数秒钟使模板rna/引物的变性溶液聚集于离心管底部;
所述模板rna/引物混合液(7μl体系),具体为:
步骤(1)中dnasei消化后rna(100ng/μl),1μl;
oligo(dt)primer(50μm),1μl;
rnasefreedh2o,5μl;
在上述离心管中配置反转录反应液后,42℃保温1h;70℃保温15min后冰上冷却,所得即为cdna;
具体反转录反应液体系(10μl)为:
上述模板rna/引物变性溶液,7μl;
5×m-mlvbuffer,2μl;
dntpmixture(各10mm),0.5μl;
rnaseinhibitor(40u/μl),0.25μl;
rtasem-mlv(rnaseh-)(200u/μl),0.25μl。
(3)pcr扩增
首先,设计pcr扩增用引物序列如下:
f:5'-atggagaaagaaattctgga-3',
r:5'-ctaaactgctactctctctg-3'。
随后,以步骤(2)中所制备cdna为模板,进行pcr扩增,50μl扩增体系设计如下:
cdna模板,1μl;
gxlpolymerase,1μl;
5×gxlbuffer,10μl;
dntpmixture(10mm),4μl;
primer-f/r,8μl;
ddh2o,26μl;
pcr反应程序如下表所示:98℃、10sec;55℃、15sec,68℃、30sec,35个循环,72℃延伸5min。
对扩增获得的pcr产物进行1%的琼脂糖凝胶电泳(凝胶电泳结果如图1所示),随后回收pcr扩增产物并纯化后,进行测序。
测序结果表明,本申请克隆所得ntduf599基因,包括711bp碱基,其碱基序列如seqidno.1所示,具体如下:
atggagaaagaaattctggattatgtcttggtaccagtaggattgctatttatggtggcttatcacatatggcttcttaatcgcattcttaaacaccctaatcgtacggttatcggcattaattccattaatcgtcacttctgggttcgtgctatgatggaggactcgtccaagaatggagttctagcagtacaaacgttaaggaacaacataatggcgtcaacccttttagcatctactgctattatgcttagttccctaatcgccgtcttaatgactggcggaagcaaaggtcgttctatcggatttcatgtttacggcgataagagcgatctttgcttatcaattaaattcttctctatattggtatgttttatggttgcatttttgtttaacgtgcaatcaattaggtattatagtcacgctagtatacttattaacgtgccttacaagaagttggattgttcaagacatattgtgacggcggaatatgtagggaggacagtgaatcgaggcagctatttctggtcacttggactgcgcgcattttacttttcgtttcctctatttttgtggatctttggccctattcctatgttcctctgctgtattttccttgtttttatgctttatttcctggatggtagttcggattttgggtgggttgcagcaactgatgtcgacacccacacagagagagtagcagtttag。
对ntduf599基因进行分析后,可知其编码236个氨基酸,氨基酸序列如seqidno.2所示,具体如下:
mekeildyvlvpvgllfmvayhiwllnrilkhpnrtviginsinrhfwvrammedsskngvlavqtlrnnimastllastaimlssliavlmtggskgrsigfhvygdksdlclsikffsilvcfmvaflfnvqsiryyshasilinvpykkldcsrhivtaeyvgrtvnrgsyfwslglrafyfsfplflwifgpipmflcciflvfmlyfldgssdfgwvaatdvdthtervav。
实施例2
在实施例1克隆获得ntduf599基因基础上,为进一步对该基因功能进行验证,发明人进一步构建了rnai载体,本实施例就该载体的构建过程简要说明如下。
(1)酶切、连接
首先,以ntduf599基因中第121-300位核苷酸作为rnai的引导序列,进行正反方向的pcr扩增;具体扩增引物序列设计为:
扩增正向ntduf599基因片段的引物:
ntduf599-f:5'-agaaggttggtgacctgcagaattccattaatcgtcac-3',
ntduf599-r:5'–gagaaaaactagacctgcagagaacgacctttgcttcc-3';
f引物5’端的“agaaggttggtgacctgcag”、r引物5’端的“gagaaaaactagacctgcag”部分序列为载体接头序列;
扩增反向ntduf599基因片段的引物:
ntduf599-f:5'-gatagttacagagcccgggagaacgacctttgcttcc-3';
ntduf599-r:5'–agaaggttggtgagcccgggaattccattaatcgtcac-3'
f引物5’端的“gatagttacagagcccggg”、r引物5’端的“agaaggttggtgagcccggg”部分序列为载体接头序列;
其次,以质粒pbwa(v)hs-rnai作为载体,对pbwa(v)hs载体采用psti单酶切,并分别回收酶切产物;随后利用infusion连接酶对pcr扩增获得的rnai产物与酶切后pbwa(v)hs载体进行连接;10μl连接体系设计如下:
5×infusion连接酶,2μl;
酶切后(psti)的pbwa(v)hs-rnai,2μl;
pcr扩增产物,6μl;
50℃反应15分钟后放冰上2-3分钟,备用。
在将正向片段连接到pbwa(v)hs后,利用smai酶切连接有正向片段的pbwa(v)hs,再将反向序列连接到pbwa(v)hs,连接方法与上述相同。
(2)热激法转化
无菌条件下取步骤(1)中的10μl连接产物加到感受态细胞中,轻轻混匀后冰浴30min;
42℃热激90s,然后将离心管迅速转到冰浴中放置2-3min;
加无抗生素的lb培养基800μl,37℃、120rpm摇床摇振1h左右;
取200μl培养液涂于(在涂菌液之前首先加入x-gal和iptg涂匀)含抗生素50μg/ml的lb固体培养基上,37℃倒置培养12h。
(3)筛选及鉴定
培养过程中,培养基中菌斑会分为蓝色和白色两类,待菌斑长到合适大小时,用灭菌的枪头挑取几个白斑,分别于含有50μg/ml卡那霉素的lb液体培养基中振荡培养12h,然后抽提质粒,进行酶切鉴定,确保重组载体构建正确,对于构建正确的质粒(或者含有质粒的菌株)保存备用。最终对构建正确的重组质粒命名为:pbwa(v)hs-ntduf599-rnai。
实施例3
在实施例2所构建重组质粒基础上,利用农杆菌介导的烟草转化方法,发明人将该重组质粒转化至烟草中,通过表型区别来对ntduf599基因进行实际分析。具体过程简要介绍如下。
(1)冻融法转化农杆菌,并制备转染用菌液
将1μg实施例2所制备pbwa(v)hs-ntduf599-rnai重组载体加入到100μl的eha105农杆菌感受态中,混匀后在冰上静置30min;
随后放入液氮中冷冻5min,从液氮中取出后立即放入37℃水浴锅中水浴5min,再在冰上静置5min;
加入500μl的lb培养液,28℃、震荡条件下恢复培养4h,最后将菌液均匀涂抹于添加有抗生素的固体培养基(50mg/l卡那霉素和50mg/l利福平)上,28℃条件下培养24h左右。
挑取单菌斑于含50mg/l卡那霉素和50mg/l利福平的5mllb液体培养基中,在28℃、200r/min条件下培养过夜,培养至菌液浓度达到od600=1.5左右;
取2ml菌液加入到离心管中,4000r/min离心5min;
去除上清液,吸1ml新的ms液体培养基,重悬农杆菌,4000r/min离心5min,重复此操作一次;
最后,将1ml的ms液体培养基重悬后菌液,加入到40ml的ms的液体培养基中(含40μl、25mg/l的乙酰丁香酮),即为侵染液,放置2h以后用于侵染。
(2)叶盘法转化
(a)将无菌的烟草k326种子播种于ms培养基上进行培养,待烟草苗长至3-5cm时(约20-30d),取顶芽放于ms+ba0.2mg/l(壮芽,使其快速成长)培养基上,进行继代培养;
(b)继代培养14天后(有小叶片即可),取大小1cm×1cm左右叶片,切去叶柄,叶片表面及叶边缘划伤后,放入ms+ba1.0mg/l(ph6.0-6.5)的预培养培养基上,正面朝下紧贴培养基放置,于黑暗条件下预培养2d;
(c)取出步骤(b)中预培养的叶片,放入农杆菌侵染液中进行侵染15min,取出后,用灭过菌的干燥滤纸上吸干菌液;
(d)将浸染后叶片放回到预培养基上,28℃黑暗条件下共培养2-3天,至叶片切口周围有微菌斑形成;
再次取出共培养的烟草叶片,用添加500mg/lcef的无菌水冲洗,以洗去外植体表面的农杆菌;
(e)用滤纸吸干步骤(d)中表面液体后,转移到烟草诱芽培养基上(ms+ba1.0mg/l+hyg25mg/l+cef500mg/lph5.8);
培养过程中,每2周更换1次培养基,直至长出不定芽(一般情况为2周);
切下再生的小苗(1cm左右),转入继代培养基(ms+ba0.2mg/l+hyg25mg/l+cef500mg/l,ph5.8)培养;
生长至至小苗长至2cm长时(有小芽即可),转接入生根培养基(ms+naa0.2mg/l)上,25℃、12h光照,培养3周左右,确保长出粗壮根系;
(g)待根生长至2~3cm、苗高7~10cm左右时,移出三角瓶洗去根部培养基,移栽于花盆中,温室培养。
(3)转基因株系鉴定
提取步骤(2)中烟草幼苗的基因组dna,设计引物,利用pcr方法进行kan抗性鉴定,具体引物序列设计如下:
kan-f:5’-tctggacgaagagcatcagg-3’,
kan-r:5’-atgaatccagaaaagcggcc-3’。
鉴定结果表明,共得到kan阳性抗性植株20株。
进一步地,利用实时定量pcr方法,对转基因植株中的ntduf59基因表达量进行分析,具体qrt-pcr分析时,引物序列设计如下:
qntduf599-f:5’-tgaatcgaggcagctatttctg-3’;
qntduf599-r:5’-agggccaaagatccacaaaa-3’;
分析过程,内参基因引物设计为:
26s-f:5’-gaagaaggtcccaagggttc-3’;
26s-r:5’-tctccctttaacaccaacgg-3’。
部分检测结果如图2所示。从图2可以看出,不同转基因株系中ntduf599基因表达量都得到了不同程度的沉默。为便于观察和研究,选取表达量最低的两个转基因株系(rnai-4和rnai-9)作为后续低温早花表型的研究对象。
将野生型烟草k326植株和2个rnai干扰转基因株系(rnai-4和rnai-9)转基因烟草种子均匀播于含营养土的小盆中,置于光照培养室中培养。待幼苗长至4-6叶期,12℃低温处理10天,同时设置在正常温度下生长的烟株为对照。
低温处理10天后移至正常温度(25℃)下继续生长至现蕾期,观察低温处理植株及对照烟株开花情况,并记录统计烟株的开花时间等相关数据。
结果如图3所示。分析可以看出,ntduf599基因沉默后,转基因烟草植株表现出低温胁迫后花期比非转基因植株及转基因植株提前大约10天的效果。也即,这一结果表明,ntduf599基因与烟草的低温胁迫条件下的早花表型相关,而基于这一结果,可为烟草新品种培育奠定一定技术和理论基础。
sequencelisting
<110>中国烟草总公司郑州烟草研究院
<120>烟草低温早花相关基因ntduf599及其应用
<130>none
<160>2
<170>patentinversion3.5
<210>1
<211>711
<212>dna
<213>nicotianatabacum
<400>1
atggagaaagaaattctggattatgtcttggtaccagtaggattgctatttatggtggct60
tatcacatatggcttcttaatcgcattcttaaacaccctaatcgtacggttatcggcatt120
aattccattaatcgtcacttctgggttcgtgctatgatggaggactcgtccaagaatgga180
gttctagcagtacaaacgttaaggaacaacataatggcgtcaacccttttagcatctact240
gctattatgcttagttccctaatcgccgtcttaatgactggcggaagcaaaggtcgttct300
atcggatttcatgtttacggcgataagagcgatctttgcttatcaattaaattcttctct360
atattggtatgttttatggttgcatttttgtttaacgtgcaatcaattaggtattatagt420
cacgctagtatacttattaacgtgccttacaagaagttggattgttcaagacatattgtg480
acggcggaatatgtagggaggacagtgaatcgaggcagctatttctggtcacttggactg540
cgcgcattttacttttcgtttcctctatttttgtggatctttggccctattcctatgttc600
ctctgctgtattttccttgtttttatgctttatttcctggatggtagttcggattttggg660
tgggttgcagcaactgatgtcgacacccacacagagagagtagcagtttag711
<210>2
<211>236
<212>prt
<213>nicotianatabacum
<400>2
metglulysgluileleuasptyrvalleuvalprovalglyleuleu
151015
phemetvalalatyrhisiletrpleuleuasnargileleulyshis
202530
proasnargthrvalileglyileasnserileasnarghisphetrp
354045
valargalametmetgluaspserserlysasnglyvalleualaval
505560
glnthrleuargasnasnilemetalaserthrleuleualaserthr
65707580
alailemetleuserserleuilealavalleumetthrglyglyser
859095
lysglyargserileglyphehisvaltyrglyasplysseraspleu
100105110
cysleuserilelysphepheserileleuvalcysphemetvalala
115120125
pheleupheasnvalglnserileargtyrtyrserhisalaserile
130135140
leuileasnvalprotyrlyslysleuaspcysserarghisileval
145150155160
thralaglutyrvalglyargthrvalasnargglysertyrphetrp
165170175
serleuglyleuargalaphetyrpheserpheproleupheleutrp
180185190
ilepheglyproileprometpheleucyscysilepheleuvalphe
195200205
metleutyrpheleuaspglyserserasppheglytrpvalalaala
210215220
thraspvalaspthrhisthrgluargvalalaval
225230235
- 还没有人留言评论。精彩留言会获得点赞!