一种化合物、组合物及其在制备具有抗过敏作用的食品、保健品或药物中的应用的制作方法
本发明涉及生物医学技术领域,具体涉及一种化合物、组合物及其在制备具有抗过敏作用的食品、保健品或药物中的应用。
背景技术:
食物过敏是指由人体免疫系统介导的食物不良反应,常见皮肤、消化道、呼吸道症状,如皮疹,过敏性鼻炎等疾病,严重时会出现休克等现象,属于过敏性疾病的一种。婴幼儿为其易感人群,据报道,我国31个城市中0-14岁儿童食物过敏的总患病率为5.83%,其中学龄前儿童(3-5岁)患病率最高(6.65%),并且全球范围内呈逐年增加的趋势。目前常用的治疗策略有避免接触过敏原、口服和舌下免疫疗法等。
中药治疗在亚洲已有上千年历史,在西方国家也早已作为一种辅助性疗法而流行,对食物过敏、过敏性鼻炎等疾病有很好的治疗潜力,比如:中药复方formula-3可以有效降低体内的ige以及肥大细胞脱颗粒并减轻肠道病理改变,从而治疗食物过敏。
益生菌是一类定殖于人体内对宿主有益的活性微生物,它们通过影响肠道菌群而进一步机体的免疫系统,当机体中食物过敏风险因素增加时,益生菌可以促进肠内抗原的降解或结构的修饰、调控促炎因子的分泌、促使肠道菌群正常化、改善肠道黏膜屏障功能,从而影响肠道微生态和免疫系统功能。
中药的有效活性成分通常在于细胞壁内,而植物细胞壁结构致密,这就使有效成分在溶出的过程中受到细胞壁的阻力作用,进而导致药效降低。益生菌在代谢过程中分泌的多种胞外酶,可以分解植物细胞壁中的纤维素等成分,破坏其结构,促进有效成分的溶出从而提高药效。而且中药通过益生菌的发酵还可以使人体更易吸收以及降低毒副作用等。
因此,从中药益生菌发酵物中分离获得结构新颖并具有抗过敏作用的生物活性的小分子化合物具有重要的应用价值。
技术实现要素:
鉴于此,本发明首先提供一种全新结构的化合物,经进一步研究表明,所述的化合物具有抗过敏作用。
本发明的详细技术方案如下:
本发明的第一方面,提供一种化合物,其具有式ⅰ或式ⅱ所示的结构:
为
式ⅰ所述所示结构的化合物命名为:(z)-1-(2,4-dihydroxy-6-methoxy-3-(3-methylbut-1-en-1-yl)-5-(3-methylbut-2-en-1-yl)phenyl)ethan-1-one,简写为lmrs-1。
式ⅱ所述所示结构的化合物命名为:(z)-1-(2,4-dihydroxy-6-methoxy-5-(3-methylbut-1-en-1-yl)-3-(3-methylbut-2-en-1-yl)phenyl)ethan-1-one,简写为lmrs-2。
本发明的第二方面提供一种组合物,其包含式ⅰ和式ⅱ所示结构的化合物。
优选地,式ⅰ和式ⅱ所示结构的化合物的摩尔比为1~10:1~10。
进一步优选地,式ⅰ和式ⅱ所示结构的化合物的摩尔比为1~3:1~3。
最优选地,式ⅰ和式ⅱ所示结构的化合物的摩尔比为1:1。
发明人在经大量的实验研究中发现,式ⅰ所示结构的化合物和式ⅱ所示结构的化合物组合后,取得了比单独使用式ⅰ所示结构的化合物或式ⅱ所示结构的化合物具有更好的抗过敏效果,二者组合后表现出协同抗过敏作用;这是本发明的另一重大研究成果。
优选地,所述的组合物还包含载体,其中,式ⅰ和式ⅱ所示结构的化合物在组合物中的所占的质量分数为10%~85%。
进一步可选的,式ⅰ和式ⅱ所示结构的化合物在组合物中的所占的质量分数为10%~30%、15%~60%或25%~80%。
进一步优选地,所述的载体包括溶剂、聚合物和脂质体中的至少一种。
具体地,所述溶剂包括但不限于水、生理盐水,以及其它非水性溶剂。
具体地,所述聚合物可以但不限于为聚赖氨酸、聚乙烯亚胺及其改性物、壳聚糖、聚乳酸、明胶。
具体地,所述脂质体可以但不限于为胆固醇、豆卵磷脂、蛋黄卵磷脂。进一步可选的,所述载体还包括稀释剂和赋形剂中的一种或多种。
进一步可选的,所述稀释剂包括淀粉类、糖类、纤维素类和无机盐中的一种或多种。
进一步可选的,所述赋形剂包括片剂中的黏合剂、填充剂、润滑剂,半固体制剂软膏剂、霜剂中的基质部分,液体制剂中的防腐剂、抗氧剂、矫味剂、芳香剂、助溶剂、乳化剂、着色剂中的至少一种。
进一步优选地,所述组合物还可以包括第二活性成分。所述第二活性成分根据所述组合物的用途进行选择,在此不作限定。具体的,包括但不限于维生素c、维生素e、辅酶q、谷胱甘肽、胡萝卜素和甜菜碱中的至少一种。
本发明的第三方面,提供上述化合物或组合物在制备具有抗过敏作用的食品、保健品或药物中的应用。
优选地,所述的抗过敏具体为抗食物过敏。
本发明的第四方面,提供上述化合物或组合物在制备具有抗肠炎作用的食品、保健品或药物中的应用。
优选地,所述的化合物或组合物在制备具有抗食物过敏导致肠道内皮细胞炎性损伤作用的食品、保健品或药物中的应用。
本发明的第五方面,提供上述化合物的制备方法,其中,式ⅰ或式ⅱ所示的结构的化合物从枸杞-鼠李糖乳杆菌发酵物中分离得到。
有益效果:本发明提供了全新结构的式ⅰ(lmrs-1)或式ⅱ(lmrs-1)所示的结构的化合物;实验结果表明lmrs-1和lmrs-2可以明显抑制食物过敏导致的肠道内皮细胞炎性因子分泌。这说明本发明所述的lmrs-1和lmrs-2具有优异的抗过敏以及抗肠炎作用;尤其是具有优异的抗食物过敏导致肠道内皮细胞炎性损伤作用。进一步研究表明,将lmrs-1和lmrs-2混合后,其对食物过敏导致的肠道内皮细胞炎性因子分泌抑制作用更加明显,这说明lmrs-1和lmrs-2混合后发挥了协同抗过敏以及抗肠炎作用。(2)由于lmrs-1和lmrs-2具有优异的抗食物过敏以及抗肠炎活性;因此,本发明lmrs-1和lmrs-2可作为抗食物过敏或抗肠炎活性物使用,在保健品或药物中具有广泛的应用前景;(3)此外,本发明所述的lmrs-1和lmrs-2可以采用从枸杞-鼠李糖乳杆菌发酵物中分离得到,其来源丰富、毒副作用低,有利于其在食品、保健品及药品中的应用。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例的附图,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图。
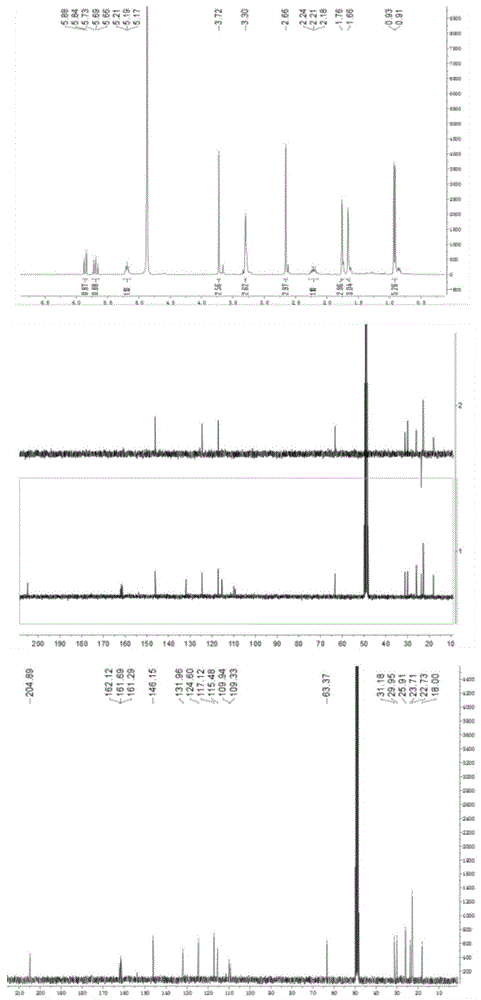
图1是lmrs-1的nmr图。
图2是lmrs-2的nmr图。
图3是lmrs-1、lmrs-2及llh抑制食物过敏诱发的肠道细胞炎性因子分泌实验结果图。
图4是lmrs-1、lmrs-2及llh抑制食物过敏诱发的肠道细胞nf-κb、nlrp3等信号通路蛋白表达实验结果图。
具体实施方式
下面将结合实施例对本发明技术方案进行清楚、完整地描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
实施例1化合物的制备
(1)枸杞-鼠李糖乳杆菌发酵物的制备:枸杞-鼠李糖乳杆菌发酵物的制备方法:新鲜枸杞果榨汁(50g),并加入含有酵母粉5g/l、蛋白胨10g/l、牛肉膏15g/l的鼠李糖乳杆菌发酵培养基(500ml)中发酵12h。收集发酵产物,5000g离心15分钟,收集上清液,低温冻干,获得枸杞-鼠李糖乳杆菌发酵物。
(2)lmrs-1的制备:将10g枸杞-鼠李糖乳杆菌发酵物用100ml乙酸乙酯和1000ml水混合均匀,静置后萃取得到水相层,3次重复萃取过程,将水相层进行真空低温冻干,再经制备型hplc进行制备分离,得到lmrs-1;
其中,制备型hplc的制备条件为:采用rp-hplc(agilent1200hplc)zorbax,sbc-18柱(4.6×250毫米,5μm)分离。洗脱溶剂体系为水-三氟乙酸(溶剂a;100:0.1,v/v)和乙腈三氟乙酸(溶剂b;100:0.1,v/v)。以1.0ml/min的流速从10%到65%的溶剂b梯度洗脱60min,检测波长设置为280nm。lmrs-1的出峰时间为:10.118min。
(3)lmrs-2的制备:将10g枸杞-鼠李糖乳杆菌发酵物用100ml乙酸乙酯和1000ml水混合均匀,静置后萃取得到水相层,3次重复萃取过程,将水相层进行真空低温冻干,再经制备型hplc进行制备分离,得到lmrs-2;
其中,制备型hplc的制备条件为:采用rp-hplc(agilent1200hplc)zorbax,sbc-18柱(4.6×250毫米,5μm)分离。洗脱溶剂体系为水-三氟乙酸(溶剂a;100:0.1,v/v)和乙腈三氟乙酸(溶剂b;100:0.1,v/v)。以1.0ml/min的流速从10%到65%的溶剂b梯度洗脱60min,检测波长设置为280nm。lmrs-2的出峰时间为:15.437min。
将分离得到的lmrs-1和lmrs-2利用质谱和高效液相色谱、nmr对其进行测定,其中质谱测定条件为esi正离子模式毛细管电压3kv,锥孔电压50v,萃取电压5v,脱溶剂温度350℃,雾化气流350l/h;高效液相色谱测定条件为采用bostongreenods-aq色谱柱(250*4.6mm),以0.1%三氟乙酸水溶液为流动相a,以0.1%三氟乙酸的甲醇溶液为流动相a,流动相a:流动相b=60:40,流速为1ml/min,检测波长为310μm,进样量10μl。lmrs-1和lmrs-2的nmr图见图1~图2。
lmrs-1:黄色油状物,hr-esi-ms显示准分子离子峰m/z341.1729[m+na]+(c19h26o4na,理论计算值:341.1723),确定分子式为c19h26o4。1hnmr(300mhz,meod)谱中共显示24个质子信号。δh13.74(1h,s)提示有1个苯环上的羟基氢信号;δh5.19(1h,t,j=6.6hz),5.87(1h,d,j=10.8hz),5.69(1h,dd,j=10.8,9.9hz)提示分子中有3个烯烃质子信号;δh3.30(2h,d,j=6.6hz)为1个连氧次甲基氢信号;δh2.21(1h,m)为1个连氧次甲基氢信号;δh3.72(3h,s),2.66(3h,s),1.76(3h,s),1.66(3h,s),0.92(6h,d,j=6.6hz)提示该化合物还有6个甲基质子信号,其中δh3.72(3h,s),2.66(3h,s)为2个连氧甲基信号。13cnmr(75mhz,meod)谱中共出现19个碳信号,结合dept-135谱可知其分别为8个季碳、4个次甲基、1个亚甲基和6个甲基。低场区可见δc204.9的1个酮羰基信号;δc132.0,124.6和δc146.2,117.1为2对双键碳信号;δc162.1,161.7,161.3,115.5,109.9,109.3可推测为苯环的碳信号。根据以上数据,最终将lmrs-1鉴定为
(z)-1-(2,4-dihydroxy-6-methoxy-3-(3-methylbut-1-en-1-yl)-5-(3-methylbut-2-en-1-yl)phenyl)ethan-1-one(即式ⅰ所示的结构)。
lmrs-2:黄色油状物,hr-esi-ms显示准分子离子峰m/z319.1904[m+h]+(c19h27o4,理论计算值:319.1904),确定分子式为c19h26o4。1hnmr(300mhz,meod)谱中共显示24个质子信号。δh3.34(2h,d,j=6.7hz)为1个连氧亚甲基氢信号;δh2.47(1h,m)为1个连氧次甲基氢信号;δh3.73(3h,s),2.69(3h,s),1.80(3h,s),1.71(3h,s),1.12(6h,d,j=6.7hz)提示该化合物还有6个甲基质子信号,其中δh3.73(3h,s),2.69(3h,s)为连氧甲基信号。13cnmr(75mhz,meod)谱中共出现19个碳信号,结合dept-135谱可知其分别为8个季碳、4个次甲基、1个亚甲基和6个甲基。低场区可见δc205.1的1个酮羰基信号;δc132.5,124.4和δc143.8,117.8为2对双键碳信号;δc162.8,161.3,161.1,115.7,111.1,109.6可推测为苯环的碳信号。根据以上数据,将lmrs-2鉴定为(z)-1-(2,4-dihydroxy-6-methoxy-5-(3-methylbut-1-en-1-yl)-3-(3-methylbut-2-en-1-yl)phenyl)ethan-1-one(即式ⅱ所示的结构)。
实验例
为了评估本发明式ⅰ(lmrs-1)或式ⅱ(lmrs-1)所示的结构的化合物的生物活性,进行如下效果实施例。
利用单纯卵清蛋白(ova)建立小鼠食物过敏模型,将c57bl/6小鼠随机分为5组,每组6只,然后检测以下内容:
将动物分组为:①玉米油空白对照组(a);②ova对照组(b);③lmrs-1组(c);④lmrs-2组(d);⑤llh组(llh为lmrs-2及lmrs-1的等摩尔比例组合物)。
采用灌胃的方法对4-6周龄的c57bl/6雌性小鼠进行处理。a组(空白对照组)则用玉米油灌胃。b组(单纯ova对照组)。ova过敏动物模型的免疫方法方法如下:首先致敏:第9天和第13天皮下注射ova(100μg/只,用生理盐水配制成1mg/ml,并且采用氢氧化铝为佐剂50μl/只);其次激发:每只老鼠灌胃50mgova(溶于0.3ml的生理盐水中),在第19天,第21天,第23天激发三次。lmrs-1组、lmrs-2组及llh组,第23天激发后,每只老鼠灌胃2mglmrs-1、lmrs-2及llh(溶于0.3ml的生理盐水中),连续2天。
小鼠最后一次激发并治疗2天后(day25)眼眶静脉取血(大约500μl):采用双抗体一步夹心法elisa检测血清中il-10,tnf-a、ifn-γ炎性因子含量;采用western-blot检测nk-κb信号通路及nlrp3炎症小体相关蛋白的表达情况。
结果如下:
如图3所示,与control组相比,ova暴露使小鼠体内il-10、tnf-a、ifn-γ含量增加,说明ova暴露诱发小鼠严重的炎症反应,小鼠食物过敏模型构建成功;而lmrs-1、lmrs-2及llh显著抑制了ova暴露诱发的il-10,tnf-a、ifn-γ过量分泌,这说明lmrs-1、lmrs-2以及llh(lmrs-1和lmrs-2的组合物)发挥出显著的抗炎以及抗食物过敏活性。进一步地,由图3还可以看出,lhh活性显著高于lmrs-1及lmrs-2,说明lhh中lmrs-1、lmrs-2具有一定的协同作用,能够协同抑制ova暴露诱发的il-10、tnf-a、ifn-γ过量分泌,发挥协同抗炎以及抗食物过敏活性。
tnf-a、ifn-γ等炎性因子分泌增加会进一步导致小鼠肠道细胞炎性损伤,激活nf-κb信号通路及nlrp3炎症小体。在本研究中,ova刺激可显著上调p-p65、p-iκbα及p-ikkα/β的表达,而lmrs-1、lmrs-2及llh处理显著抑制了p-p65、p-iκbα及p-ikkα/β的表达,表明lmrs-1、lmrs-2及llh(lmrs-1和lmrs-2的组合物)通过抑制nf-κb信号通路激活来调控ova暴露导致的肠道细胞炎性损伤(见图4),发挥抗肠炎活性。进一步的,ova暴露导致的肠道细胞nlrp3炎症小体相关蛋白表达也被lmrs-1、lmrs-2及llh(lmrs-1和lmrs-2的组合物)抑制。其中,lhh对nf-κb信号通路及nlrp3炎症小体激活的抑制活性强于lmrs-1及lmrs-2;这说明lmrs-1和lmrs-2组合后可以发挥协同抗食物过敏导致肠道内皮细胞炎性损伤以及协同抗肠炎活性。
以上所揭露的仅为本发明较佳实施例而已,当然不能以此来限定本发明之权利范围,本领域普通技术人员可以理解实现上述实施例的全部或部分流程,并依本发明权利要求所作的等同变化,仍属于发明所涵盖的范围。
- 还没有人留言评论。精彩留言会获得点赞!