具有光声效果的有机小分子化合物及其制备方法和应用
1.本发明专利涉及生化医学材料技术领域,尤其是指具有光声效果的近红外二区有机小分子荧光探针及其制备方法和在生物医学光声/荧光成像领域的应用。
背景技术:
2.癌症(又名恶性肿瘤),作为人类健康的一大杀手,严重的威胁着人民群众的生活健康。目前,传统的癌症主要检测手段包括x光,ct,mri等成像方法,但由于其时间空间分辨率低,敏感度差,放射性强,背景信号高等缺点,对于早期的癌症的诊断具有一定的不足。
3.光学成像利用分子荧光性质进行成像,包括荧光成像与光声成像,能够克服传统成像方式的不足,实现实时动态监测。近年来开发了近红外二区(1000-1700nm)生物医学荧光成像技术,它为非侵入性生物成像提供了一个高度通用的平台,可以利用它来更深、更清晰地探查生物组织和器官,具有灵敏度高、穿透深度深、时间和空间分辨率高、组织背景干扰少、生物相容性好等优点。此外,在荧光成像的研究之余,光声成像技术开始备受关注。相较于荧光成像,光声成像在深层组织成像中的分辨率更高,比纯光学成像有更好的穿透力,比传统的超声成像拥有更高的分辨率,其图像分辨率可达到微米量级,因此,光声成像可以实现高分辨率的组织成像。
4.在肿瘤诊断中,将近红外二区荧光成像与光声成像联合使用,利用荧光成像确定肿瘤轮廓,再借助光声成像确定肿瘤深度,能够发挥两者成像优势,从而更好的实现肿瘤的全方面定位。然而,目前有报道的具有1000nm以上荧光的近红外二区有机小分子染料种类很少,同时具有光声效果的分子几乎没有,这极大限制了近红外光学成像与光声成像的发展和临床应用。
5.所以,开发具有光声效果的近红外二区有机小分子荧光探针迫在眉睫,具有极大的科研、临床与经济效益。
技术实现要素:
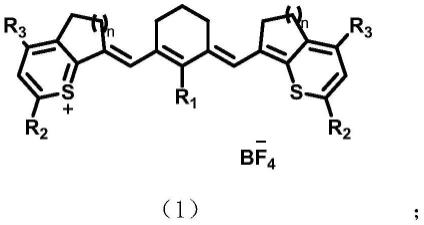
6.本发明旨在至少在一定程度上解决现有技术中存在的技术问题之一,由此,在本发明的第一方面,本发明提供一种具有光声效果的近红外二区有机小分子化合物,所述具有光声效果的近红外二区有机小分子化合物的结构式如下式(1)所示:
7.8.其中,n为1或2;r1选自h、cl和ch3中的一种;r2选自选自中的一种;r3选自选自中的一种。
9.优选地,n为1。
10.优选地,所述具有光声效果的近红外二区有机小分子化合物的结构式如下式(1a)所示:
[0011][0012]
在本发明的一个或多个实施例中,所述具有光声效果的近红外二区有机小分子化合物的荧光发射波长为1000~1200nm,光声最大强度对应的波长为600~900nm。
[0013]
在本发明的第二方面,本发明提供一种本发明的第一方面所述的具有光声效果的近红外二区有机小分子化合物的制备方法,所述式(1)化合物由式(7)化合物制备得到。
[0014]
在本发明的一个或多个实施例中,式(7)化合物制备式(1)化合物的反应式如下所示:
[0015][0016]
其中,n为1或2;r1选自h、cl和ch3中的一种;r2选自
中的一种;r3选自选自中的一种。
[0017]
式(7)化合物制备式(1)化合物包括如下步骤:
[0018]
将化合物(7)、化合物(8)和乙酸钠溶于乙酸酐并置于反应容器中,在60~90℃下反应0.5~6h,冷却至15~35℃,将反应液倒入乙醚中,过滤处理,对所述过滤处理得到的滤渣进行纯化,得到所述式(1)化合物。
[0019]
在本发明的一个或多个实施例中,所述式(7)化合物由式(6)化合物制备得到;
[0020]
式(6)化合物制备式(7)化合物的反应式如下所示:
[0021][0022]
式(6)化合物制备式(7)化合物包括如下步骤:
[0023]
将化合物(6)溶于乙酸酐后加入到反应容器内,再加入三氟化硼乙醚和硫代乙酸,在45~65℃下加热回流,反应2~6h,冷却至15~35℃,加入乙醚,析出固体,过滤,所得滤渣即为化合物(7);
[0024]
在本发明的一个或多个实施例中,所述式(6)化合物由式(4)化合物制备得到;
[0025]
式(4)化合物制备式(6)化合物的反应式如下所示:
[0026][0027]
式(4)化合物制备式(6)化合物包括如下步骤:
[0028]
将化合物(4)与1,4-二氧六环加入到反应容器内,混匀,再加入化合物(5),加热回流2~24h,冷却至15~35℃,分离纯化,得到化合物(6)。
[0029]
在本发明的一个或多个实施例中,所述式(4)化合物由式(2)化合物制备得到;
[0030]
式(2)化合物制备式(4)化合物的反应式如下所示:
[0031][0032]
式(2)化合物制备式(4)化合物包括如下步骤:
[0033]
将化合物(3)与85wt%氢氧化钾溶液中加入到反应容器内,在0℃下混合,10~
30min后,向反应容器内加入化合物(2),在冰浴中搅拌反应3~6h,过滤,将滤渣用冷甲醇洗涤,并真空干燥、结晶,得到化合物(4)。
[0034]
优选地,所述氢氧化钾溶液溶质为氢氧化钾,溶剂为甲醇和水组成的混合溶剂,混合溶剂中,甲醇和水的体积比为(5~7):1;更优选地,混合溶剂中,甲醇和水的体积比为6:1。
[0035]
在本发明的第三方面,本发明提供一种在本发明第一方面所述的具有光声效果的近红外二区有机小分子化合物在制备用于生物体内光声成像的近红外二区荧光成像探针中的用途。
[0036]
在本发明的第四方面,本发明提供一种用于生物体内光声成像的近红外二区荧光成像探针,所述探针由本发明第一方面所述的具有光声效果的近红外二区有机小分子化合物制备得到,所述的具有光声效果的近红外二区有机小分子化合物在其可调控位点修饰多肽、蛋白、聚乙二醇或其衍生物、核酸适配体和叶酸或其衍生物中的一种或多种即得到所述用于生物体内光声成像的近红外二区荧光成像探针。
[0037]
在本发明的第五方面,本发明提供一种在本发明的第四方面所述的用于生物体内光声成像的近红外二区荧光成像探针在制备用于肿瘤光声成像造影剂中的应用。
[0038]
在本发明的第六方面,本发明提供一种在本发明的第四方面所述的用于生物体内光声成像的近红外二区荧光成像探针在制备用于肿瘤近红外二区成像造影剂中的应用。
[0039]
在本发明的第七方面,本发明提供一种自组装纳米胶束,包括本发明的第四方面所述的用于生物体内光声成像的近红外二区荧光成像探针。
[0040]
相比于现有技术,本发明的有益效果在于:
[0041]
1、本发明提供的具有光声效果的近红外二区有机小分子化合物为具有光声性质的全新化合物,其荧光发射波长位于近红外二区,无毒,生物相容性好,易被生物体吸收和代谢,其经包载获得生物相容性好的探针,可用于近红外二区与光声的肿瘤检测等;
[0042]
2、本发明提供的具有光声效果的近红外二区有机小分子化合物具有很强的光声性质,使其比其他仅具有荧光性质的有机小分子探针更优越;
[0043]
3、本发明还提供的具有光声效果的近红外二区有机小分子化合物的合成方法,其合成路线简单,反应效率高,收率高,具有较高的工业应用前景。
[0044]
4、本发明还提供一种荧光探针,在生物医学成像实验中发现该探针的光声成像与荧光效果均非常好,具有广阔的应用前景。
附图说明
[0045]
图1为本发明具有光声效果的近红外二区有机小分子化合物的合成路线;
[0046]
图2为实施例4中化合物(1a)的maldi-tof质谱图;
[0047]
图3为实施例5中荧光探针的制备方法示意图;
[0048]
图4为实施例5中荧光探针lsx的吸收光谱;
[0049]
图5为实施例5中荧光探针lsx发射光谱;
[0050]
图6为实施例5中荧光探针lsx光声信号强度谱;
[0051]
图7为实施例5中荧光探针lsx对于生物组织穿透能力图;
[0052]
图8为实施例5中荧光探针lsx纳米颗粒的dls粒径图;
[0053]
图9为实施例6中荧光探针lsx对原位骨肉瘤小鼠模型的体内近红外二区成像图;
[0054]
图10为实施例7中荧光探针lsx对原位骨肉瘤小鼠模型的体内光声成像图。
具体实施方式
[0055]
下面将结合实施例对本发明的方案进行解释。本领域技术人员将会理解,下面的实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。以下实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行,使用的方法如无特别说明,均为本领域公知的常规方法,使用的耗材和试剂如无特别说明,均为市场购得。除非另有说明,本文中所用的专业与科学术语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法或材料也可应用于本发明中。
[0056]
本发明提供一种具有光声效果的近红外二区有机小分子化合物,所述具有光声效果的近红外二区有机小分子化合物的结构式如下式(1)所示:
[0057][0058]
其中,n为1或2;r1选自h、cl和ch3中的一种;r2选自选自中的一种;r3选自选自中的一种。
[0059]
上述具有光声效果的近红外二区有机小分子化合物(式(1)所示化合物)的制备路线(如图1所示)如下所示:
[0060][0061]
以下以化合物(1a)为示例具体化合物说明以通式1的合成方法:
[0062]
具有光声效果的近红外二区有机小分子化合物1a的合成路线如下所示,
[0063][0064]
具有光声效果的近红外二区有机小分子化合物1a的合成具体步骤如实施例1~4所示。
[0065]
实施例1:化合物(4a)的制备
[0066]
取化合物(3a)(20mmol,2.24g),20ml 85%的koh溶液(85%的koh溶液是通过将1.32g koh溶解在5ml的水和30ml的meoh中制得),二者混合在0℃条件下反应。10min后,向其中加入2.33ml的化合物(2a)(21.6mmol,2.72g),在冰浴中搅拌3h,然后过滤以获得滤渣。将滤渣用40mmol冷甲醇洗涤,并真空干燥,得4.2g淡黄色结晶,为化合物(4a),产率90%。
[0067]
化合物(4a)的结构检测结果如下:
[0068]1h nmr(400mhz,cdcl3)δ7.96(d,j=15.2hz,1h),7.84(dd,j=3.7,0.9hz,1h),7.67(dd,j=4.9,0.9hz,1h),7.39(dd,j=23.9,4.2hz,2h),7.24(d,j=12.2hz,1h),7.20
–
7.16(m,1h),7.09(dd,j=5.0,3.7hz,1h).
[0069]
13
c nmr(101mhz,cdcl3)δ181.54,145.54,140.07,136.39,134.04,132.30,131.87,129.11,128.49,128.41,120.29.
[0070]
实施例2:化合物(6a)的制备
[0071]
取实施例1制备得到的化合物(4a)(4.5mmol,1.0g)溶于10ml 1,4-二氧六环,混匀后再加入化合物5a(9mmol,1.2g),加热回流2h,冷却至室温。通过柱硅胶分离纯化(pe:ea=
20:1)。得500mg为深红色固体,为化合物(6a),产率72%。
[0072]
化合物(6a)的结构检测结果如下:
[0073]1h nmr(400mhz,cdcl3)δ7.83(dd,j=3.8,0.9hz,1h),7.62(dd,j=4.9,0.9hz,1h),7.15
–
7.08(m,2h),6.91
–
6.84(m,2h),4.07(td,j=7.2,3.9hz,1h),3.75(dt,j=17.6,8.8hz,1h),3.40(dd,j=16.4,7.1hz,1h),2.58
–
2.47(m,1h),2.32
–
2.13(m,2h),2.05
–
1.92(m,1h),1.90
–
1.61(m,4h).
[0074]
实施例3:化合物(7a)的制备
[0075]
将实施例2制备得到的化合物(6a)(0.7mmol,200mg)溶于10ml乙酸酐中,加入三氟化硼乙醚(5.2mmol,0.52ml)和硫代乙酸(2.6mmol,0.09ml),在55℃下加热回流。反应2h后冷却至室温,加入50ml乙醚,析出沉淀,过滤,得土黄色粉末192mg,为化合物(7a),产率43%。
[0076]
化合物(7a)的结构检测结果如下:
[0077]1h nmr(400mhz,cd3cn)δ8.66(s,1h),8.25(d,j=3.5hz,1h),8.21(d,j=5.0hz,1h),8.00(dd,j=6.0,4.6hz,2h),7.51
–
7.45(m,1h),7.41
–
7.35(m,1h),3.53(dt,j=17.0,7.6hz,4h),2.46
–
2.37(m,2h).
[0078]
13
c nmr(101mhz,cd3cn)δ138.58,137.06,135.65,132.34,130.97,117.93,38.56,36.11,24.30.
[0079]
实施例4:化合物(1a)的制备
[0080]
将实施例3制备得到的化合物(7a)(0.02mmol,6.3mg),化合物(8a)(0.01mmol,3.2mg)和乙酸钠(0.02mmol,1.7mg)溶于5ml乙酸酐中,85℃下反应2h。反应结束后冷却至室温,将反应液倒入20ml乙醚中,洗掉杂质,过滤,得到的黑色固体即为化合物(1a)粗产品。经hplc(0min:95%a,5%b;30min:5%a,95%b;a相为含0.5%tfa的一级水,b相为含0.5%tfa的乙腈)纯化得1mg深黑色固体,为化合物1a,产率16%。
[0081]
化合物(1a)的结构检测结果如下:
[0082]1h nmr(400mhz,cd3cn)δ8.90(dd,j=8.2hz,4h),7.89(s,1h),7.59(m,4h),7.15(d,2h),7.01(d,2h),6.51(s,1h),6.10(d,2h),3.14(s,4h),2.56(t,4h),1.79(s,4h),1.21(m,1h).
[0083]
maldi-tof-ms calcd for:c40h30cls6+([m-bf4]+):737.04,found:736.76.
[0084]
制备得到的化合物(1a)的maldi-tof质谱图如图2所示。
[0085]
实施例5
[0086]
将实施例4制备得到的化合物(1a)进一步制备为近红外二区荧光探针lsx,并检测其光声性能荧光探针的制备方法示意图如图3所示,具体步骤如下:
[0087]
将6mg二硬脂酰基磷脂酰乙醇胺-聚乙二醇、1mg化合物(1a)置于2ml离心管中并加入1ml四氢呋喃将其溶解,得到四氢呋喃混合液。另取50ml离心管并加入20ml一级冰水,在超声条件将上述四氢呋喃混合液滴加至一级水中,并保持超声10min。然后在室温下使用氮气流吹干有机溶剂。将溶液过0.22微米滤膜,再使用30k millipore超滤离心管,5000r/min离心20min,浓缩至1ml,制得浓度为1mg/ml的荧光探针lsx。荧光探针lsx的吸收光谱、发射光谱以及光声信号强度谱如图4、图5、图6所示;其中,图4为荧光探针lsx的吸收光谱;图4为荧光探针lsx发射光谱;图6为荧光探针lsx光声信号强度谱;由图可知,吸收波长约为
1075nm,在808nm激光的激发下,发射波长约为1150nm。图8为实施例5所示荧光探针lsx纳米颗粒的dls粒径图。由图可知,探针lsx纳米颗粒的dls平均粒径约为120nm。
[0088]
将荧光探针lsx置于直径3mm的细管中,使用不同厚度的鸡胸肉覆盖在细管上,使用光声成像仪检测其细管内的光声信号,从而测得荧光探针lsx对于生物组织的最大穿透深度。图7为荧光探针lsx对于生物组织穿透能力图。
[0089]
实施例6:荧光探针lsx对原位骨肉瘤小鼠近红外二区活体成像
[0090]
将实施例5制备得到的荧光探针lsx(200μg/ml pbs,200μl)通过尾静脉注入到原位骨肉瘤荷瘤小鼠体内,并对其进行不同时间点(8h、12h、24h、30h、36h、48h、54h、60h、72h)的近红外二区活体荧光成像。结果如图9所示,由图可以看出,随着注射探针时间的推移,荧光探针lsx在模型鼠的肿瘤部位的富集明显增加,60小时达到最大,说明探针lsx对骨肉瘤具有很好的靶向性,能用于活体骨肉瘤近红外二区荧光成像。
[0091]
实施例7:荧光探针lsx对原位骨肉瘤小鼠的光声活体成像
[0092]
将实施例5制备得到的荧光探针lsx(1mg/ml pbs,200μl)通过尾静脉注入到骨肉瘤荷瘤小鼠体内,并在第60小时对其进行光声成像。结果如图10所示,由图可以看出,模型鼠的肿瘤部位出现了明显的光声信号,说明探针lsx能够在肿瘤部位富集,且荧光信号较强,能用于活体骨肉瘤光声成像。
[0093]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1