一种脆弱拟杆菌灭活菌粉及其制备方法与流程
本发明涉及脆弱拟杆菌灭活菌粉的制备和应用技术,特别是一种脆弱拟杆菌灭活菌粉及其制备方法。
背景技术:
1、脆弱拟杆菌(bacteroides fragilis)是革兰氏阴性厌氧细菌中拟杆菌属的成员,属于拟杆菌门,完全不同于厚壁菌门的双歧杆菌、乳酸菌等。拟杆菌属有25个菌种,仅来自人类的有10个菌种,仅来自动物的有10个菌种,来自人和动物的有5个菌种。脆弱拟杆菌是一种专性厌氧细菌,依据能否合成、分泌脆弱拟杆菌肠毒素(bft)可将其分为产肠毒素型脆弱拟杆菌(enterotoxigenic bacteroides fragilis,etbf)和非产肠毒素型脆弱拟杆菌(nontoxigenic bacteroides fragilis,ntbf)。脆弱拟杆菌作为人及动物肠道正常菌群的一部分,主要存在于结肠中。此外,呼吸道、胃肠道及泌尿生殖道粘膜也可定植生长。
2、已有文献报道了ntbf作为益生菌的可能性(sun f,zhang q,zhao j,zhang h,zhai q,chen w.a potential species of next-generation probiotics?the dark andlight sides of bacteroides fragilis in health.food res int.2019dec;126:108590.doi:10.1016/j.foodres.2019.108590.epub 2019 jul 27.pmid:31732047.)。但是,由于益生菌的活菌特性,在它的使用中,存在以下副作用:1)在危重病人、老人及新生儿,特别是早产儿中存在易位到局部组织和血液的风险;2)活菌可能获得/转移抗生素抗性基因和/或毒力基因;3)活菌对环境条件要求严格,易在提取、运输和储存中失活,且不易标准化;4)产品质地随活菌状态改变,稳定性和适口性波动。
3、针对上述问题,副益生菌(paraprobiotic)应运而生。副益生菌被定义为“无活力的微生物细胞,如果口服或局部使用足够的数量,即可为使用者带来好处”。该定义包括形态不完整的微生物细胞和形态完整的微生物细胞,主流研究观点认为,破碎的微生物细胞能够更好地释放功能分子,因此具有更好的效果;但对于完整的灭活微生物细胞,没有统一的观点能够说明其在某些应用中优于活菌的原因。目前针对副益生菌的研究集中在乳杆菌、双歧杆菌等一代益生菌上,研究方向相对固定。因此,有必要开发新型副益生菌,扩展副益生菌的适应症范围。
技术实现思路
1、鉴于以上背景技术,本发明提供如下技术方案:
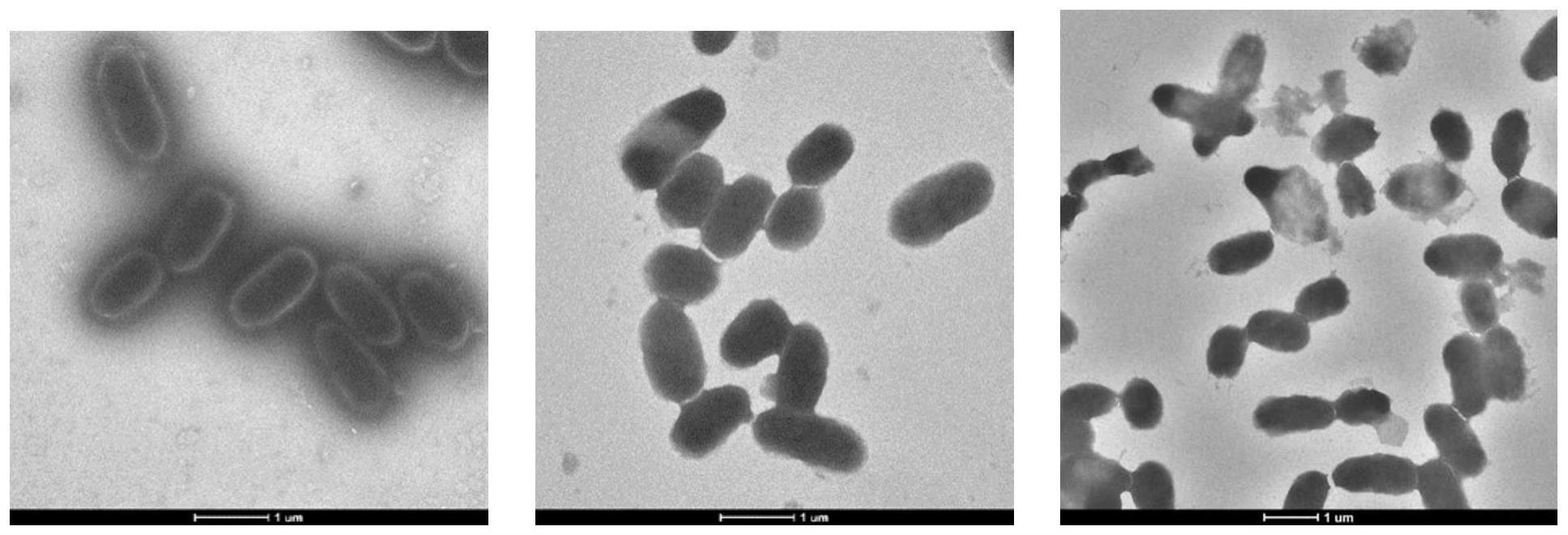
2、在第一方面,本发明提供了一种脆弱拟杆菌灭活菌粉,其中包括脆弱拟杆菌灭活菌(脆弱拟杆菌的保藏号为cgmcc no.10685的脆弱拟杆菌zy-312);所述脆弱拟杆菌灭活菌的菌体包括完整的细胞形态结构;菌数达到1×1011cell/g以上。
3、根据本发明的实施方案,所述脆弱拟杆菌灭活菌粉还包括辅料。
4、根据本发明的实施方案,所述脆弱拟杆菌灭活菌粉中,所述脆弱拟杆菌灭活菌与所述辅料的质量比为1:(0.05-4)。
5、根据本发明的实施方案,所述辅料包括赋形剂。优选地,所述辅料在室温下为固体。
6、优选地,所述赋形剂包括甘露醇、山梨醇、麦芽糊精、乳糖、氯化钠、麦芽糖、蔗糖、葡萄糖、海藻糖、右旋糖酐、脯氨酸、赖氨酸、丙氨酸、酪蛋白、脱脂乳中的至少一种或两种以上的组合。
7、根据本发明的实施方案,所述赋形剂中包括氯化钠。优选地,所述赋形剂中,氯化钠的质量分数为0-25wt%。
8、在第二方面,本发明还提供脆弱拟杆菌灭活菌粉的制备方法,特别地,通过所述制备方法制得的脆弱拟杆菌灭活菌粉,其菌体细胞结构完整,所述制备方法包括以下步骤:
9、(1)取脆弱拟杆菌发酵培养;
10、(2)发酵培养结束后,对发酵液进行离心,收集菌体,按菌体与氯化钠水溶液的重量体积比为1g:(10~30)ml加入氯化钠水溶液洗涤、离心,得到洗涤后菌体;
11、(3)向洗涤后菌体中加入第一赋形剂溶液混合重悬得到菌体溶液,再进行灭活处理,离心,收集灭活菌泥;
12、(4)向步骤(3)获得的灭活菌泥中加入第二赋形剂溶液,得灭活菌原液;
13、(5)将步骤(4)获得的灭活菌原液干燥至残留水分低于5wt%,即得脆弱拟杆菌灭活菌粉。
14、根据本发明的实施方案,步骤(2)中,发酵液的菌数达到108cfu/ml以上。
15、根据本发明的实施方案,步骤(2)中,所述氯化钠水溶液的质量浓度为0.6-1.5wt%,优选为0.65-1.2wt%,更优选为0.8-1.0wt%,最优选0.85-0.95wt%,例如为0.9wt%的氯化钠水溶液。
16、根据本发明的实施方案,步骤(3)中,所述菌体与第一赋形剂溶液的重量体积比为1g:(5~40)ml。
17、根据本发明的实施方案,步骤(3)中,所述第一赋形剂溶液中,赋形剂的质量分数为4~30wt%,所述赋形剂具有如上所述含义。
18、根据本发明的实施方案,步骤(3)中,所述第一赋形剂溶液的溶剂选自氯化钠水溶液,其中,所述氯化钠水溶液具有如上所述含义。进一步优选地,所述第一赋形剂溶液的溶剂选自生理盐水,例如0.9wt%氯化钠水溶液。
19、根据本发明的实施方案,步骤(3)中,所述灭活处理的方法选自热灭活、冷冻灭活或者化学灭活中的至少一种,优选为热灭活。
20、优选地,所述热灭活的温度为60~100℃,热灭活的时间为10~60min。
21、根据本发明的实施方案,步骤(4)中,加入第二赋形剂溶液使灭活菌原液的总重量与步骤(3)灭活前的菌体溶液重量一致。优选地,所述第二赋形剂溶液与所述第一赋形剂溶液相同或不相同。
22、根据本发明的实施方案,所述第二赋形剂溶液中,赋形剂的质量分数为4~30wt%,所述赋形剂具有如上所述含义。
23、优选地,所述第二赋形剂溶液的溶剂选自氯化钠水溶液,其中,所述氯化钠水溶液具有如上所述含义。进一步优选地,所述第一赋形剂溶液的溶剂选自生理盐水,例如0.9wt%氯化钠水溶液。
24、示例性地,所述第二赋形剂溶液与所述第一赋形剂溶液相同。
25、根据本发明的实施方案,步骤(5)中,所述干燥的方式选自真空冷冻干燥和/或喷雾干燥,优选为真空冷冻干燥。
26、优选地,所述真空冷冻干燥的条件包括:冷冻温度为-20~-40℃,冷冻时间为1~3小时,真空度为0.20~0.25mbar。
27、示例性地,所述真空冷冻干燥的工艺包括:-40±2℃预冻1~3小时后,-20±2℃预冻0.5~1h,最后-40±2℃再预冻0.5~2h,0.25mbar真空度下经一次干燥、解析干燥制备成灭活菌粉。
28、根据本发明的实施方案,所述制备方法中,对所述离心的条件不做具体限定,只要能实现所需的离心效果即可,例如所述离心的转速为10000~20000rpm。
29、在第三方面,本发明还提供一种药物制剂,所述药物制剂含有上述脆弱拟杆菌灭活菌粉。
30、根据本发明的实施方案,所述药物制剂选自经口给药制剂、灌肠剂或凝胶剂中的至少一种或两种以上的组合。
31、本领域技术人员能够理解,根据本发明的各个方面以及各个实施方案中所包含的特征可以彼此独立进行组合,只要进行组合的特征之间不存在冲突。
32、有益效果:
33、本发明的发明人通过开发了能够保证脆弱拟杆菌灭活菌体完整的菌粉及其制备方法,通过本发明的制备方法所制得的脆弱拟杆菌灭活菌粉能够更有效保证与活菌制剂相关性质的一致性,尤其是在使用时能够减轻癌症相关的胃肠道副作用。另外,与活菌制剂相比,通过本发明的灭活菌粉制备的药物制剂的存储方式更为简单,还延长了药物制剂的有效期。
- 还没有人留言评论。精彩留言会获得点赞!