一种脐带华通氏胶二次培养收获原代间充质干细胞的方法与流程
1.本发明涉及生物技术领域,具体而言,涉及一种脐带华通氏胶二次培养收获原代间充质干细胞的方法。
背景技术:
2.间充质干细胞(mscs,mesenchymal stem cells)是干细胞家族的重要成员,来源于发育早期的中胚层,属于多能干细胞,可以在骨髓、脂肪、滑膜、骨骼、肌肉和脐带等多种组织中分离,具有向成骨细胞、成软骨细胞、成脂肪细胞、骨髓基质、神经细胞、肝脏细胞、胰岛细胞和心肌细胞等多向分化的潜能。具有来源方便,易于分离、培养、扩增和纯化,多次传代扩增后仍具有干细胞特性,不存在免疫排斥的特性。脐带来源的间充质干细胞由于脐带采集过程简单,对产妇及新生儿无任何危害及损伤,脐带间充质干细胞生长环境单一、体外提取方便,使得提取的间充质干细胞纯度高、数量大,且不存在伦理问题,成为骨髓间充质干细胞的理想替代物,具有更广阔的临床应用潜能。
3.脐带华通氏胶为脐带间充质干细胞的主要来源,分离方法分为酶消化和组织块贴壁,其中,组织块贴壁法为一次或多次贴壁分离,一次贴壁分离不能最大化获取华通氏胶中的间充质干细胞,多次贴壁分离虽然可以更多获得间充质干细胞,但会使用到动物源血清,存在感染病原微生物的风险,且操作繁琐,同时细胞易分化。
4.有鉴于此,特提出本发明。
技术实现要素:
5.本发明的目的在于提供一种脐带华通氏胶收获原代间充质干细胞的方法。
6.为了实现本发明的上述目的,特采用以下技术方案:
7.一种脐带华通氏胶收获原代间充质干细胞的方法,脐带华通氏胶组织块依次经过首次培养和二次培养,获得原代间充质干细胞;
8.其中,首次培养和二次培养所用的培养基包括:dmem培养基、13v/v%-17v/v%自体血小板裂解液、1-3mmol/l l-谷氨酰胺和0.5-2mmol/l白血病抑制因子。
9.进一步地,首次培养和二次培养所用的培养基包括:dmem培养基、15v/v%自体血小板裂解液、2mmol/l l-谷氨酰胺和1mmol/l白血病抑制因子。
10.进一步地,首次培养包括:脐带华通氏胶组织块第0天加入培养基静置培养6-8天,此后每隔2-3天换液培养,第13-14天收获原代间充质干细胞。
11.优选地,第0天,脐带华通氏胶组织块与培养基的体积比为1:(1-5),优选为1:3;
12.优选地,培养至第2天,还包括补加培养基的步骤,所述补加培养基的体积为补加前体积的1-3倍,优选为2倍。
13.进一步地,收集首次培养后的华通氏胶组织块进行二次培养,二次培养包括:第0天将脐带华通氏胶组织块加入培养基静置培养4-5天,然后换液培养,第6-7天收获原代间充质干细胞。
14.进一步地,收获原代间充质干细胞的方法采用胰酶消化收集。
15.进一步地,还包括对原代间充质干细胞进行检测的步骤。
16.进一步地,检测指标包括:细胞计数、细胞活力、表面标志物、细胞周期和间充质干细胞三系分化能力。
17.进一步地,表面标志物包括阳性指标和阴性指标,阳性指标包括cd44、cd73、cd90和cd105,阴性指标包括cd14、cd19、cd34、cd45和hla-dr。
18.进一步地,脐带华通氏胶组织块的制备方法包括:选取无淤血、无组织损伤的脐带,经消毒后剥离华通氏胶,华通氏胶剪碎得到华通氏胶组织块。
19.进一步地,消毒包括先用0.9%生理盐水清洗,再用医用碘伏消毒2-3min。
20.与现有技术相比,本发明的有益效果为:
21.本发明提供的脐带华通氏胶收获原代间充质干细胞的方法,避免了动物血清的使用,同时由于培养基中使用的是血小板裂解液和白血病抑制因子,所以加快了间充质干细胞爬出的时间从而将脐带华通氏胶的培养次数控制在二次以内,抑制了多次培养造成的细胞分化。
附图说明
22.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
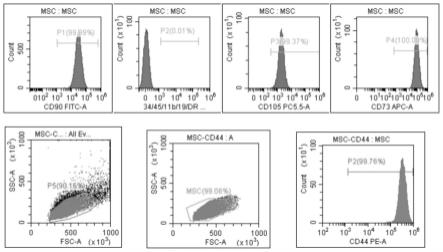
23.图1为实施例1的原代间充质干细胞表面标志物流式检测结果;
24.图2为对比例1的原代间充质干细胞表面标志物流式检测结果;
25.图3为对比例2的原代间充质干细胞表面标志物流式检测结果;
26.图4为实施例1的原代间充质干细胞显微镜观察结果;
27.图5为对比例1的原代间充质干细胞显微镜观察结果;
28.图6为对比例2的原代间充质干细胞显微镜观察结果;
29.图7为实施例1的原代间充质干细胞革兰氏染色结果;
30.图8为对比例1的原代间充质干细胞革兰氏染色结果;
31.图9为对比例2的原代间充质干细胞革兰氏染色结果。
具体实施方式
32.下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。
33.除非另有说明,本文中所用的专业与科学术语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法或材料也可应用于本发明中。
34.本发明提供一种脐带华通氏胶收获原代间充质干细胞的方法,脐带华通氏胶组织块依次经过首次培养和二次培养,获得原代间充质干细胞;
35.其中,首次培养和二次培养所用的培养基包括:dmem培养基、13v/v%-17v/v%自
体血小板裂解液、1-3mmol/l l-谷氨酰胺和0.5-2mmol/l白血病抑制因子。
36.白血病抑制因子(leukemia inhibitory factor,lif)是一种具有多种生物学功能的细胞因子。白血病抑制因子是il-6族的重要成员,可调节细胞的分化、生长和更新等多个生理过程。lif可以创造一个免疫抑制的微环境,在胚胎的着床、生长、分化、发育等过程中起重要作用。lif还具有抑制脂蛋白脂肪酶的活性、抑制干细胞的分化等功能。lif调控的stat3信号可以调节细胞的生存、自我更新以及众多抗凋亡相关的靶基因。大量的文献表明,lif能够维持多种细胞在不同生理或病理环境下的生存。lif在大鼠子宫壁全层损伤、脑出血后胶质瘢痕形成及大鼠坐骨神经再生研究中表现出明显的优势效应。
37.血小板裂解液,脐带血富集血小板(prp)激活获得的裂解物,由于其源于血小板,内含丰富的各类生长因子及蛋白质,如血小板源性生长因子,转化生长因子β,血管内皮细胞生长因子,表皮生长因子和类胰岛素生长因子等;这些生长因子在促进细胞增殖、再分化、趋化和刺激血管再生、修复等多方面发挥重要的作用。
38.本发明提供的脐带华通氏胶收获原代间充质干细胞的方法,避免了动物血清的使用,同时由于培养基中使用的是血小板裂解液和白血病抑制因子,所以加快了间充质干细胞爬出的时间从而将脐带华通氏胶的培养次数控制在二次以内,抑制了多次培养造成的细胞分化。
39.需要说明的是,培养基中自体血小板裂解液指的是与华通氏胶相同来源的脐带血制备得到的血小板裂解液。
40.在优选地实施方式中,首次培养和二次培养所用的培养基包括:dmem培养基、15v/v%自体血小板裂解液、2mmol/l l-谷氨酰胺和1mmol/l白血病抑制因子。在该培养基培养条件下,脐带华通氏胶可以快速大量得到间充质干细胞。
41.在优选地实施方式中,首次培养包括:脐带华通氏胶组织块第0天加入培养基静置培养6-8天,此后每隔2-3天换液培养,第13-14天后收获原代间充质干细胞。
42.优选地,第0天,脐带华通氏胶组织块与培养基的体积比为1:(1-5),优选为1:3;
43.优选地,培养至第2天,还包括补加培养基的步骤,所述补加培养基的体积为补加前体积的1-3倍,优选为2倍。
44.在优选地实施方式中,收集首次培养后的华通氏胶组织块进行二次培养,二次培养包括:第0天将脐带华通氏胶组织块加入培养基静置培养4-5天,然后换液培养,第6-7天收获原代间充质干细胞。
45.在优选地实施方式中,收获原代间充质干细胞的方法采用胰酶消化收集。
46.在优选地实施方式中,在首次培养和二次培养后得到的原代间充质干细胞需要进行检测。检测指标包括:细胞计数、细胞活力、表面标志物、细胞周期和间充质干细胞三系分化能力。
47.具体地,表面标志物包括阳性指标和阴性指标,阳性指标包括cd44、cd73、cd90和cd105,阴性指标包括cd14、cd19、cd34、cd45和hla-dr。
48.在优选地实施方式中,脐带华通氏胶组织块的制备方法包括:选取无淤血、无组织损伤的脐带,经消毒后剥离华通氏胶,华通氏胶剪碎得到华通氏胶组织块。进一步地,消毒包括先用0.9%生理盐水清洗,再用医用碘伏消毒2-3min。
49.基于上述技术方案,进一步地,脐带华通氏胶收获原代间充质干细胞的方法步骤
如下:
50.步骤一、脐带标本的选取、前处理:选取无淤血、无组织损伤的脐带,先使用0.9%生理盐水清洗,目的是去除胎粪;再使用医用碘伏消毒处理2-3分钟,目的是降低细菌的污染的风险。
51.步骤二、华通氏胶的剥离:剔除脐带的两条动脉,一条静脉,位于羊膜与血管之间的白色结缔组织即为华通氏胶,用有齿镊将其撕下,放入无菌平皿中;将剥离的华通氏胶,使用手术剪刀剪成小的组织块,使用0.9%生理盐水洗涤胶体,采用1800prm离心5min的方法收集胶体。
52.步骤三、组织块首次贴壁:根据胶体重量,第0天加入适量培养基静置培养24小时后,补加培养基,将接种好的培养瓶放置co2培养箱中静置培养至第6-8天,之后每隔2-3天进行换液培养,直至第13-14天收获原代间充质干细胞。
53.收集的脐带华通氏胶用于二次贴壁,贴壁细胞加入胰酶消化,在倒置显微镜下观察,贴壁细胞80%脱落加入:dmem培养基(内含胰酶抑制剂)中止消化过程,反复吹打瓶底至细胞完全脱落,收集,原培养瓶中加入少量氯化钠注射液冲洗,洗涤液收集。将消化液和洗涤液混合,离心收集原代间充质干细胞。
54.步骤四、组织块二次贴壁:根据在倒置显微镜下观察组织块爬出的细胞生长状态,将原有培养基与组织块离心洗涤。将组织块(华通氏胶)用生理盐水清洗1800prm离心5min,重新贴壁培养,第0天加5ml培养基,静置培养4-5天,第5天换液,第7天可以收获原代间充质干细胞。
55.步骤五、收获原代间充质干细胞、鉴定:步骤三、四获取的原代间充质干细胞进行细胞活力、细胞纯度及均一性、间充质干细胞三系诱导分化、细胞周期鉴定。
56.下面通过具体的实施例进一步说明本发明,但是,应当理解为,这些实施例仅仅是用于更详细地说明之用,而不应理解为用于以任何形式限制本发明。
57.实施例1
58.1、脐带筛选:脐带来自医院足月妊娠健康产妇,产前检查乙型肝炎、丙型肝炎、梅毒、人类免疫缺陷病病毒、巨细胞病毒、eb病毒等均阴性。产妇及家属对脐带和脐带血用于实验研究均知情同意。
59.2、脐带处理:从采集瓶中取出脐带,测量脐带长度。用无菌有齿镊转移脐带至10cm空白培养皿中,用碘伏消毒整根脐带外表面3min,转入新的平皿中,用氯化钠注射液冲洗,去除血渍。用无菌剪刀剪去两端手术结扎线,取脐带约长10~15cm用于制备。
60.3、华通氏胶分离:用无菌组织剪将制备用脐带剪成约2~3cm数段,加入氯化钠注射液洗涤血凝块,重复洗涤直至无血渍,洗涤液清晰。剔除血管:剔除脐带的两条动脉,一条静脉。分离华通氏胶:位于羊膜与血管之间的白色结缔组织即为华通氏胶,用有齿镊将其撕下,放入无菌平皿中,加入氯化钠注射液,洗涤胶体。
61.4、组织块制备:华通胶用生理盐水充分洗涤3次,转移至新的50ml离心管中,充分剪碎至1mm3~3mm3大小;加入氯化钠注射液1500prm,离心5min。
62.5、接种:根据胶体重量,加入脐带间充质干细胞培养基,培养基组成如下表所示,定容组织匀浆,t75培养瓶中接种1ml组织匀浆,加入3ml培养基培养。
[0063][0064]
6、原代细胞培养
[0065]
将接种好的组织块,在培养瓶放置37℃培养箱中静置培养24h后,补加8ml培养基。将接种好的培养瓶放置co2培养箱中静置培养6-8天,之后每隔2-3天进行换液培养,直至第13-14天收获原代间充质干细胞。
[0066]
7、原代细胞收获
[0067]
将瓶中的贴壁组织块晃掉和完全培养基一并转移至离心管内备用,加入少量氯化钠注射液冲洗原瓶,弃除冲洗液。在培养瓶中加入3ml胰酶消化,消化1min左右在倒置显微镜下观察,贴壁细胞80%脱落加入备用培养基中止消化过程,反复吹打瓶底至细胞完全脱落,移入一支新的离心管中,原培养瓶中加入少量氯化钠注射液冲洗,洗涤液并入离心管中。配平1500prm,离心5min。
[0068]
8、组织块二次培养
[0069]
二次培养是把收获原代细胞的华通氏胶用生理盐水清洗离心后重新贴壁培养,第0天加5ml培养基,静置培养4-5天,第5天进行换液,第7天可以收获原代间充质干细胞。
[0070]
对比例1
[0071]
与实施例1的区别在于,脐带间充质干细胞培养基中不添加白血病抑制因子(lif)。
[0072]
对比例2
[0073]
与实施例1的区别在于,脐带间充质干细胞培养基中不添加自体血小板裂解液。
[0074]
试验例1
[0075]
检测实施例1和对比例1-2收获的原代间充质干细胞的细胞活率和细胞计数,如下表所示:
[0076] 细胞活率细胞计数实施例199.52%4.1
×
105/ml对比例190.56%1.2
×
105/ml对比例288.52%2.3
×
105/ml
[0077]
结论:对比例1、2与实施例1相比细胞活率和细胞密度有所下降,其中未添加白血病抑制因子(lif)的对比例1细胞密度减少,收获的细胞量少。
[0078]
试验例2
[0079]
对实施例1和对比例1-2的间充质干细胞表面标志物流式检测,结果如图1、图2和图3所示。
[0080]
结论:直观上从流式表面标志物的比例是符合间充质干细胞的要求,但是从fsc(细胞大小)和ssc(细胞内容物)还是有区别的:实施例1细胞相对小些,收获的颗粒中,占比在90%以上,细胞均一;对比例1细胞相对大些,与实施例1相比,cd90和cd105要稍弱些,且cd90数据要离散;对比例2细胞小,与实施例1相比,cd90分两个锋,有一小部分表达弱。
[0081]
试验例3
[0082]
对实施例1和对比例1-2的间充质干细胞进行显微镜观察和革兰氏染色,结果图4、图5、图6、图7、图8和图9所示。实施例1的细胞在培养瓶中贴壁生长,梭形,并呈鱼群状生长;革兰氏染色后,细胞呈球形,大小均一,内容物饱满,健硕。
[0083]
对比例1的细胞个体较大,大小为实施例1的3-5倍。
[0084]
对比例2的细胞呈梭形,但有悬浮细胞出现;革兰氏染色后,其细胞大小与实施例1一致,但细胞形态不均一,有分化份趋势。
[0085]
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以作出许多其它的更改和修改。因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些变化和修改。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1