一种琥珀酸亚铁四水合物晶型、其制备方法、包含该晶型的原料组合物及其用途与流程
1.本发明涉及药物化学技术领域,具体涉及一种琥珀酸亚铁四水合物新的晶型、其制备方法、包含该晶型的原料组合物及其在药物制剂中的应用。
背景技术:
2.琥珀酸亚铁为一种相对稳定的琥珀酸与亚铁的络合物,不易被氧化,比起三价铁,亚铁刺激性小,不容易引起胃肠道刺激等副作用。琥珀酸亚铁传统晶型为琥珀酸亚铁的碱式盐(fec4h4o4)4.fe(oh)2,虽然其性能相对稳定,亚铁在贮存过程中不易氧化,但是其溶解度低,在肠液中几乎不溶,导致制剂生物利用度低,临床研究数据表明琥珀酸亚铁的碱式盐的生物利用度仅有16%,需要多次、高剂量服药,才能达到目标血药浓度要求。
3.专利cn 101205180a公开了一种统琥珀酸亚铁的制备工艺,其为传统的琥珀酸亚铁碱式盐制备方法,未能获得溶解度较高的琥珀酸亚铁晶型。
4.本发明中涉及的琥珀酸亚铁四水合物晶型,解决了现有琥珀酸亚铁的溶解度问题,且保存了亚铁的稳定性特性,并将其制备成的原料组合物,最终制备成缓释制剂、速释制剂等。
技术实现要素:
5.为了解决目前琥珀酸亚铁碱式盐的溶解度低,生物利用度低的问题,本发明的目的是提供一种琥珀酸亚铁四水合物晶型,其在肠液ph中溶出较快,提高了药物的生物利用度,且保存了亚铁的稳定性优势;为此,本发明还提供了上述琥珀酸亚铁四水合物晶型的制备方法,及包含该晶型的原料组合物和其用途。
6.为了实现上的目的,本发明采用以下技术方案:
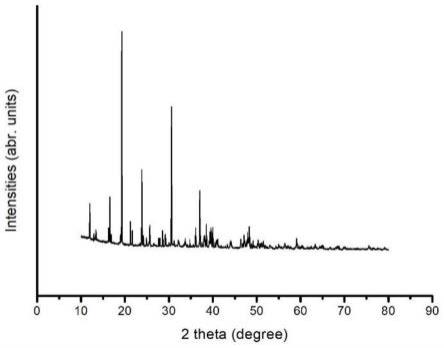
7.本发明的第一方面,提供一种琥珀酸亚铁四水合物晶型,所述琥珀酸亚铁四水合物晶型的x射线粉末衍射图中,以度表示的2θ衍射角在约11.98、16.56、19.28、21.24、23.84、25.62、30.68、37.04、38.54处有明显的特征吸收峰。
8.具体地,所述琥珀酸亚铁四水合物晶型具有基本上如图1所示的x射线粉末衍射图。
9.本发明的第二方面,提供一种上述琥珀酸亚铁四水合物晶型的制备方法,包括如下步骤:
10.s1、将六水合丁二酸钠和七水合硫酸亚铁分别溶于水中,得到六水合丁二酸钠溶液、七水合硫酸亚铁溶液;
11.s2、将六水合丁二酸钠溶液缓慢滴加至七水合硫酸亚铁溶液中,在惰性气体保护下反应,反应时,调节反应溶液ph至4.0-4.8,反应温度为70-80℃,反应完成后,再进行降温结晶处理,得到结晶液;
12.s3、将结晶液经过滤处理,滤出物经同温的去离子水和乙醇洗涤,再经真空干燥,
即得琥珀酸亚铁四水合物。
13.具体地,所述步骤s2中,在进行降温结晶处理时,先将反应溶液温度降至55-65℃,再以18-22℃/h的降温速率将反应溶液的温度逐级降温至25-35℃。
14.具体地,所述步骤s1中,六水合丁二酸钠和七水合硫酸亚铁的质量比为1:(0.9-1.1)。
15.本发明的第三方面,提供一种原料组合物,包括权利要求1或2所述的琥珀酸亚铁四水合物晶型80-120份、保护剂80-120份、抗氧剂0.1-0.3份和致孔剂5-15份。
16.优选地,原料组合物,包括琥珀酸亚铁四水合物晶型100份、保护剂100份、抗氧剂0.2份和致孔剂10份。
17.具体地,所述保护剂为十六醇、混合脂肪酸甘油酯38型、混合脂肪酸甘油酯40型中的至少一种,所述抗氧剂为生育酚,具体地为dl-α-生育酚,所述致孔剂为蔗糖、氯化钠中的至少一种。
18.本发明的第四方面,提供一种上述原料组合物的制备方法,具体步骤如下:将保护剂在45-50℃下搅拌融化完全,再向其中依次加入抗氧剂和致孔剂搅拌均匀,随后向其中加入琥珀酸亚铁四水合物晶型,搅拌均匀,然后经冷却固化、粉碎后,即得原料组合物。
19.本发明的第五方面,提供一种上述原料组合物的用途,所述原料组合物用于制备治疗贫血相关疾病的药物组合物,所述药物组合物包括药物有效量的所述原料组合物以及药学上可接受的赋形剂。
20.具体地,所述药物组合物的剂型为速释剂型或缓释剂型。
21.琥珀酸亚铁四水合物的速释剂型制剂,其处方成分包括:原料组合物、填充剂、崩解剂、润滑剂和包衣粉。填充剂为微晶纤维素、磷酸氢钙二水合物、无水磷酸氢钙、淀粉、乳糖、甘露醇、糊精中的一种或几种组合;崩解剂为羧甲淀粉钠、交联聚维酮、交联羧甲基纤维素钠中的一种或几种组合;润滑剂为硬脂酸镁、硬脂酸锌、硬酯富马酸钠中的一种或几种组合;包衣粉包括欧巴代85f或欧巴代85g。
22.上述速释剂型制剂制备方法如下:将原料组合物、填充剂、崩解剂于干法制粒机中制粒,随后整粒,之后加润滑剂进行混合;对于颗粒剂,直接按照相关规格进行包装;对于片剂,则在混合时外加崩解剂,压片,后加入包衣粉进行包衣处理。
23.琥珀酸亚铁四水合物的缓释剂型制剂,其处方组成包括:原料组合物、填充剂/缓释骨架、粘合剂、润滑剂、包衣粉。缓释骨架材料为羟丙甲纤维素k100、羟丙甲纤维素k15m、羟丙甲纤维素k4m中的一种或几种组合;填充剂为微晶纤维素、蔗糖、甘露醇、乳糖中的一种或几种组合;粘合剂为聚维酮k30或羟丙甲纤维;润滑剂为硬脂酸镁、硬脂酸锌、硬脂富马酸钠中的一种或几种组合;包衣粉包括欧巴代85f或欧巴代85g。
24.溶蚀型缓释片制备方法如下:原料组合物与填充剂,于湿法制粒机中混匀,之后加入粘合剂进行制粒,再于沸腾干燥器中干燥,后进行整粒,后加润滑剂混合,再压片,后加入包衣粉进行包衣处理。
25.渗透型缓释片制备方法如下:原料组合物与缓释骨架材料,于湿法制粒机中混匀,之后加入粘合剂进行制粒,再于沸腾干燥器中干燥,后进行整粒,后加润滑剂混合,再压片,后加入包衣粉进行包衣处理。
26.与现有技术相比,本发明具有如下有益效果:
27.本发明中的琥珀酸亚铁四水合物晶型,其在肠液ph中溶出较快,提高了药物的生物利用度,并且保存了亚铁的稳定性的优势;并将琥珀酸亚铁四水合物晶型制备成原料组合物,进一步提高原料药的稳定性,使得其不易被氧化,能够在常规环境下长期保存;此外,采用该琥珀酸亚铁四水合物晶型,不仅能制备成缓释剂型制剂,一天一次,避免多次服药,增加患者适应性,还能制成速释剂型制剂,达到快速释放,快速补铁功能。
附图说明
28.下面结合附图与具体实施例对本发明作进一步详细说明。
29.图1为实施例1中琥珀酸亚铁四水合物晶型的的x-射线粉末衍射谱图。
具体实施方式
30.实施例1
31.琥珀酸亚铁四水合物晶型的制备:
32.s1、将六水合丁二酸钠125g溶于250ml水中,加热至60℃搅拌溶解,再进行过滤,滤液在60℃保温待用,得到六水合丁二酸钠溶液;
33.s2、将250ml水加热至60℃,加入硫酸(质量分数为98%)0.7ml,然后再加入七水合硫酸亚铁125g搅拌溶解,然后通入氮气,置换反应容器内空气,并持续保温60℃;
34.s3、将六水合丁二酸钠溶液缓慢滴加至七水合硫酸亚铁溶液中,控制滴加速度,在15min内滴加完毕,并通氮气保护整个反应过程,之后用5wt%的稀硫酸/10wt%氢氧化钠溶液调节反应溶液ph至4.5,反应温度为70℃,在缓慢搅拌条件下,保温反应40min,当反应液开始由淡绿色澄清,变成棕色略发白浑浊时,反应完成,此时将反应溶液缓慢降温至55℃,之后再以18℃/h的降温速率将反应溶液的温度逐级降温至25℃,继续搅拌30min,得到结晶液;
35.s4、将结晶液经过滤处理,滤出物经同温的去离子水和乙醇分别洗涤两次,再在60℃下真空干燥,即得白色颗粒(琥珀酸亚铁四水合物晶型)87.1g,收率82%。
36.取实施例1的白色颗粒产物进行xrd粉末衍射检测,仪器型号:日本理学smartlab 9kw;参数设置:smartlab 9kw advance powder x-ray cu ka radiation diffractometer,波长0.15406nm,电压40kv,电流40ma;
37.测得琥珀酸亚铁四水合物晶型的x射线粉末衍射图谱见图1,衍射相关数据见表1。
38.表1
[0039][0040]
实施例2
[0041]
琥珀酸亚铁四水合物晶型的制备:
[0042]
s1、将六水合丁二酸钠125g溶于250ml水中,加热至60℃搅拌溶解,再进行过滤,滤液在60℃保温待用,得到六水合丁二酸钠溶液;
[0043]
s2、将250ml水加热至60℃,加入硫酸0.7ml,然后再加入七水合硫酸亚铁112.5g搅
拌溶解,然后通入氮气,置换反应容器内空气,并持续保温60℃;
[0044]
s3、将六水合丁二酸钠溶液缓慢滴加至七水合硫酸亚铁溶液中,控制滴加速度,在20min内滴加完毕,并通氮气保护整个反应过程,之后用5wt%的稀硫酸/10wt%氢氧化钠溶液调节反应溶液ph至4.0,反应温度为80℃,在缓慢搅拌条件下,保温反应30min,当反应液开始由淡绿色澄清,变成棕色略发白浑浊时,反应完成,此时将反应溶液缓慢降温至65℃,之后再以22℃/h的降温速率将反应溶液的温度逐级降温至35℃,继续搅拌30min,得到结晶液;
[0045]
s4、将结晶液经过滤处理,滤出物经同温的去离子水和乙醇分别洗涤两次,再在60℃下真空干燥,即得白色颗粒(琥珀酸亚铁四水合物)86.7g,收率81.6%。
[0046]
对实施例2中获得的样品进行x射线粉末衍射分析,其衍射图谱基本如图1所示,与实施例1的鉴定结果一致。
[0047]
实施例3
[0048]
琥珀酸亚铁四水合物晶型的制备:
[0049]
s1、将六水合丁二酸钠125g溶于250ml水中,加热至60℃搅拌溶解,再进行过滤,滤液在60℃保温待用,得到六水合丁二酸钠溶液;
[0050]
s2、将250ml水加热至60℃,加入硫酸0.7ml,然后再加入七水合硫酸亚铁137.5g搅拌溶解,然后通入氮气,置换反应容器内空气,并持续保温60℃;
[0051]
s3、将六水合丁二酸钠溶液缓慢滴加至七水合硫酸亚铁溶液中,控制滴加速度,在15min内滴加完毕,并通氮气保护整个反应过程,之后用5wt%的稀硫酸/10wt%氢氧化钠溶液调节反应溶液ph至4.8,反应温度为75℃,在缓慢搅拌条件下,保温反应40min,当反应液开始由淡绿色澄清,变成棕色略发白浑浊时,反应完成,此时将反应溶液缓慢降温至60℃,之后再以20℃/h的降温速率将反应溶液的温度逐级降温至30℃,继续搅拌30min,得到结晶液;
[0052]
s4、将结晶液经过滤处理,滤出物经同温的去离子水和乙醇分别洗涤两次,再在60℃下真空干燥,即得白色颗粒(琥珀酸亚铁四水合物)87.3g,收率82.2%。
[0053]
对实施例3中获得的样品进行x射线粉末衍射分析,其衍射图谱基本如图1所示,与实施例1的鉴定结果一致。
[0054]
实验例1
[0055]
对实施例1中制得的琥珀酸亚铁四水合物晶型与现有的琥珀酸亚铁碱式盐进行饱和溶解度测定
[0056]
介质:水、0.1n盐酸、ph6.8磷酸盐
[0057]
0.1n盐酸配制:9ml盐酸加入1000ml水中,搅拌均匀,即得。
[0058]
ph6.8磷酸盐配制:6.8g磷酸二氢钾与0.9g氢氧化钠于1000ml水中,搅拌溶解,即得。
[0059]
饱和溶解度测试条件:温度37
±
0.5℃,介质体积100ml,取样时间24h,30h。取样10ml,用pes膜过滤,弃初滤液2ml,取续滤液测定总铁含量。
[0060]
供试品溶液:取0.66ml续滤液于100ml量瓶中,加入10ml的2m乙酸钠溶液,2ml的盐酸羟胺放置5min,再加2ml的邻二氮菲显色,用水稀释定容,10min后进行紫外分光光度计测定吸收在510nm处的吸收强度。并用相应的对照品测试,计算供品浓度。
[0061]
测试结果见表2。
[0062]
表2
[0063][0064]
由表2中测试结果可知,对比琥珀酸亚铁碱式盐,实施例1中制得的琥珀酸亚铁四水合物晶型在高ph条件下,具有明显提高饱和溶解度的优势,此性质,更利于制得的铁剂在肠道等弱碱环境中的吸收。
[0065]
实施例4
[0066]
琥珀酸亚铁四水合物晶型的原料组合物的制备过程如下:
[0067]
将2kg保护剂(十六醇)加入至不锈钢锅中,在50℃下搅拌融化完全,保温,再向其中依次加入4g抗氧剂(dl-α-生育酚)和200g致孔剂(蔗糖)搅拌均匀,随后向其中加入2kg由实施例1中制备方法制得的琥珀酸亚铁四水合物晶型,搅拌均匀,然后经冷却固化、粉碎后,粉碎机筛网孔径1mm,得到小颗粒状的混合物,即得原料组合物。
[0068]
实施例5
[0069]
琥珀酸亚铁四水合物晶型的原料组合物的制备过程如下:
[0070]
将0.8kg保护剂(混合脂肪酸甘油酯38型)加入至不锈钢锅中,在45℃下搅拌融化完全,再向其中依次加入1g抗氧剂(dl-α-生育酚)和50g致孔剂(蔗糖)搅拌均匀,随后向其中加入0.8kg由实施例1中制备方法制得的琥珀酸亚铁四水合物晶型,搅拌均匀,然后经冷却固化、粉碎后,粉碎机筛网孔径1mm,得到小颗粒状的混合物,即得原料组合物。
[0071]
实施例6
[0072]
琥珀酸亚铁四水合物晶型的原料组合物的制备过程如下:
[0073]
将1.2kg保护剂(混合脂肪酸甘油酯40型)加入至不锈钢锅中,在50℃下搅拌融化完全,再向其中依次加入3g抗氧剂(dl-α-生育酚)和150g致孔剂(氯化钠)搅拌均匀,随后向其中加入1.2kg由实施例1中制备方法制得的琥珀酸亚铁四水合物晶型,搅拌均匀,然后经冷却固化、粉碎后,粉碎机筛网孔径1mm,得到小颗粒状的混合物,即得原料组合物。
[0074]
实验例2
[0075]
琥珀酸亚铁四水合物晶型的原料组合物影响因素试验
[0076]
试验条件:高温60℃;高湿92.5%rh;高温+高湿:40℃+75%rh;敞口放置;
[0077]
时间15天;30天
[0078]
测定方法:测定样品中高铁含量
[0079]
高铁含量测定方法:取本品3g,置于250ml碘瓶中,用除去二氧化碳的水l00ml与盐
酸l0ml的混合溶液溶解,加碘化钾3g,立即密塞,轻轻摇匀,在暗处放置5分钟,用0.1m硫代硫酸钠滴定液滴定释放的碘,用淀粉浆作为指示剂。不加供试品重复以上滴定操作。每1ml的0.1m硫代硫酸钠滴定液相当于5.585mg的fe
3+
。
[0080]
对比现有技术的琥珀酸亚铁碱式盐、实施例1中制得的琥珀酸亚铁四水合物晶型、实施例4中制得的含有琥珀酸亚铁四水合物晶型的原料组合物在不同实验条件下样品中的高铁含量,测试结果见表3。
[0081]
表3
[0082][0083][0084]
由表3中测试结果可知,琥珀酸亚铁碱式盐与实施例1中琥珀酸亚铁四水合物在高温、高湿、高温+高湿环境中的稳定性类似,实施例4中的含有琥珀酸亚铁四水合物晶型的原料组合物比琥珀酸亚铁碱式盐及实施例1中琥珀酸亚铁四水合物在高温、高湿、高温+高湿环境中的稳定性高,其能够长期在极端条件下放置而不被氧化。
[0085]
实施例7
[0086]
琥珀酸亚铁四水合物缓释片i制备
[0087]
处方如表4所示:
[0088]
表4
[0089]
原辅料名称作用单剂量(mg)琥珀酸亚铁四水合物api200十六醇骨架材料200蔗糖致孔剂20dl-生育酚抗氧剂0.4硬脂酸镁润滑剂4二氧化硅助流剂4
欧巴代包衣粉85g包衣12总重 440.4
[0090]
琥珀酸亚铁四水合物原料的制备:将2kg保护剂(十六醇)加入至不锈钢锅中,在50℃下搅拌融化完全,保温,再向其中依次加入4g抗氧剂(dl-a-生育酚)和200g致孔剂(蔗糖)搅拌均匀,随后向其中加入2kg实施例1中制得的琥珀酸亚铁四水合物晶型,搅拌均匀,然后经冷却固化、粉碎后,粉碎机筛网孔径1mm,得到小颗粒状的混合物4.13kg;
[0091]
整粒:得到的粉末颗粒用40目筛网进行整粒,粗颗粒再用粉碎整粒机进行整粒,粉碎整粒机筛网孔径1.2mm,然后再40目筛网整粒,合并细颗粒,得到颗粒3.98kg。
[0092]
混合:将整粒好的颗粒于三维混合机中,加入二氧化硅39.8g,预混5min,转速9rpm。然后再加入硬脂酸镁39.8g,混合3min。
[0093]
压片:直径11mm,圆形冲;片重440mg;硬度:80-120n。
[0094]
包衣:将欧巴代包衣粉85g配制成12%浓度的混悬液,然后于包衣锅中对素片进行包衣,包衣进风温度60℃,包衣增重2.5-3.5%。
[0095]
实施例8
[0096]
琥珀酸亚铁四水合物缓释片ii制备
[0097]
处方如表5所示:
[0098]
表5
[0099]
原辅料名称作用单剂量(mg)琥珀酸亚铁四水合物api200羟丙甲纤维素k100m骨架材料220羟丙甲纤维素k4m骨架材料80微晶纤维素填充剂70蔗糖致孔剂30聚维酮k30粘合剂30硬脂酸镁润滑剂6欧巴代包衣粉85g包衣18总重 654
[0100]
粘合剂配制:称取0.3kg聚维酮k30,加入2.7kg水中,搅拌溶解,配制成10%粘合剂。
[0101]
制粒:称取实施例1中制得的琥珀酸亚铁四水合物晶型2kg,羟丙甲纤维素k100m 2.2kg,羟丙甲纤维素k4m 0.8kg微晶纤维素0.7kg,蔗糖0.3kg于湿法制粒机中,搅拌干混,混匀,搅拌转速120rpm,之后加入粘合剂制粒,粘合剂加入制粒时间6min,搅拌转速120rpm,然后剪切10s,剪切速度1500rpm。
[0102]
干燥:将颗粒于沸腾干燥器中干燥,干燥进风温度60℃,干燥时间15-20min,监测水分,水分控制小于3%,收料6.53kg。
[0103]
整粒:于震荡筛过20目筛,粗颗粒于粉碎整粒机中整粒,筛网孔径2mm,之后再进行震荡筛整粒,反复操作,得到细颗粒合并,得6.45kg。
[0104]
混合:整粒好的物料颗粒于三维混合机中混合,开始混合6min,转速9rpm,后加入硬脂酸镁64g,混合3min,收料6.5kg。
[0105]
压片:冲模直径12mm,圆形冲。片重636mg;硬度:100-150n。
[0106]
包衣:将欧巴代包衣粉85g配制成12%浓度的混悬液,然后于包衣锅中对素片进行包衣,包衣进风温度60℃,包衣增重2.5-3.5%。
[0107]
实施例9
[0108]
琥珀酸亚铁四水合物速释片制备
[0109]
处方如表6所示:
[0110]
表6
[0111]
原辅料名称作用单剂量(mg)琥珀酸亚铁(四水合)api100无水磷酸氢钙(直压型)填充剂120微晶纤维素102填充剂80羧甲淀粉钠崩解剂10硬脂酸镁润滑剂2胶态二氧化硅助流剂2欧巴代包衣粉85g包衣10总重 324
[0112]
过筛分散:将琥珀酸亚铁(四水合)1kg,无水磷酸氢钙(直压型)1.2kg,微晶纤维素(102型)0.8kg及羧甲淀粉钠100g,胶态二氧化硅20g于三维混合机中混合3min,之后再粉碎整粒机中分散,筛网孔径1mm,得混粉3.1kg。
[0113]
混合:将过筛混粉于三维混合机中混合6min,然后再加硬脂酸镁20g,混合3min,混合速度9rpm。
[0114]
压片:冲模直径9mm,圆形冲;片重314mg;硬度70-110n。
[0115]
包衣:将欧巴代包衣粉85g配制成12%浓度的混悬液,然后于包衣锅中对素片进行包衣,包衣进风温度60℃,包衣增重2.5-3.5%。
[0116]
实验例3
[0117]
实施例7、实施例8中制得的琥珀酸亚铁(四水合)缓释片i、ii及实施例9中制得的速释片在ph6.8磷酸盐介质中的释放曲线测定
[0118]
ph6.8磷酸盐配制:6.8g磷酸二氢钾与0.9g氢氧化钠于1000ml水中,搅拌溶解,即得。
[0119]
溶出条件(缓释片):桨法,介质体积900ml,温度:37
±
0.5℃;取样时间30min,60min,90min,2h,4h,6h,8h。
[0120]
溶出条件(速释片):桨法,介质体积900ml,温度:37
±
0.5℃;取样时间:5min,10min,15min,20min,30min,45min。
[0121]
检测方法:参考中国药典2020版第四部通则对总铁含量测定法。
[0122]
实施例7、实施例8中制得的琥珀酸亚铁(四水合)缓释片i、ii的溶出曲线结果见表7,实施例9中制得的速释片的溶出曲线结果见表8。
[0123]
表7
[0124][0125]
表8
[0126][0127]
由表7和表8中测试结果可知,采本发明中制得到的琥珀酸亚铁四水合物晶型制备成缓释剂型制剂,能持久、缓慢地释放,一天一次,避免多次服药,增加患者适应性;采用制得到的琥珀酸亚铁四水合物晶型制备成速释剂型制剂,在30min内溶出度达到96%,达到快速释放,快速补铁功能。
[0128]
综上,本发明中的琥珀酸亚铁四水合物晶型,其在肠液ph中溶出较快,提高了药物的生物利用度,并且保存了亚铁的稳定性的优势;并将琥珀酸亚铁四水合物晶型制备成原料组合物,进一步提高原料药的稳定性,使得其不易被氧化,能够在常规环境下长期保存;此外,采用该琥珀酸亚铁四水合物晶型,不仅能制备成缓释剂型制剂,一天一次,避免多次服药,增加患者适应性,还能制成速释剂型制剂,达到快速释放,快速补铁功能。
[0129]
以上应用了具体个例对本发明进行阐述,只是用于帮助理解本发明,并不用以限制本发明。对于本发明所属技术领域的技术人员,依据本发明的思想,还可以做出若干简单推演、变形或替换。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1