导致血小板无力症的ITGA2B基因复合突变体、复合突变体蛋白和应用的制作方法
导致血小板无力症的itga2b基因复合突变体、复合突变体蛋白和应用
技术领域
1.本发明属于生物医学技术领域,具体涉及导致血小板无力症的itga2b基因复合突变体、复合突变体蛋白和应用。
背景技术:
2.血小板无力症(mim 273800)又称glanzmann病,1918年由glanzmann首先报道本病,故称“glanzmann病(glanzmann thrombasthenia,gt)”,是一种常染色体隐性遗传性出血病。特点为血细胞对多种生理诱聚剂反应低下或缺如,由血小板膜糖蛋白ⅱb(gpⅱb)和(或)ⅲa(gpⅲa)质或量的异常引起。1990年国际血栓与止血学会标准化委员会将glanzmann病定义为由于gp
ꢀⅱ
b或gpⅲa基因缺陷引起的血小板对多种诱聚剂(如腺苷二磷酸、凝血酶、胶原等)的先天性遗传性无聚集或反应减低。
3.本病是由于血小板膜糖蛋白ⅱb(gpⅱb)和(或)ⅲa(gpⅲa)质或量的异常引起。gpⅱb
‑ⅲ
a复合物是钙依赖性多聚体,是纤维蛋白原受体,也能结合vwf、纤维结合蛋白和血栓敏感蛋白,在各种生理诱聚剂,如adp、txa2的作用下,介导血小板聚集。因此受体的异常可导致血管损伤处血小板血栓不能形成发生出血不止或淤斑。gpⅱb
‑ⅲ
a受体同时也能帮助血小板α颗粒摄取纤维蛋白原,因此,glanzmann病患者血小板纤维蛋白原水平显著下降。gpⅱb
‑ⅲ
a复合物是连接膜外侧的纤维蛋白原和膜内侧的肌动蛋白丝主要附着点,参与血块回缩功能故gt患者常出现血块回缩不良。血小板无力症被分为3型:表达量小于正常人的5%为ⅰ型,5%-20%为ⅱ型,表达量正常但有功能缺陷的为ⅲ型,亦称为变异型血小板无力症。
4.gpⅱb和gpⅲa是由不同的基因编码,其中编码gpⅱb的itga2b基因(mim 607759)定位于染色体17q21.31,基因全长17.5kb,包含30个外显子和29个内含子,编码1030个氨基酸组成的gpⅱb。目前发现的基因突变类型包括点突变、缺失和插入基因突变等可以引起glanzmann病,最常见的突变类型为错义突变和无义突变,其次为小的插入缺失突变,而大的缺失和插入突变很罕见。基因突变导致gpⅱb
‑ⅲ
a四级结构异常而不具备受体活性同样不能结合纤维蛋白原。研究表明,gpⅱb与gpⅲa在粗面内质网内合成后很快地形成复合物,复合物形成有助于防止糖蛋白被蛋白溶解酶消化。gpⅱb和gpⅲa都为血小板受体功能所必需,因此,两者之一的缺陷均可导致相同的功能障碍。本病患者磷酸甘油醛脱氢酶、丙酮酸激酶、谷胱苷肽过氧化物酶和谷胱苷肽还原酶异常,活力降低从而使血小板功能和血块回缩不良。
5.基因突变是导致血小板无力症发生发展的重要遗传基础,基因诊断是确诊血小板无力症的重要标准。临床上需要针对不同突变建立相应的检测技术并用于明确病因和疾病诊断,现有技术中对基因突变位点基因型的检测,可以采用其他方法限制性酶切片段长度多态性、单链构象多态性、等位基因特异的寡聚核苷酸杂交等等,但这些检测方法均不能同时满足定性、定量及明确突变基因的序列的目的,所以需要针对特异突变位点设计引物,并结合sanger测序技术完成基因序列检测工作。
技术实现要素:
6.本发明的目的在于提供导致血小板无力症的itga2b基因复合突变体、复合突变体蛋白和应用,本发明发现了新的itga2b基因突变位点,与现有itga2b基因突变位点复合形成新的itga2b基因复合突变体,可以作为血小板无力症的筛查和诊断位点,将患者、携带者和正常人群区分开,指导患者的精准治疗和优生优育。
7.本发明提供了itga2b基因突变体,所述itga2b基因突变体与野生型itga2b基因相比包括c.1156c》t突变。
8.本发明还提供了上述技术方案所述的itga2b基因突变体编码的itga2b突变体蛋白,所述itga2b突变体蛋白与野生型itga2b蛋白相比包括p.r386*突变。
9.本发明提供了导致血小板无力症的itga2b基因复合突变体,所述itga2b基因复合突变体包括复合杂合突变,所述复合杂合突变包括c.2333a》c突变和上述技术方案所述的c.1156c》t突变。
10.本发明还提供了上述技术方案所述的itga2b基因复合突变体编码的itga2b复合突变体蛋白,所述itga2b复合突变体蛋白包括p.q778p突变和上述技术方案所述的p.r386*突变。
11.本发明还提供了上述技术方案所述的itga2b基因复合突变体或所述的itga2b复合突变体蛋白作为检测靶点在制备下述ⅰ~ⅶ中的一种或多种的试剂盒中的应用:
[0012]ⅰ:血小板无力症诊断试剂盒;
[0013]ⅱ:血小板无力症筛查试剂盒;
[0014]ⅲ:血小板无力症产前诊断试剂盒;
[0015]ⅳ:血小板无力症产前筛查试剂盒;
[0016]
ⅴ
:血小板无力症孕前诊断试剂盒;
[0017]ⅵ:血小板无力症孕前筛查试剂盒;
[0018]ⅶ:辅助防治血小板无力症的试剂盒。
[0019]
本发明还提供了一种用于检测上述技术方案所述的itga2b基因复合突变体或所述的itga2b复合突变体蛋白的试剂,所述试剂包括引物、探针、抗体和质谱检测试剂中的至少一种。
[0020]
本发明还提供了一种用于检测上述技术方案所述的itga2b基因复合突变体的引物组,所述引物组包括检测所述c.1156c》t突变的引物对itga2b-1和检测所述c.2333a》c突变的引物对itga2b-2;
[0021]
所述引物对itga2b-1的上游引物itga2b-1f的核苷酸序列如seq id no.1所示,所述引物对itga2b-1的下游引物itga2b-1r的核苷酸序列如seq id no.2所示;
[0022]
所述引物对itga2b-2的上游引物itga2b-2f的核苷酸序列如seq id no.3所示,所述引物对itga2b-2的下游引物itga2b-2r的核苷酸序列如seq id no.4所示。
[0023]
本发明还提供了一种用于诊断和/或筛查血小板无力症的试剂,所述试剂包括上述技术方案所述的引物组。
[0024]
优选的,所述试剂还包括测序引物和扩增所需要的试剂;
[0025]
所述测序引物包括所述c.1156c》t突变的测序引物itga2b-seq1和所述c.2333a》c突变的测序引物itga2b-seq2;
[0026]
所述测序引物itga2b-seq1的上游引物itga2b-seq1f的核苷酸序列如seq id no.5所示,所述测序引物itga2b-seq1的下游引物itga2b-seq1r的核苷酸序列如seq id no.6所示;
[0027]
所述测序引物itga2b-seq2的上游引物itga2b-seq2f的核苷酸序列如seq id no.7所示,所述测序引物itga2b-seq2的下游引物itga2b-seq2r的核苷酸序列如seq id no.8所示。
[0028]
本发明还提供了上述技术方案所述的试剂在制备诊断、筛查和辅助防治血小板无力症的任意一种或多种试剂盒中的应用。
[0029]
有益效果:
[0030]
本发明提供了itga2b基因突变体,所述itga2b基因突变体与野生型itga2b基因相比包括c.1156c》t突变。本发明所述itga2b基因突变体为首次发现的itga2b基因突变体,所述c.1156c》t突变指野生型itga2b基因第12号外显子的第12号外显子的第1156位上的碱基由c突变为t碱基,导致所编码的蛋白质的第386位氨基酸残基由精氨酸突变为终止密码子,形成itga2b突变体蛋白。
[0031]
本发明还提供了导致血小板无力症的itga2b基因复合突变体,所述itga2b基因复合突变体包括上述技术方案所述的c.1156c》t突变和c.2333a》c突变。本发明所述itga2b基因复合突变体中的c.2333a》c突变为现有itga2b基因突变位点,指野生型itga2b基因第23号染色体上的第2333位a突变为c,该突变可能导致所编码的蛋白质第778位氨基酸残基由谷氨酰胺变为脯氨酸。由本发明首次发现的c.1156c》t突变与现有的c.2333a》c突变复合组成复合杂合突变,进而形成itga2b基因复合突变体。本发明所述itga2b基因复合突变体可以形成itga2b复合突变体蛋白,所述突变体蛋白包括p.r386*突变和p.q778p突变。本发明首次发现itga2b基因复合突变体或itga2b复合突变体蛋白可以导致血小板无力症,且与血小板无力症的发病密切相关,通过检测该itga2b突变体蛋白在生物样品中是否存在,可以有效地检测受试者是否携带有上述突变,用于筛查或诊断血小板无力症致病基因突变携带者或患者,以提供优生优育和治疗干预指导为治疗血小板无力症提供可能的药物靶点。
附图说明
[0032]
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍。
[0033]
图1显示血小板无力症1号家系遗传图谱;其中,表示男性携带者,表示女性携带者,
■
表示男性患者,
↗
表示先证者;
[0034]
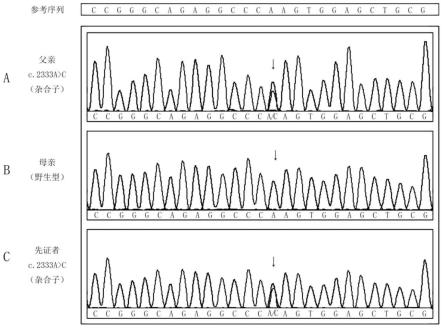
图2显示利用sanger测序检测1号家系itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点基因型的结果图,其中,a层和c层:1号家系中突变者;b层:1号家系中基因型为野生型(测序图中箭头所指为突变发生位置);
[0035]
图3显示利用sanger测序检测1号家系itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*位点基因型的结果图,其中,b层和c层:1号家系中突变者;a层:1号家系中基因型为野生型(测序图中箭头所指为突变发生位置);
[0036]
图4显示血小板无力症2号家系遗传图谱;其中,表示男性携带者,表示女性携带者,
■
表示男性患者,
◇
表示胎儿,
↗
表示先证者;
[0037]
图5显示利用试剂盒检测2号家系itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点基因型的结果图;其中,b、c和d层:1号家系中突变者;a层:1号家系中基因型为野生型(测序图中箭头所指为突变发生位置);
[0038]
图6显示利用试剂盒检测2号家系itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*位点基因型的结果图;其中,a、c层和d层:1号家系中突变者;b层:1号家系中基因型为野生型(测序图中箭头所指为突变发生位置)。
[0039]
图7显示血小板无力症1号家系遗传图谱;其中,表示男性携带者,表示女性携带者,
●
表示女性患者,
↗
表示先证者;
[0040]
图8显示利用sanger测序检测1号家系itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点基因型的结果图,其中,b层和c层:1号家系中突变者;a层:1号家系中基因型为野生型(测序图中箭头所指为突变发生位置);
[0041]
图9显示利用sanger测序检测1号家系itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*位点基因型的结果图,其中,a层和c层:1号家系中突变者;b层:1号家系中基因型为野生型(测序图中箭头所指为突变发生位置);
具体实施方式
[0042]
本发明提供了itga2b基因突变体,所述itga2b基因突变体与野生型itga2b基因相比包括c.1156c》t突变。
[0043]
本发明野生型itga2b基因的cdna序列参见genbank登录号为nm_000419.5的序列。本发明所述c.1156c》t突变指野生型itga2b基因第12号外显子的第1156位上的碱基由c突变为t碱基,形成itga2b基因突变体。
[0044]
本发明还提供了上述技术方案所述的itga2b基因突变体编码的itga2b突变体蛋白,所述itga2b突变体蛋白与野生型itga2b蛋白相比包括p.r386*突变。本发明所述itga2b突变体蛋白中的p.r386*突变是由c.1156c》t突变引起的。
[0045]
本发明提供了导致血小板无力症的itga2b基因复合突变体,所述itga2b基因复合突变体包括复合杂合突变,所述复合杂合突变包括上述技术方案所述的c.1156c》t突变和c.2333a》c突变。
[0046]
本发明针对一例血小板无力症家系(其中1号家系包括先证者、先证者父亲和母亲)通过全外显子测序、家系分析联合sanger测序验证的方法对此家系进行致病变异检测和验证。在itga2b基因确定了新的复合杂合突变,包括新发现的c.1156c》t突变和现有的c.2333a》c突变,c.1156c》t突变和c.2333a》c突变分别来自患者父源和母源的等位基因,二者组成新的复合杂合突变,可以导致血小板无力症的发生。本发明首次发现了itga2b基因上c.1156c》t突变,并确认了将c.1156c》t突变和c.2333a》c突变组成的复合杂合突变与血小板无力症的密切关系,可用于血小板无力症的分子遗传学研究和血小板无力症相关疾病的诊断。
[0047]
本发明所述c.2333a》c突变指野生型itga2b基因第23号染色体上的第2333位a突变为c,该突变可能导致所编码的蛋白质第778位氨基酸残基由谷氨酰胺变为脯氨酸。本发明所述c.2333a》c突变与首次发现的c.1156c》t突变形成复合杂合突变,进而形成本发明中itga2b基因复合突变体。通过检测受试者是否携带有上述复合杂合突变,能够筛查或诊断
血小板无力症致病基因突变携带者或患者,以提供优生优育和治疗干预指导。特别地,本发明所提供的诊断试剂盒可用于快速、有效地预测或诊断血小板无力症。另一方面,本发明为血小板无力症的发病机制研究奠定了重要基础,为血小板无力症患者的治疗提供全新的理论依据。第三方面,本发明可以为治疗血小板无力症提供可能的药物靶点。
[0048]
本发明还提供了上述技术方案所述的itga2b基因复合突变体编码的itga2b复合突变体蛋白,所述itga2b复合突变体蛋白包括上述技术方案所述的p.r386*突变和p.q778p突变。本发明所述itga2b复合突变体蛋白中的p.q778p突变由c.2333a》c突变引起;与由c.1156c》t突变引起的所述的p.r386*突变组成本发明中的itga2b复合突变体蛋白。
[0049]
本发明还提供了上述技术方案所述的itga2b基因复合突变体或所述的itga2b复合突变体蛋白作为检测靶点在制备下述试剂盒中的应用:ⅰ:血小板无力症诊断试剂盒;ⅱ:血小板无力症筛查试剂盒;ⅲ:血小板无力症产前诊断试剂盒;ⅳ:血小板无力症产前筛查试剂盒;
ⅴ
:血小板无力症孕前诊断试剂盒;ⅵ:血小板无力症孕前筛查试剂盒;ⅶ:辅助防治血小板无力症的试剂盒。本发明通过检测生物样本中是否含有所述itga2b基因复合突变体,可以有效检测生物样本是否患有血小板无力症,或是否易患血小板无力症。本发明通过检测所述含有itga2b复合突变体蛋白在生物样本中是否表达,可以有效确证生物样本中是否患有血小板无力症,或是否易患血小板无力症。
[0050]
本发明还提供了一种用于检测上述技术方案所述的itga2b基因复合突变体或所述的itga2b复合突变体蛋白的试剂,所述试剂包括引物、探针、抗体和质谱检测试剂中的至少一种,进一步优选包括引物和/或探针,更优选包括引物。
[0051]
本发明还提供了一种用于检测上述技术方案所述的itga2b基因复合突变体的引物组,所述引物组包括检测所述c.1156c》t突变的引物对itga2b-1和检测所述c.2333a》c突变的引物对itga2b-2;所述引物对itga2b-1的上游引物itga2b-1f的核苷酸序列如seq id no.1所示,所述引物对itga2b-1的下游引物itga2b-1r的核苷酸序列如seq id no.2所示;所述引物对itga2b-2的上游引物itga2b-2f的核苷酸序列如seq id no.3所示,所述引物对itga2b-2的下游引物itga2b-2r的核苷酸序列如seq id no.4所示。
[0052]
本发明所述seq id no.1~4的核苷酸序列具体如下:seq id no.1:5
’‑
cagatggcgtcgtatttt-3’;seq id no.2:5
’‑
ccagtctcccaccaagtc-3’;seq id no.3:5
’‑
ggctgaggcaggagaatag-3’;seq id no.4:5
’‑
tggatgctgaggtgaagac-3’。
[0053]
本发明还提供了一种用于诊断和/或筛查血小板无力症的试剂,所述试剂包括上述技术方案所述的试剂。本发明所述试剂优选还包括测序引物和扩增所需要的试剂;所述测序引物优选包括所述c.1156c》t突变的测序引物itga2b-seq1和所述c.2333a》c突变的测序引物itga2b-seq2;所述测序引物itga2b-seq1的上游引物itga2b-seq1f的核苷酸序列优选如seq id no.5所示,所述测序引物itga2b-seq1的下游引物itga2b-seq1r的核苷酸序列优选如seq id no.6所示;所述测序引物itga2b-seq2的上游引物itga2b-seq2f的核苷酸序列优选如seq id no.7所示,所述测序引物itga2b-seq2的下游引物itga2b-seq2r的核苷酸序列优选如seq id no.8所示。本发明所述seq id no.5~8的核苷酸序列具体如下:seq id no.5:5
’‑
gccctctgtctccctttcc-3’;seq id no.6:5
’‑
tctccactcagcaccccat-3’;seq id no.7:5
’‑
ccctgtttctcctcatcccc-3’;seq id no.8:5
’‑
ggggagcttagcgcctc-3’。
[0054]
本发明所述pcr扩增所需要的试剂优选包括但不限于dntp,pcr缓冲液,镁离子和
tap聚合酶。本发明所述pcr缓冲液优选为10
×
pcr缓冲液,具体包括500mmol/lkcl,100mmol/l tris-cl(ph 8.3)和15mmol/lmgcl2。本发明所述试剂中优选还包括dna测序用试剂。本发明对所述dna测序用试剂的类型没有特殊限定,采用本领域中常规dna测序用试剂即可。本发明所述试剂中的测序引物能够对扩增所述itga2b基因复合突变体的引物组的扩增产物进行测序,从而判断itga2b基因上是否存在c.1156c》t突变和c.2333a》c突变,快速精准诊断血小板无力症。
[0055]
本发明还提供了上述技术方案所述的试剂在制备诊断、筛查和辅助防治血小板无力症的任意一种或多种试剂盒中的应用。本发明所述试剂盒具体优选包括ⅰ:血小板无力症诊断试剂盒;ⅱ:血小板无力症筛查试剂盒;ⅲ:血小板无力症产前诊断试剂盒;ⅳ:血小板无力症产前筛查试剂盒;
ⅴ
:血小板无力症孕前诊断试剂盒;ⅵ:血小板无力症孕前筛查试剂盒;ⅶ:辅助防治血小板无力症的试剂盒。
[0056]
本发明还提供了一种检测血小板无力症的方法,包括如下步骤:采用所述itga2b基因突变体的引物对对待测样本dna进行扩增,将扩增得到的产物进行测序和比对,结果判定。
[0057]
本发明对待测样本dna的获取方法没有特殊限定,采用本领域中常规dna提取方法即可。本发明所述致病基因突变体的引物对优选与上述技术方案相同,不再进行赘述。本发明对扩增、测序和比对的步骤和具体过程没有特殊限定,采用本领域中常规方式即可。本发明所述待测样本dna的来源优选为血液或羊水。本发明所述结果判定优选包括:如果发现itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点的基因型是“c.2333a》c杂合突变+c.1156c》t杂合突变”,则判断itga2b基因存在复合杂合突变,个体为患者;若两位点的基因型为“c.2333a》c纯合突变”+“c.1156c野生型”或“c.2333a野生型”+“c.1156c》t纯合突变”或“c.2333a》c纯合突变”+“c.1156c》t纯合突变”或“c.2333a》c纯合突变”+“c.1156c》t杂合突变”或“c.2333a》c杂合突变”+“c.1156c》t纯合突变”,个体也为患者;若两位点的基因型是“c.2333a》c杂合突变”或“c.1156c》t杂合突变”,则判断itga2b基因存在单个杂合突变,个体是携带者;若位点的基因型是“野生型”,则判断itga2b基因为野生型,个体是正常人。
[0058]
为了进一步说明本发明,下面结合附图和实施例对本发明提供的技术方案进行详细地描述,但不能将它们理解为对本发明保护范围的限定。
[0059]
下列实施例中未注明具体条件的实验方法,通常按照常规条件如sambrook等人,分子克隆实验室手册(第三版;molecular cloning a laboratory manual 1second edition;new york:cold spring harbor laboratorypress,2014)中所述的条件,或按照制造厂商所建议的条件。
[0060]
实施例1样本获取
[0061]
发明人发现了一个血小板无力症家系(简称1号家系),该1号家系部分成员的临床信息见表2。图1显示了itga2b基因突变1号家系图谱,其中,表示男性携带者,表示女性携带者,
■
表示男性患者,
↗
表示先证者。
[0062]
1.诊断标准:
[0063]
可参照《人类单基因遗传疾病》2010年版。
[0064]
血小板无力症患者主要表现为不同程度的出血,皮肤黏膜出血多见,除此之外还可表现为鼻衄、齿龈出血、胃肠道出血、颅内出血、拔牙后出血、女性月经增多等。血小板无
力症患者的临床表现具有异质性,表现在发病年龄、出血部位、严重程度和对治疗反应不同等方面。以往根据血小板表面gpⅱb和gpⅲa的表达情况和功能,血小板无力症被分为3型:
[0065]
表1血小板无力症分型
[0066][0067]
表2血小板无力症1号家系成员的临床信息
[0068][0069]
如图1所示,编号采用ⅰ(第一代)、ⅱ(第二代)。
[0070]
1号家系人员ⅰ:1、ⅰ:2、ⅱ:1外周血dna用于测序。
[0071]
实施例2外显子测序
[0072]
1.仪器设备如表3所示。
[0073]
表3仪器设备一览表
[0074][0075][0076]
2.试剂耗材
[0077]
人类全外显子测序试剂盒(agilent)、dna 1000试剂盒(agilent)、96孔板(axygen)、不同型号枪头(axygen)、200μl离心管(eppendorf)、1.5ml离心管(eppendorf)、毛细管电泳缓冲液(thermo)、测序标准物(thermo)、无水乙醇(thermo)、bigdye terminator v3.1(thermo)、外周血gdna提取试剂盒(tiangen)、琼脂糖(tiangen)、eb染液(amresco)。
[0078]
3.试剂配方
[0079]5×
tbe电泳液贮存液按照表4配制。
[0080]
表4 5
×
tbe电泳液配方
[0081]
试剂体积/重量tris5.4g硼酸750.0mgedta(ph8.0,0.5mol/l)2.0mlddh2o90.0ml
[0082]
用ddh2o将最终体积调整为100ml。
[0083]
0.5
×
tbe电泳液工作液,用ddh2o稀释10倍即可。
[0084]
10
×
红细胞裂解液按照表5配制。
[0085]
表5 10
×
红细胞裂解液配方
[0086]
试剂体积/重量nh4cl82.9gkhco310.0gedta0.37g加dh2o至1000ml
[0087]
高压灭菌,4℃保存。
[0088]1×
细胞核裂解液按照表6配制。
[0089]
表6 1
×
细胞核裂解液配方
[0090]
试剂体积/重量2mtris-hcl,ph8.20.5ml4m nacl10ml2mm edta0.4ml
[0091]
4.实验步骤
[0092]
签署知情同意书后,采集家系中ⅰ:1、ⅰ:2、ⅱ:1成员的外周血3-5ml作为研究样品。
[0093]
4.1样本dna提取
[0094]
1)将外周血3-5ml装入15ml离心管中,加2~3倍体积的1
×
红细胞裂解液,混匀,冰上静置30分钟,直至溶液变透明。
[0095]
2)4℃,3000转/分钟离心10分钟,小心去上清液。沉淀中加1ml 1
×
细胞核裂解液,混匀,再加2ml 1
×
细胞核裂解液和150μl 20%sds,摇匀,至出现粘稠透明状。加10μl 20mg/ml蛋白酶k,摇匀。37℃消化6小时以上或过夜。
[0096]
3)加等体积饱和酚,轻摇混匀,室温3000转/分钟离心10分钟。
[0097]
4)小心移上清至另一离心管,加酚和氯仿混合液混匀,酚:氯仿的体积比是1:1,室温3000转/分钟离心10分钟。
[0098]
5)小心移上清,若上清不清亮透明,则用等体积氯仿再抽提一次。
[0099]
6)将上清移入另一离心管中,加二倍体积无水乙醇,摇匀,见白色絮状dna。用火焰灭菌的玻璃钩针将dna钩出,70%乙醇洗二次,室温干燥5分钟,再将dna溶于200μl 1
×
te中,转鼓溶解过夜。紫外测od值。
[0100]
7)te溶解的dna,在4℃下可保存一年,如要求长期保存,则需加2倍体积无水乙醇置-70℃保存。
[0101]
4.2外显子测序
[0102]
参考人类全外显子测序试剂盒(agilent)说明书和分子克隆实验室手册(第三版;molecular cloning a laboratory manual 1second edition;new york:cold spring harbor laboratorypress,2014)操作指南。
[0103]
1)取2μg dna,机械打断,使片段大小在200bp左右,切胶回收150-250bp片段;
[0104]
2)dna片段做末端修复和3’末端加a;
[0105]
3)连接测序接头,对连接产物进行纯化,再行pcr扩增,扩增产物纯化;
[0106]
4)agilent试剂盒探针加入纯化后的扩增产物进行杂交捕获,杂交产物经洗脱回收后做pcr扩增,再行最终产物回收,取小样行琼脂糖凝胶电泳进行质控分析;
[0107]
5)nextseq500测序仪测序和数据分析。
[0108]
4.3结果
[0109]
最终得到具有致病意义的基因复合杂合突变itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*,分别来自患者的父源和母源的等位基因;其中c.1156c》t的突变为首次发现,该突变可能导致所编码的蛋白质第386位氨基酸由精氨酸变为终止密码子;另c.2333a》c的突变为曾经发现过的突变,该突变可能导致所编码的蛋白质第778位氨基酸残基由谷氨酰胺变为脯氨酸;在1号家系患者个体中itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点的基因型是“c.2333a》c杂合突变+c.1156c》t杂合突变”的复合杂合突变,在家系携带者个体中两位点的基因型是“c.2333a》c杂合突变”或“c.1156c》t杂合突变”的单个杂合突变。
[0110]
实施例3 sanger测序验证
[0111]
对于外显子组测序结果进一步利用sanger测序法,对itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点进行验证。分别对实施例1中的1号家系3名人员(先证者、先证者父亲、先证者母亲)和100名家系外正常人进行itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点基因型检测。
[0112]
具体方法步骤如下:
[0113]
1、dna提取
[0114]
按照实施例2的方法提基因组dna。
[0115]
2、候选引物设计、验证及优选
[0116]
2.1候选引物设计参考人类基因组序列数据库hg19/build36.3。
[0117]
2.2针对旧突变位点c.2333a》c和新发现突变位点c.1156c》t分别设计15对候选引
物(见表7和表8),并利用pcr实验来验证和评价各对候选引物的优劣情况。
[0118]
表7 c.1156c》t各对候选引物基本情况和验证实验结果一览表
[0119]
[0120][0121]
表8 c.2333a》c各对候选引物基本情况和验证实验结果一览表
[0122]
[0123]
[0124][0125]
注:正常pcr扩增结果电泳后只有一条特异性条带,若出现引物二聚体条带、非特异产物条带均是引物异常反应的结果;目标引物尽可能避免这类情况。
[0126]
2.3候选引物pcr验证反应
[0127]
按照表9中的反应体系进行pcr并保持反应体系在冰上;每对引物设置8个反应测试管(表9中序号1至8)。
[0128]
表9引物检测pcr反应体系
[0129]
[0130][0131]
反应条件:将上述测试反应管放入pcr仪,执行以下反应程序:
[0132]
第一步:95℃,5min;第二步:30个循环(95℃,30sec
→
tm,30sec
→
72℃,60sec);(根据表6中各引物tm值设置pcr扩增参数,如为双引物则取tm平均值);第三步:72℃,7min;第四步:4℃直至取样时。
[0133]
2.4候选引物pcr结果进行琼脂糖凝胶电泳检测,以评估引物反应的有效性、特异性:
[0134]
1)用胶带将洗净干燥的凝胶成样器两端封好,置于一水平台面上,在成样器的一端约1cm处放置梳子。
[0135]
2)称量2g琼脂粉末于一锥形瓶中,加入100ml 0.5
×
tbe电泳缓冲液,摇匀后置微波炉或电炉上(加石棉网)加热,沸腾后取出摇匀,再加热,直至凝胶完全熔解,取出室温冷却。
[0136]
3)待凝胶冷却至50℃左右,倒入封好的凝胶成样器,使厚度在5mm左右。
[0137]
4)凝胶凝固拆除胶带,将凝胶与成样器一起放入电泳槽中。
[0138]
5)加入电泳缓冲液,使液面高于胶面1~2mm,向上拔出梳子;用微量移液器将样品和dna大小标准品分别与载样液混匀后,加入各加样孔内,由于载样液中蔗糖比重较大,dna沉入孔底。
[0139]
6)盖上电泳槽,接通电源,调至适当电压,开始电泳。根据载样液中溴酚蓝的指示,判断样品的大概位置,决定是否终止电泳。
[0140]
7)切断电源,取出凝胶,放入0.5g/ml的eb水溶液中染色10~15分钟。
[0141]
8)将凝胶放到透射式紫外照射仪下观察结果,波长254nm,并用加红色滤色片的相机照相或用凝胶扫描系统记录电泳结果。
[0142]
2.5结果评价:
[0143]
1)如果7号管仅出现一条明亮清晰目的条带,无其它条带,则判断该对引物和发应体系有效性好和特异性强;
[0144]
2)如果7号管没有出现目的条带,则判断该对引物和反应体系无效;
[0145]
3)如果7号管出现目的条带外的引物引物二聚体带,并在2、3、4、5、6号部分管中也同样出现引物二聚体带,则判断该对引物和反应体系有效性差;
[0146]
4)如果7号管出现目的条带外的非特异性带,并在5、6号部分管中也同样出现非特异性带,则判断该对引物和反应体系特异性差;
[0147]
5)如果7号管出现目的条带外的引物二聚体和非特异性带,并在2、3、4、5、6号部分管中也同样出现引物二聚体和非特异性带,则判断该对引物和反应体系有效性和特异性差。
[0148]
2.6根据表7~8验证测试后统计的结果,选择其中最优一对(表7中seq id no.1和seq id no.2,表8中seq id no.3和seq id no.4)作为突变家系检测用引物。
[0149]
针对itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点的引物序列如下所示:5
’‑
ggctgaggcaggagaatag-3’(seq id no.3),5
’‑
tggatgctgaggtgaagac-3’(seq id no.4);
[0150]
针对新发现突变itga2b:nm_000419.5exon12:c.1156c》t:p.r386*位点的引物序列如下所示:5
’‑
cagatggcgtcgtatttt-3’(seq id no.1),5
’‑
ccagtctcccaccaagtc-3’(seq id no.2)。
[0151]
3、1号家系人员和100名家系外人员突变位点pcr扩增
[0152]
按照表10中的反应体系进行pcr并保持反应体系在冰上。分别以引物对itga2b-1和引物对itga2b-2对1号家系人员和100名家系外人员均进行扩增。
[0153]
表10突变位点pcr反应体系
[0154]
试剂体积10
×
pcr缓冲液2.0μl10mmol/l dntps0.4μl100ng/μl itga2b-1f(或itga2b-2f)0.5μl100ng/μl itga2b-1r(或itga2b-2r)0.5μl100ng/μl外周血抽提dna1.0μl5u/μl taq酶0.2μlddh2o15.4μl
[0155]
反应条件:将反应体系放入pcr仪,执行以下反应程序:针对c.2333a》c位点,反应程序为:第一步:95℃,5分钟;第二步:30个循环(95℃,30秒
→
54℃,30秒
→
72℃,60秒);第三步:72℃,7分钟;第四步:4℃直至取样时。
[0156]
针对c.1156c》t位点,反应程序为:第一步:95℃,5分钟;第二步:30个循环(95℃,30秒
→
52℃,30秒
→
72℃,60秒);第三步:72℃,7分钟;第四步:4℃直至取样时。
[0157]
4、琼脂糖凝胶电泳检测
[0158]
参照上述2.4步骤。
[0159]
5、pcr产物酶解法纯化:5μl pcr产物中分别加入0.5μl核酸外切酶i(exo i),1μl碱性磷酸酶(aip),37℃消化15分钟,85℃使酶失活15分钟。
[0160]
6、bigdye反应
[0161]
bigdye反应体系见表11。
[0162]
表11 bigdye反应体系
[0163][0164][0165]
测序pcr循环条件:第一步:96℃,1分钟;第二步:33个循环(96℃,30秒
→
55℃,15秒
→
60℃,4分钟);第三步:4℃直至取样时。
[0166]
7、bigdye反应产物纯化:
[0167]
1)每管加入1μl 125mm edta(ph 8.0),加到管底,再加入1μl 3mol/l naac(ph5.2);
[0168]
2)加入70μl 70%酒精,震荡混匀4次,室温放置15分钟;
[0169]
3)3000g,4℃离心30分钟;马上倒置96孔板,185g离心1分钟;
[0170]
4)室温放置5分钟,让残余的酒精在室温挥发干,加入10μl hi-di甲酰胺溶解dna,96℃变性4分钟,迅速置冰上4分钟,上机测序。
[0171]
8、测序
[0172]
将纯化后的bigdye反应产物进行dna测序,测序引物则在上述pcr优选引物的基础上设计巢式引物(第二组引物是在第一组引物扩增得到的产物序列范围内设计的)作为测序引物。
[0173]
针对itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点的测序引物序列如下所示:5
’‑
ccctgtttctcctcatcccc-3’(seq id no.7),5
’‑
ggggagcttagcgcctc-3’(seq id no.8);
[0174]
针对新发现突变位点itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*的测序引物序列如下所示:5
’‑
gccctctgtctccctttcc-3’(seq id no.5),5
’‑
tctccactcagcaccccat-3’(seq id no.6)。
[0175]
9、结果分析
[0176]
sanger测序结果显示,1号家系中1名患者itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点基因型是“c.2333a》c杂合突变+c.1156c》t杂合突变”的复合杂合突变;1号家系中2名携带者该位点的基因型分别是“c.2333a》c杂合突变”或“c.1156c》t杂合突变”的单杂合突变;100个无血缘关系的正常对照的itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点基因型是“野生型”。图2测序图中箭头所指位置a层和c层显示家系中个体itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点基因型是“c.2333a》c杂合突变”,图2中b层显示家系中个体itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点基因型是“野生型”。图3测序图中箭头所指位置b层和c层显示家系中个体itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*位
点基因型是“c.1156c》t杂合突变”,图3中a层显示家系中个体itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*位点基因型是“野生型”。
[0177]
实施例4血小板无力症诊断试剂盒及应用
[0178]
1、试剂盒组成:
[0179]
1)扩增引物:如实施例3中表7中seq id no.1和seq id no.2和表8中seq id no.3和seq id no.4所示的序列,2)缓冲液:10
×
pcr缓冲液具体组分为:500mmol/lkcl,100mmol/ltris-cl(ph8.3),15mmol/lmgcl2,3)taq酶,4)dntps,5)itga2b:c.2333a》c和c.1156c》t阳性突变参考品dna,c.2333a》c阳性参考品为一段双链dna,具体序列如下所示:ggctgaggcaggagaatagcttgaaccgaacctgggaggtggaggttgcagtgagctgagattgggccactgcactccagccttccagcctgggcgacagtgcgagattctatctcaaaagaaaaaaaaaaaggtctttgaagaagcctggttccctttcttcctcagagatttatgtctgagtcttggagccctagaggaagttctttcccaggtctaacttcagtgtggcatgctctttgtataattagctctctctgaactctctaaaattctggcctcacccccagaaagtcactgggctggtgtccctggccctgtttctcctcatcccctcccctctagcaagaacagccagaatccaaacagcaagattgtgctgctggacgtgccggtccgggcagaggccccagtggagctgcgagggtgagaggccaggggtggagaagggagatggcattcagggctctaaactccagggggcgctggggaaacctcacaggccaatcagggcatcacactctctctgggggtcttgggcacctgcaggaactcctttccagcctccctggtggtggcagcagaagaaggtgagagggagcagaacagcttggacagctggggacccaaagtggagcacacctatgaggtattggggagcctcgcgtccctggctggggtgagcgggtcctcagaactccgggtgaggcgctaagctccccacaccctgccaccaccaccccttcagctccacaacaatggccctgggactgtgaatggtcttcacctcagcatcca(seq id no.65)
[0180]
c.1156c》t阳性参考品为一段双链dna,具体序列如下所示:
[0181]
cagatggcgtcgtattttgggcattcagtggctgtcactgacgtcaacggggatgggtgaggagggacatgccccacccctacccagttgggtcccaaattaccagagctgccctctgtctccctttcctagccctagtctcacgtatccactggaggaacaggagagcaagggtcgaggagatttggccctagccccaatatacccctggtccagtcccatgtaaccactcatctggcccacaggaggcatgatctgctggtgggcgctccactgtatatggagagccgggcagaccgaaaactggccgaagtggggcgtgtgtatttgttcctgcagccgcgaggcccccacgcgctgggtgcccccagcctcctgctgactggcacacagctctatgggtgattcggctctgccatcgcacccctgggcgacctcgaccgggatggctacaatggtgagggaagagaggagccctacttgctgcagaggggttaacagccactcaaaaagcatggagttggcctgagggcagccagaaccaggatgggttttaagcatataagtatgtggcttagacacatggggtgctgagtggagagcagatgggagagttgaagactaattaggaagtgtttgccttaatccaagcaagagacaatgaccacctggatgtggattttggcagtggagttagagatgggagtgacttcacagatatttaggactcggattattaggacttggtgggagactgg(seq id no.66),6)测序引物:如实施例3所示。
[0182]
2、使用方法:
[0183]
应用于2号家系患者检测(见表12)。
[0184]
表12血小板无力症2号家系成员的临床信息
[0185][0186]
如图4和图7所示,编号采用ⅰ(第一代)、ⅱ(第二代)。其中,表示男性携带者,表示女性携带者,
■
表示男性患者,
◇
表示胎儿,
↗
表示先证者患者。
[0187]
2号家系人员ⅰ:1、ⅰ:2、ⅱ:1外周血dna和ⅱ:2羊水dna用于该试剂盒检测;
[0188]
3号家系人员ⅰ:1、ⅰ:2和ⅱ:1外周血dna用于该试剂盒检测。
[0189]
1)基因组dna提取:提取样本基因组dna;
[0190]
2)先采用上述itga2b-1和itga2b-2pcr扩增引物、taq酶、缓冲液、dntps、样本基因组dna等进行pcr扩增反应;
[0191]
3)对pcr扩增产物进行纯化;
[0192]
4)采用上述测序引物对纯化的pcr产物进行bigdye反应;
[0193]
5)对biydye反应产物纯化;
[0194]
6)对biydye反应产物测序,测序序列与正常序列相比较。
[0195]
试剂盒检测结果显示,2号家系中先证者itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点基因型是“c.2333a》c杂合突变+c.1156c》t杂合突变”的复合杂合突变。图5测序图中箭头所指位置显示家系中先证者、先证者母亲和胎儿itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点基因型是“c.2333a》c杂合突变”杂合突变,先证者父亲为野生型;图6测序图中箭头所指位置显示家系中先证者、先证者父亲和胎儿itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*位点基因型是“c.1156c》t杂合突变”,先证者母亲为野生型;图5和图6结果提示胎儿同先证者一样为血小板无力症患者,遗传咨询后先证者父母双方自主决定是否终止妊娠。
[0196]
试剂盒检测结果显示,3号家系中先证者itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p和exon12:c.1156c》t:p.r386*位点基因型是“c.2333a》c杂合突变+c.1156c》t杂合突变”的复合杂合突变。图8测序图中箭头所指位置显示家系中先证者和先证者母亲itga2b:nm_000419.5:exon23:c.2333a》c:p.q778p位点基因型是“c.2333a》c杂合突变”杂合突变,先证者父亲为野生型;图9测序图中箭头所指位置显示家系中先证者和先证者父亲itga2b:nm_000419.5:exon12:c.1156c》t:p.r386*位点基因型是“c.1156c》t杂合突变”,先证者母亲为野生型;图8和图9结果提示胎儿同先证者一样为血小板无力症患者,其母亲和父亲为突变基因携带者;遗传咨询意见为该夫妻再生育血小板无力症患者的几率是1/4,生育携带者后代的几率是1/2,生育完成正常个体的几率是1/4,建议夫妻计划再生育时行胚胎植入前遗传学诊断以及妊娠后来医院行产前诊断。
[0197]
由以上实施例可以得出:本发明确认了新的itga2b基因复合突变体,即包括c.1156c》t突变和c.2333a》c突变,且确认了新突变体与血小板无力症的发病密切相关,所述基因突变体可用于血小板无力症的分子诊断及与相关疾病的鉴别诊断。
[0198]
尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例,而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其他实施例,这些实施例都属于本发明保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1