一种大柴胡汤HPLC特征图谱构建方法及含量测定方法与流程
一种大柴胡汤hplc特征图谱构建方法及含量测定方法
技术领域
1.本发明属于中药分析检测领域,具体涉及一种大柴胡汤hplc特征图谱构建方法及含量测定方法。
背景技术:
2.大柴胡汤方出自张仲景的《伤寒杂病论》,由柴胡、黄芩、芍药、半夏、生姜、枳实、大枣、大黄组成,具有和解少阳,内泻热结之功。在中医的理论里,少阳包括胆与三焦,若少阳受邪,枢机不利,肝胆气机郁滞,必然影响三焦气化功能,若肝失疏泄,横逆犯胃,因而出现胸胁苦满,或胁下痞硬,或腹中痛等症,若伤及脾胃,气机壅塞,土壅木郁,燥热与糟粕互结,积于胃肠,阻滞腑气通降,可引起腹胀满而大便秘结等证候。由于少阳三焦为通行元气和运行水谷之要道,若邪热壅滞胆腑,上不得越,下不得泄,胆热木郁,克脾犯胃,胃失和降,可出现呕吐、泛酸、腹胀痛、纳差等病证。
3.方中柴胡专入少阳、疏邪透表为君药,黄芩擅清少阳之郁热,与柴胡同用,能和解少阳,是为少阳病未解、往来寒热、胸胁苦满而设;少用大黄泻热通腑,枳实行气破结,二者相配,可内泻热结,是为“热结在里”之心下痞满硬痛、大便不解、呕不止、郁郁微烦而设;芍药缓急止痛,配大黄可治腹中实痛,伍枳实能调和气血,协柴胡、黄芩清肝胆之热,以防木乘中土;半夏和胃降逆,生姜重用则止呕之功更著,以治呕逆不止;大枣和中益气,合芍药酸甘化阴,既可防热邪入里伤阴之虞,又能缓和枳实、大黄泻下伤阴之弊。总之,本方配伍体现了和解及攻下两法的结合运用,但以和解少阳为主、泻下之力较缓。
4.大柴胡汤在临床应用广泛,疗效稳定清晰,但其具体的功效物质基础尚不明确。大柴胡汤临床常用药效为保肝、利胆、抗炎、降糖、降脂;现代药理研究也表明大柴胡汤具有保肝、降糖、降脂、利胆、抗炎的作用。但是,目前尚无大柴胡汤的标准质量检测方法,部分生产相关产品的药企的企业质量标准方法中仅采用薄层色谱法(tlc)或高效液相色谱法(hplc)对大柴胡汤方剂中几个含量较高的有效成分进行定性或定量检测。大柴胡汤全方成分复杂,由8味中药组成,仅以两三个成分的检测结果无法全面表征处方的物质基础,难以全面控制大柴胡汤的内在质量。
技术实现要素:
5.为了解决上述技术问题,有必要提供一种能够更全面地表征大柴胡汤的内在质量的大柴胡汤hplc特征图谱构建方法和含量测定方法。
6.具体地,通过以下几个方面的技术方案实现了本发明:
7.在第一个方面中,本发明提供了一种大柴胡汤hplc特征图谱构建方法,其特征在于:所述大柴胡汤由柴胡、黄芩、芍药、半夏、生姜、枳实、大枣和大黄制成,所述hplc特征图谱构建方法包括以下步骤:
8.(1)将大柴胡汤制成供试品溶液:
9.将大柴胡汤标准煎液定容于1000ml容量瓶中,精密量取1ml,置10ml的容量瓶内,
加入一定量有机溶剂,摇匀,超声提取10min,静置,放冷,用有机溶剂定容至刻度线,摇匀,过0.22μm微孔滤膜,取续滤液,即得供试品溶液,同法制备单味药及阴性对照水煎液供试品;
10.(2)制备对照品溶液:
11.精密称取芍药苷对照品11.30mg、柚皮苷对照品11.26mg、橙皮苷11.30mg、新橙皮苷10.90mg、黄芩苷11.55mg、汉黄芩苷5.30mg、柴胡皂苷b
2 5.36mg、黄芩素4.80mg置于10ml容量瓶内,加有机溶剂使溶解并定容摇匀,作为储备液,精密移取上述储备液各1ml,置10ml容量瓶中,有机溶剂定容,摇匀,即得混合对照品溶液;
12.以及,(3)对所述供试品溶液和所述对照品溶液进行hplc检测,得到具有共有特征峰的所述大柴胡汤hplc特征图谱:
13.其中,hplc检测的色谱条件如下所示:采用ods-c
18
硅胶色谱柱,以a相乙腈和b相0.05%磷酸水溶液作为流动相,二极管阵列检测器,检测波长为230nm-280nm,流速1.0ml
·
min-1
,柱温:25-35℃,进样体积10μl。
14.作为可选方式,在上述hplc特征图谱构建方法中,所述大柴胡汤标准煎液采用以下方法制备:大柴胡汤遵古煎煮,加水2400ml,40min武火煮至沸腾转文火煎煮110min,获得1200ml煎液,去渣滓后文火煎煮180min,最终得到600ml大柴胡汤标准煎液,所述大柴胡汤由北柴胡110.4g、黄芩41.4g、白芍41.4g、大黄27.6g、生姜69.0g、姜半夏60.0g、麸炒枳实58.3g和大枣55.2g制成。
15.作为可选方式,在上述hplc特征图谱构建方法中,在步骤(1)和步骤(2)中的有机溶剂为甲醇,且在步骤(2)中的对照品芍药苷、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、柴胡皂苷b2和黄芩素是针对大柴胡汤和解少阳内泻热结功效的药效标志物(q-markers)。
16.作为可选方式,在上述hplc特征图谱构建方法中,在步骤(3)中采用的洗脱方式为梯度洗脱,洗脱条件为:0-5min,3%-3%a;5-10min,3%-10%a;10-15min,10%-12%a;15-25min,12%-16%a;25-30min,16%-16%a;30-50m in,16%-20%a;50-55min,20%-20%a;55-75min,20%-25%a;75-85min,25%-46%a;85-90min,46%-85%a;90-100mi n,85%-85%a。
17.作为可选方式,在上述hplc特征图谱构建方法中,在步骤(3)中,使用的色谱柱为ods-c
18
色谱柱,规格为4.6
×
250mm,5μm,检测波长为240nm,柱温为30℃。
18.在第二个方面中,本发明提供了一种大柴胡汤指标性活性成分的含量测定方法,所述大柴胡汤由柴胡、黄芩、芍药、半夏、生姜、枳实、大枣和大黄制成,所述含量测定方法包括以下步骤:
19.(1)将大柴胡汤制成供试品溶液:
20.将大柴胡汤标准煎液定容于1000ml容量瓶中,精密量取1ml,置10ml的容量瓶内,加入一定量有机溶剂,摇匀,超声提取10min,静置,放冷,用有机溶剂定容至刻度线,摇匀,过0.22μm微孔滤膜,取续滤液,即得供试品溶液,同法制备单味药及阴性对照水煎液供试品;
21.(2)制备对照品溶液:
22.精密称取芍药苷对照品11.30mg、柚皮苷对照品11.26mg、橙皮苷11.30mg、新橙皮
苷10.90mg、黄芩苷11.55mg、汉黄芩苷5.30mg、柴胡皂苷b
2 5.36mg、黄芩素4.80mg置于10ml容量瓶内,加有机溶剂使溶解并定容摇匀,作为储备液,精密移取上述储备液各1ml,置10ml容量瓶中,有机溶剂定容,摇匀,即得混合对照品溶液;
23.以及,(3)对所述供试品溶液和所述对照品溶液进行hplc检测,以测定大柴胡汤指标性活性成分的含量:
24.其中,hplc检测的色谱条件如下所示:采用ods-c
18
硅胶色谱柱,以a相乙腈和b相0.05%磷酸水溶液作为流动相,二极管阵列检测器(dad),检测波长为230nm-280nm,流速1.0ml
·
min-1
,柱温:25-35℃,进样体积10μl。
25.作为可选方式,在上述含量测定方法中,所述大柴胡汤标准煎液采用以下方法制备:大柴胡汤遵古煎煮,加水2400ml,40min武火煮至沸腾转文火煎煮110min,获得1200ml煎液,去渣滓后文火煎煮180min,最终得到600ml大柴胡汤标准煎液,所述大柴胡汤由北柴胡110.4g、黄芩41.4g、白芍41.4g、大黄27.6g、生姜69.0g、姜半夏60.0g、麸炒枳实58.3g和大枣55.2g制成。
26.作为可选方式,在上述含量测定方法中,在步骤(1)和步骤(2)中的有机溶剂为甲醇,且在步骤(2)中的对照品芍药苷、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷、柴胡皂苷b2和黄芩素是针对大柴胡汤和解少阳、内泻热结功效的药效标志物(q-markers)。
27.作为可选方式,在上述含量测定方法中,在步骤(3)中采用的洗脱方式为梯度洗脱,洗脱条件为:0-5min,3%-3%a;5-10min,3%-10%a;10-15min,10%-12%a;15-25min,12%-16%a;25-30min,16%-16%a;30-50min,16%-20%a;50-55min,20%-20%a;55-75min,20%-25%a;75-85min,25%-46%a;85-90min,46%-85%a;90-100min,85%-85%a。
28.作为可选方式,在上述含量测定方法中,其特征在于:在步骤(3)中,使用的色谱柱为ods-c
18
色谱柱,规格为4.6
×
250mm,5μm,检测波长如下所示:芍药苷230nm,柴胡皂苷b
2 254nm,柚皮苷、橙皮苷、新橙皮苷、黄芩苷、黄芩素和汉黄芩苷280nm,柱温为30℃。
29.本发明相对于现有技术,具有以下有益效果:
30.指纹图谱是当今国内外公认的能够较好反映中药内在质量和鉴别真伪的方法,通过建立药用植物指纹图谱,可以较全面的反映中药所含内在化学成分的种类和数量。
31.本发明建立了大柴胡汤hplc特征图谱,采用指纹图谱软件共标定出18个特征峰,相似度大于0.93,说明大柴胡汤的化学成分基本稳定,不同批次间的差异较小,生成的对照图谱具有很好的代表性,能够为大柴胡汤的质量评价提供依据。此外,本发明还以q-marke rs作为指标性成分建立了大柴胡汤的含量测定方法。
32.本发明在大柴胡汤质量检测和含量测定过程中首次引入q-markers概念,为大柴胡汤的质量研究提供了试验依据,为大柴胡汤提供了综合质量评价方法,为大柴胡汤质量内部管控和提升提供了保障,同时也对确保其临床疗效具有非常重要的意义。
附图说明
33.附图用来提供对本发明的进一步理解,并且构成说明书的一部分,与本发明的实施例一起用于解释本发明,并不构成对本发明的限制。在附图中:
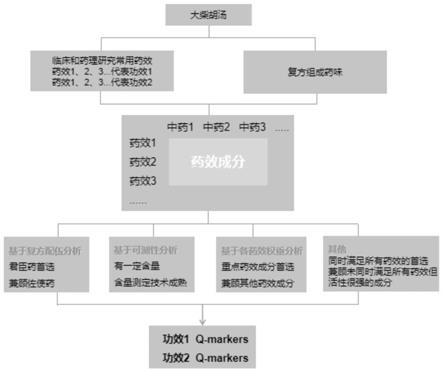
34.图1:大柴胡汤功效q-makers精准分析的流程图。
35.图2:大柴胡汤全方与单味药比较色谱图及特征峰归属。
36.图3:大柴胡汤全方特征峰归属(a)和大柴胡汤局部放大图(b)。
37.图4:大柴胡汤全方、阴性对照及各指标性成分对比。a.混标;b.全方;c.缺大黄;d.缺黄芩;e.缺柴胡;f.缺生姜;g.缺半夏;h.缺大枣;i.缺白芍;j.缺枳实;6.芍药苷;9.柚皮苷;10.橙皮苷;11.新橙皮苷;12.黄芩苷;14.黄芩素;15.汉黄芩苷;16.柴胡皂苷b2。
38.图5:15批大柴胡汤标准煎液及其对照特征图谱。s1-s15分别对应大柴胡汤批号p1-p15,r为对照特征图谱。
具体实施方式
39.下面参照具体的实施例对本发明做进一步说明。应当理解,此处所描述的具体实施例仅用于解释本发明,并不用于限定本发明的范围。
40.实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道购买得到的常规产品。
41.下面实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为市售产品。
42.实施例:
43.1.与大柴胡汤和解少阳内泻热结功效对应的q-markers的筛选
44.采用如图1中所示的流程对与大柴胡汤和解少阳内泻热结功效对应的q-markers进行筛选,结果如下表1所示。
45.表1:与大柴胡汤和解少阳内泻热结功效对应的q-markers
46.[0047][0048]
注:加粗的药效为关键药效;加粗的成分为q-markers。
[0049]
如表1中所示,根据q-markers筛选结果,将与大柴胡汤药效相关的主要活性物质柴胡皂苷b2、黄芩苷、黄芩素、汉黄芩苷、柚皮苷、新橙皮苷、橙皮苷和芍药苷作为hplc特征图谱构建和含量测定的对照品。
[0050]
2.供试品煎液的制备
[0051]
2.1大柴胡汤标准煎液的制备
[0052]
采用随机数表法对各饮片进行随机组合并排序,依次编号为p1-p15。将大柴胡汤遵古煎煮:加水2400ml,40min武火煮至沸腾转文火煎煮110min,获得1200ml煎液。去渣滓后文火煎煮180min,最终得到600ml煎液。按上述制备方法对大柴胡汤进行煎煮,即得15批大柴胡汤的标准煎液。
[0053]
其中,所述大柴胡汤由北柴胡110.4g、黄芩41.4g、白芍41.4g、大黄27.6g、生姜69.0g、姜半夏60.0g、麸炒枳实58.3g和大枣55.2g制成。
[0054]
2.2单味药和阴性对照水煎液的制备
[0055]
单味药和阴性对照水煎液的制备方法同2.1部分。
[0056]
3.大柴胡汤特征图谱的建立
[0057]
3.1色谱条件
[0058]
ods-c
18
色谱柱,规格4.6
×
250mm,5μm;流动相乙腈(a)-0.05%磷酸水(b);梯度洗脱(0-5min,3%-3%a;5-10min,3%-10%a;10-15min,10%-12%a;15-25min,12%-16%a;25-30min,16%-16%a;30-50min,16%-20%a;50-55min,20%-20%a;55-75min,20%-25%a;75-85min,25%-46%a;85-90min,46%-85%a;90-100min,85%-85%a);流速
1.0ml
·
min-1
;二极管阵列检测器,检测波长240nm;柱温:30℃;进样体积10μl。
[0059]
3.2供试品溶液的制备
[0060]
将大柴胡汤标准煎液定容于1000ml容量瓶中,精密量取1ml,置10ml的容量瓶内。加入一定量的纯甲醇,摇匀,超声提取10min(频率为40khz,功率300w),静置,放冷。用甲醇定容至刻度线,摇匀,过0.22μm微孔滤膜,取续滤液,即得供试品溶液。同法制备单味药及阴性对照水煎液供试品。
[0061]
3.3对照品溶液的制备
[0062]
精密称取芍药苷对照品11.30mg、柚皮苷对照品11.26mg、橙皮苷11.30mg、新橙皮苷10.90mg、黄芩苷11.55mg、汉黄芩苷5.30mg、柴胡皂苷b
2 5.36mg、黄芩素4.80mg置于10ml容量瓶内,加甲醇使溶解并定容摇匀,作为储备液。精密移取上述储备液各1ml,置10ml容量瓶中,甲醇定容,摇匀,即得混合对照品溶液。
[0063]
3.4大柴胡汤特征峰及指标成分归属
[0064]
对大柴胡汤煎液的特征图谱进行特征峰归属,全方及单味药特征图谱见图2,共归属了18个特征峰,见图3a和图3b。峰1、峰2、峰3、峰4、峰7、峰8、峰9(柚皮苷)、峰10(橙皮苷)、峰11(新橙皮苷)归属于麸炒枳实;峰5、峰6(芍药苷)归属于白芍;峰12(黄芩苷)、峰13、峰14(黄芩素)、峰15(汉黄芩苷)归属于黄芩;峰16(柴胡皂苷b2)、峰17归属于柴胡;峰18归属于大黄。此外,考虑到新橙皮苷其响应值高且出峰时间适中,因此将其作为参照峰。全方中指标性成分峰9(柚皮苷)、峰10(橙皮苷)、峰11(新橙皮苷)、峰6(芍药苷)、峰12(黄芩苷)、峰14(黄芩素)、峰15(汉黄芩苷)、峰16(柴胡皂苷b2)分离良好,且无阴性干扰,其对照品与全方、各药阴性对照见图4。
[0065]
3.5特征图谱的分析处理
[0066]
将特征图谱以cdf格式导入中药色谱指纹图谱相似度评价系统(2012a),对照图谱生成方法采用中位数法,时间窗宽度设置为0.2,进行全谱峰匹配,计算相似度,同时计算特征峰的相对保留时间和相对峰面积的rsd。
[0067]
3.6精密度考察
[0068]
取同一供试品溶液,按“3.1”项下色谱条件连续进样测定6次。特征图谱方法的精密度结果相似度>0.998,以11号峰为参照峰,各特征峰相对保留时间、相对峰面积rsd值均依次小于0.13%、3.7%,表明该仪器精密度良好。
[0069]
3.7重复性考察
[0070]
按照“3.2”项下平行制备6份大柴胡汤供试品溶液,按“3.1”项下色谱条件进样测定。特征图谱方法的重复性结果相似度>0.998,以11号峰为参照峰,各特征峰相对保留时间、相对峰面积rsd值均依次小于0.16%、4.7%,表明方法重复性良好。
[0071]
3.8稳定性考察
[0072]
取同一供试品溶液,在0h、2h、4h、8h、10h、12h、24h后按“3.1”项下色谱条件进样测定。特征图谱方法的稳定性结果相似度>0.995,以11号峰为参照峰,各特征峰相对保留时间、相对峰面积rsd值均依次小于0.17%、3.6%,表明该样品稳定性良好。
[0073]
3.9 15批大柴胡汤标准煎液的特征图谱测定
[0074]
将15批大柴胡汤标准煎液按“3.2”项下制备供试品溶液,依据“3.1”项下色谱条件进样,并参照“3.5”项下进行相似度评价。15批大柴胡汤的特征图谱见图5,相似度结果见表
2。15批大柴胡汤的特征图谱的相似度均大于0.93,说明大柴胡汤的化学成分基本稳定,不同批次间的差异较小,生成的对照图谱具有很好的代表性。各特征峰与峰11(新橙皮苷)峰面积的比值结果见表3,比值范围较窄。
[0075]
表2:15批大柴胡汤标准煎液特征图谱相似度
[0076]
[0077][0078]
4.大柴胡汤指标性成分含量测定
[0079]
如上述第1部分所述,将芍药苷、黄芩素、柴胡皂苷b2、柚皮苷、橙皮苷、新橙皮苷、
黄芩苷、汉黄芩苷确定为大柴胡汤指标性成分,对其进行含量测定。
[0080]
4.1色谱条件
[0081]
色谱条件除波长外均与“3.1”项下色谱条件一致。其在230nm下检测芍药苷、254nm下检测柴胡皂苷b2、280nm下检测柚皮苷、橙皮苷、新橙皮苷、黄芩苷、黄芩素、汉黄芩苷。
[0082]
4.2专属性考察
[0083]
取“3.2”项下的混合对照品溶液、供试品溶液、各阴性供试品溶液适量,按“3.1”项下色谱条件进样测定。结果表明,阴性供试品对指标性成分测定无干扰,且分离度良好。
[0084]
4.3线性关系考察
[0085]
精密吸取混合对照品溶液,用甲醇稀释为不同质量浓度的系列混合对照品溶液,按“3.1”项下色谱条件进样测定,记录峰面积。以峰面积(y)为纵坐标,进样不同浓度的量(x)为横坐标,进行线性回归,得回归方程,结果见表4。
[0086]
表4:大柴胡汤中8种成分线性关系考察结果
[0087][0088]
4.4精密度考察
[0089]
取同一供试品溶液,“按3.1项下”色谱条件,连续进样6次,记录峰面积,计算供试品中芍药苷、黄芩素、柴胡皂苷b2、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷峰面积的rsd分别为1.7%、0.27%、0.69%、0.48%、0.47%、0.46%、0.46%、0.56%,表明仪器精密度良好。
[0090]
4.5重复性考察
[0091]
按照“3.2”项下平行制备6份大柴胡汤供试品溶液,按“3.1”项下色谱条件进样测定,记录峰面积,计算供试品中芍药苷、黄芩素、柴胡皂苷b2、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷峰面积的rsd分别为0.76%、1.2%、0.94%、0.66%、0.82%、0.68%、0.75%、0.72%,表明该方法重复性良好。
[0092]
4.6稳定性考察
[0093]
取同一供试品溶液,在0h、2h、4h、8h、10h、12h、24h后按“3.1”项下色谱条件进样测定,记录峰面积,计算供试品中芍药苷、黄芩素、柴胡皂苷b2、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷峰面积的rsd分别为0.52%、1.0%、0.52%、0.19%、0.23%、0.16%、0.27%、0.33%,表明其成分在24h内含量稳定。
[0094]
4.7加样回收率考察
[0095]
按照“3.2”项下制备大柴胡汤煎液共6份,各对照品加入量与所取供试品中待测成分量之比为1∶1,按“3.1”项下色谱条件进样测定,计算芍药苷、黄芩素、柴胡皂苷b2、柚皮苷、橙皮苷、新橙皮苷、黄芩苷、汉黄芩苷回收率及rsd值,其平均回收率为99.69%、99.69%、104.15%、99.17%、102.56%、100.23%、102.76%、98.66%,rsd为1.1%、1.6%、
1.1%、1.9%、2.0%、1.9%、1.8%、1.8%,说明本方法准确度良好,符合要求。
[0096]
4.8样品含量测定结果
[0097]
取15批大柴胡汤样品,按“3.2”项下方法制备供试品溶液,按“3.1”项下色谱条件测定,计算煎液成分含量,结果见表5。
[0098]
表5:大柴胡汤标准煎液含量测定结果(mg
·
ml-1
)
[0099][0100]
结果表明,不同批次之间,含量存在一定差异。如白芍,安徽产地的芍药苷含量普遍较高;麸炒枳实产地为江西的柚皮苷、橙皮苷、新橙皮苷的含量较高;产地为河北的柴胡其柴胡皂苷b2含量较低;产地为内蒙古的黄芩其黄芩素和黄芩苷含量较高,而产地为山西的汉黄芩苷的含量较高。
[0101]
综上所述,本发明成功建立了大柴胡汤hplc特征图谱,采用指纹图谱软件共标定出18个特征峰,相似度大于0.93,说明大柴胡汤的化学成分基本稳定,不同批次间的差异较小,生成的对照图谱具有很好的代表性,能够为大柴胡汤的质量评价提供依据。此外,本发明以q-markers作为指标成功建立了大柴胡汤的含量测定方法。
[0102]
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1