改性HDL的定量方法以及用于该定量方法的分析用试剂
改性hdl的定量方法以及用于该定量方法的分析用试剂
技术领域
1.本发明涉及能够用于生活习惯病风险及其治愈效果的判定的改性hdl的定量方法以及用于该定量方法的分析用试剂。
背景技术:
2.hdl(high-density lipoprotein,高密度脂蛋白)是所谓的胆固醇的一种,比重高、粒径小。已知hdl负责从组织向肝脏的胆固醇的输送。若hdl在血中浓度较高,则使动脉硬化的风险降低,因此有时也通称为“有益胆固醇”。另一方面,比重低的ldl(low-density lipoprotein,低密度脂蛋白)作为“有害胆固醇”而已知。hdl和ldl的浓度被用作健康诊断的指标。
3.作为hdl的生理活性,不仅抑制ldl的氧化,而且通过no的增加等减轻由氧化ldl引起的细胞毒性,发挥抗动脉硬化效果。但是,在冠状动脉疾病患者中,血中改性hdl增加,其经由lox-1作用于血管,促进动脉硬化,在人的动脉硬化灶中,作为hdl的载脂蛋白的apoai改性而成的物质大量蓄积。由于这些结果,为了将hdl用作健康诊断的指标,不仅需要测定hdl的浓度,还需要分别对具有本来的生理活性的hdl和由于改性等而活性发生了变化的hdl进行定量。尤其是,认为如果能够对改性hdl进行定量,则能够用于包含上述冠状动脉疾病在内的、与循环系统以及血液相关的疾病及其风险的验证。
4.专利文献1公开了一种功能障碍hdl的测定方法,其为试样中所含的功能障碍hdl的测定方法,其中,使试样与功能障碍hdl的受体接触,使试样中的功能障碍hdl与受体结合,并对与受体结合的功能障碍hdl进行检测,受体为lox-1或其变体,受体固定化于载体,使对功能障碍hdl进行识别的抗体进一步与结合于受体的功能障碍hdl结合。该技术试图提供一种能够广泛检测多种分子形态的功能障碍hdl的功能障碍hdl测定技术,并且提供利用了该技术的生活习惯病的检测技术。
5.另外,本发明的发明人在专利文献2中公开了在与lox-1结合的lox-1结合蛋白序列上直接或经由间隔物连结有apoa1的全部蛋白序列或部分片段蛋白序列的融合蛋白以及使用了该融合蛋白的高密度脂蛋白的测定试剂盒。该技术通过测定由lox-1和抗apoa1抗体同时识别的hdl,能够测定接受了各种改性的hdl,以及使用如针对lox-1的抗体(抗lox-1抗体)的lox-1结合部位等那样使与lox-1特异性结合的蛋白质和apoa1融合而成的融合蛋白。通过该融合蛋白,能够同时识别接受了各种改性的hdl,用于测定受体结合活性并测定生理活性本身,因此想要得到不含脂质、能够长期保存、能够再现性地进行调整、能够降低各个测定试验间的偏差而提高可靠性的可成为参考的融合蛋白。现有技术文献专利文献
6.专利文献1:日本特许第6231307号公报专利文献2:日本特愿2018-024007
技术实现要素:
发明所要解决的问题
7.改性hdl在理论上在实验室中可以通过专利文献1中记载的技术进行定量。本发明的发明人的专利文献2的技术与现有技术相比进一步精炼。可以预想到,应用这些方法,容易建立即使不是充分精炼也能够用于改性hdl的定量的方法。
8.然而,现状是专利文献1的技术也没有达到普及。进一步地,即使使用本发明的发明人的专利文献2的技术,使用实验室以外的条件、不同的检体实施时,有时改性hdl的定量结果也不是恒定的。上述差异除了实验室内的条件以外,还考虑了实施技术的人的试验技术的差异等各种因素。本发明的发明人考虑到上述的历史经过和在临床的实际应用中即使条件稍差也应该能够进行测定,以将改性hdl的定量技术改良为更具有通用性的定量技术为目标进行了深入研究。
9.本发明是鉴于上述情况而完成的,其目的在于提供一种与以往相比能够更稳定且准确地对改性hdl进行定量、对心/血管系统疾病、糖尿病或糖尿病性疾病等、或其发展程度的判定有用的改性hdl的定量方法、以及用于该定量方法的分析用试剂。用于解决问题的手段
10.为了解决上述问题,本发明具有以下的方式。[1]一种改性hdl的定量方法,其为试样中所含的改性hdl的定量方法,其中,使所述改性hdl与改性hdl结合蛋白结合,对所述改性hdl结合蛋白与所述改性hdl的结合体进行定量,所述改性hdl结合蛋白包含具有因子v的l链部位的序列的蛋白质或其突变体。[2]在所述改性hdl的定量方法的基础上,所述改性hdl结合蛋白包含因子v的磷脂识别部位的序列。[3]在所述改性hdl的定量方法的基础上,所述改性hdl结合蛋白包含因子v的序列。[4]在所述改性hdl的定量方法的基础上,所述改性hdl结合蛋白是具备与作为因子v的磷脂识别部位的c1-c2结构域具有部分同源性的部位的蛋白质。[5]在所述改性hdl的定量方法的基础上,具备与所述c1-c2结构域具有部分同源性的部位的蛋白质为mfg-e8、del-1或因子viii。[6]在所述改性hdl的定量方法的基础上,所述改性hdl结合蛋白为重组蛋白。[7]在所述改性hdl的定量方法的基础上,所述定量是形成所述改性hdl与所述改性hdl结合蛋白的复合体并通过免疫分析对所述复合体进行定量。[8]在所述改性hdl的定量方法的基础上,通过使用了将所述改性hdl结合蛋白、或将与其结合的蛋白质固相化的elisa板的elisa法来进行基于所述免疫分析的定量。[9]在所述改性hdl的定量方法的基础上,所述定量是形成所述改性hdl、所述改性hdl结合蛋白以及lox-1蛋白的复合体并通过免疫分析对所述复合体进行定量。[10]在所述改性hdl的定量方法的基础上,在所述定量中,使用血清或血浆作为试样。[11]在所述改性hdl的定量方法的基础上,在所述定量中具备使用血清作为试样并在所述试样中添加所述改性hdl结合蛋白的工序。
[12]一种分析用试剂,所述分析用试剂用于为了对心/血管系统疾病、糖尿病或糖尿病性疾病、它们的风险或其发展程度进行判定的改性hdl的定量,其中,所述分析用试剂包含能够与所述改性hdl结合的改性hdl结合蛋白,所述改性hdl结合蛋白包含具有因子v的l链部位序列的蛋白质或其突变体。[13]在所述分析用试剂的基础上,所述改性hdl结合蛋白包含因子v的磷脂识别部位的序列。[14]在所述分析用试剂的基础上,所述改性hdl结合蛋白包含因子v的序列。[15]在所述分析用试剂的基础上,所述改性hdl结合蛋白是具备与作为因子v的磷脂识别部位的c1-c2结构域具有部分同源性的部位的蛋白质。[16]在所述分析用试剂的基础上,具备与所述c1-c2结构域具有部分同源性的部位的蛋白质为mfg-e8、del-1或因子viii。[17]在所述分析用试剂的基础上,所述改性hdl结合蛋白为重组蛋白。[18]在所述分析用试剂的基础上,所述心/血管系统疾病是因动脉硬化或其发展而产生的心肌梗塞或脑中风。发明效果
[0011]
根据本发明,可以得到与以往相比能够更稳定且准确地对改性hdl进行定量、对心/血管系统疾病、糖尿病或糖尿病性疾病等、或其发展程度的判定有用的改性hdl的定量方法、以及用于该定量方法的分析用试剂。
附图说明
[0012]
图1是表示第一实施方式所涉及的改性hdl的定量方法的概要图。图2是表示第二实施方式所涉及的改性hdl的定量方法的概要图。图3是表示试验例1所涉及的改性hdl的检测灵敏度的曲线图。图4是表示试验例2所涉及的血浆中的改性hdl的检测灵敏度的曲线图。图5是表示试验例2所涉及的血清中的改性hdl的检测灵敏度的曲线图。图6是表示试验例2所涉及的另一因子v浓度下的血浆中的改性hdl的检测灵敏度的曲线图。图7是表示试验例2所涉及的另一因子v浓度下的血清中的改性hdl的检测灵敏度的曲线图。图8是表示试验例4所涉及的因子v的固相化量的曲线图。图9是表示试验例4所涉及的改性hdl结合试验的曲线图。图10是表示试验例5所涉及的血浆以及血清中的改性hdl的定量的曲线图。
具体实施方式
[0013]
以下,示出实施方式对本发明所涉及的改性hdl的定量方法以及分析用试剂进行说明。但是,本发明并不限定于以下的实施方式。
[0014]
(第一实施方式)(改性hdl的定量方法)本实施方式的改性hdl的定量方法在对试样中所含的改性hdl进行定量时,使改性
hdl与改性hdl结合蛋白结合。对该改性hdl结合蛋白与改性hdl结合而成的复合体进行定量。
[0015]
本实施方式中的改性hdl包含与本来在生物体内具有生理活性的hdl具有某种结构差异的hdl,尤其是指由于这些结构的差异而生理活性降低的改性hdl。作为hdl变为改性hdl的机理,例如包括构成蛋白质的化学修饰、部分或完全分解、遗传缺损及突变、高次结构的异常、变化、或者与使其失去活性的分子的结合等主要原因。
[0016]
作为这样的改性hdl的例子,例如包括构成hdl的蛋白质或脂质的任意部位被氧化的氧化hdl。作为这样的改性hdl,例如可列举为hclo-hdl、hne-hdl、氨基甲酰化(carbamylated)hdl以及mda-hdl等。已知这些改性hdl阻碍血管壁的血管内皮细胞,提高引起动脉硬化、血栓形成的心脏疾病、缺血疾病等动脉硬化性疾病这样的各种疾病的发病风险。
[0017]
在本实施方式的改性hdl的定量方法中,使改性hdl与改性hdl结合蛋白结合,并对改性hdl结合蛋白与改性hdl的结合体进行定量。本实施方式的改性hdl结合蛋白广泛地指能够与改性hdl直接相互作用的、例如该蛋白质本身能够与改性hdl结合的蛋白质。改性hdl有时获得了与引起对生物体不利的反应的受体相互作用的活性。此时,有时改性hdl经由改性hdl结合蛋白与受体结合,即改性hdl与改性hdl结合蛋白直接结合,该改性hdl结合蛋白与受体结合。作为改性hdl结合蛋白,例如有因子v、其突变体以及具有部分同源性的蛋白质等。作为有时经由其他蛋白质与改性hdl结合的受体,有后述的lox-1蛋白。
[0018]
在本实施方式中,改性hdl结合蛋白包含具有因子v的l链部位的序列的蛋白质或其突变体。因子v(第v因子)作为构成凝固体系的蛋白质而已知,是由a1-a2-b-a3-c1-c2结构域构成的约330kda的蛋白质,大致分为由a1-a2结构域构成的h链(重链)和由a3-c1-c2结构域构成的l链(轻链)。已知主要是h链与细胞膜结合,l链经由c1-c2结构域识别、结合磷脂。突变体是指进行了一部分序列的置换的突变体,在本实施方式中,优选为主要是因子v的l链部位以外的部位被置换的突变体。
[0019]
由于因子v的l链部位是与改性hdl直接结合的部位,因此通过使改性hdl结合蛋白为包含该部位的蛋白质或其突变体,能够使改性hdl与改性hdl结合蛋白结合并用于定量。另外,作为改性hdl结合蛋白,通过使用具有作为因子v的一部分的l链部位的序列的蛋白质,能够使用在具有与改性hdl结合的部位的同时具有与因子v不同的结构的蛋白质。即,能够使用比因子v容易获得的蛋白质、容易进行试验的蛋白质。作为比因子v容易获得的蛋白质,例如通过仅使用l链部位以及最小限度的序列,能够使用全长比因子v短、容易进行作为重组蛋白的制造的蛋白质。作为容易进行试验的蛋白质,可以使用通过变更l链以外的序列而更容易进行保存、在板上的固相化的蛋白质。
[0020]
改性hdl结合蛋白优选还包含因子v的磷脂识别部位的序列。因子v的序列中的、l链所具备的磷脂识别部位能够识别改性hdl并有效地与其结合。
[0021]
改性hdl结合蛋白优选包含因子v的序列。在此,因子v的序列是指因子v蛋白的全长,可以使用因子v本身,也可以使用与其他蛋白质的融合体或结合、修饰蛋白质等。
[0022]
改性hdl结合蛋白还优选为具备与作为因子v的磷脂识别部位的c1-c2结构域具有部分同源性的部位的蛋白质。作为这样的具备与c1-c2结构域具有部分同源性的部位的蛋白质,可列举为mfg-e8、del-1或因子viii。另外,也可以是在一部分中包含这些蛋白质、突变体、这些蛋白质的序列的蛋白质。
[0023]
改性hdl结合蛋白例如还优选使用重组蛋白。在此,重组蛋白是指通过基因重组表达而得到的蛋白质。重组蛋白可以根据需要导入与其他结构的融合、突变。
[0024]
在本实施方式中,进行试样中所含的改性hdl的定量。在此,作为试样,广泛地指包含从生物中取出的成分的试样。试样优选使用上述成分的液体,或者在上述成分中添加液体而制成液体的试样。作为试样,例如可以将生物的体液直接用作试样。作为生物的体液,例如可以使用人的血液或唾液。作为血液的样品,可以使用血清或血浆等。在本实施方式中,将这些体液作为试样供于上述的定量。
[0025]
在本实施方式中,优选使用血清作为试样。在本实施方式中,使具备与改性hdl直接结合的因子v的l链部分的序列的改性hdl结合蛋白与试样中的改性hdl结合。因此,即使将存在不包含与改性hdl直接结合的因子的情况的血清用作试样,也能够稳定且准确地对改性hdl进行定量。除此之外,血清与血浆等其他体液试样相比,血清更容易进行检体的取得、保存。实际上,作为血液试样,以血清的形式冷冻保持的检体在国际上是一般的,因此是有益的技术。
[0026]
本发明的发明人着眼于以下方面:在现有技术中将lox-1等与改性hdl相互作用的蛋白质用于改性hdl的定量的情况下,将血浆用于试样时能够检测出改性hdl,但将血清用于试样时改性hdl的检测较少,无法准确地进行定量。因此,预测了通过将在由血液、血浆形成血清的过程中分解丧失的物质填补到测定系统中,能够进行将血清用于试样的测定。作为上述填补的物质,本发明的发明人着眼于因子v。作为生物体内的反应,在改性hdl与lox-1结合时,经由因子v结合。具体而言,因子v所具备的磷脂酰丝氨酸(ps)识别部位与改性hdl结合,lox-1识别部位与lox-1结合。
[0027]
如后所述,使用血清作为试样,在试样中添加因子v时,血清中的改性hdl检测灵敏度大致与添加量对应地增加。因此,通过在血清等试样中添加因子v这样的改性hdl结合蛋白,能够对改性hdl进行定量。
[0028]
在上述的定量中,可以使用用于蛋白质的定量(蛋白质量的测定)的公知的手段。例如,可以在上述定量中使用免疫学方法。作为使用了免疫学方法的定量、免疫分析,可以适当使用酶(酶免疫分析、eia、elisa)、荧光物质(荧光免疫分析、fia)或放射性物质(放射免疫分析、ria)等。其中,elisa比较廉价、简便且能够分析多个样品,因此优选。
[0029]
例如,在本实施方式中,在上述定量中可以使用elisa法。具体而言,将改性hdl结合蛋白固相化在elisa板上。改性hdl结合蛋白的固相化(固定化)可以适当使用已知的方法。例如,可以使受体与公知的载体(支承体)结合。在该elisa板中添加试样,使试样中所含的改性hdl与改性hdl结合蛋白结合,清洗elisa板去除未结合物,使用能够检测改性hdl或复合体的抗体进行检测时,能够对定量的对象和改性hdl与改性hdl结合蛋白的复合体进行定量。作为与改性hdl或上述复合体结合的抗体,可以适当使用与hdl序列结合的抗体。
在本实施方式中,由于对elisa板上的改性hdl与改性hdl结合蛋白的复合体进行检测,因此在板上被检测的是改性hdl。需要说明的是,在本实施方式中与改性hdl结合的抗体可以使用单克隆以及多克隆抗体中的任一种。
[0030]
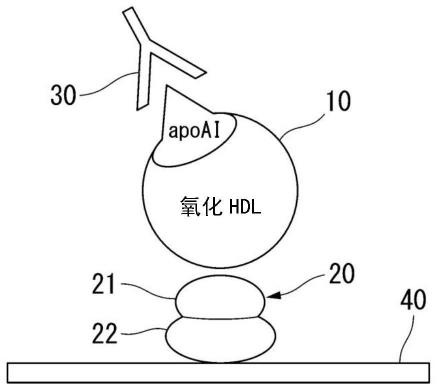
在本实施方式中,更具体而言,可以形成改性hdl与改性hdl结合蛋白结合而成的复合体,并通过免疫分析对该复合体进行定量。关于该免疫分析,在图1中示出示意图进行说明。例如,使改性hdl结合蛋白20固相化在板40上。在本实施方式中,作为例子,改性hdl结合蛋白20是具备l链部位21和h链部位22的、与因子v蛋白具有同源性的蛋白质。板40是elisa板。若利用已知的载体进行固相化,则在板40上产生上述h链部位22固相化在板40上的结构。接着,清洗板40,去除未结合的改性hdl结合蛋白20。向该板40注入来自体液的试样。试样中的改性hdl10与板40上的l链部位21结合。利用与改性hdl或上述复合体结合的抗体30对该板40上的复合进行定量。在本实施方式中,抗体30使用了抗载脂蛋白ai抗体(抗apoa1)。
[0031]
在本实施方式中,不使用现有技术那样的lox-1等改性hdl受体,而是将与改性hdl直接结合的改性hdl结合蛋白固相化在板上,因此不需要改性hdl受体。例如,作为改性hdl结合蛋白,如果使用与上述那样的因子v相比全长更短的蛋白质等容易获得的蛋白质,则与将lox-1等改性hdl受体用于定量相比,能够更容易地进行定量。
[0032]
(用于改性hdl定量的分析用试剂)接着,对用于上述体液中的改性hdl定量方法的分析用试剂进行说明。通过将该分析用试剂用于体液中的改性hdl的定量,能够用于为了对心/血管系统疾病、糖尿病或糖尿病性疾病、或其发展程度进行判定的体液中的改性hdl的定量。分析用试剂包含上述的改性hdl结合蛋白。通过包含改性hdl结合蛋白,能够进行具有生理活性的改性hdl的定量。
[0033]
(其他构成)本实施方式的分析用试剂也可以含有其他免疫分析的试剂中所含的成分。
[0034]
另外,本实施方式的分析用试剂也可以作为具备多个上述构成的试剂盒来提供。例如,该试剂盒可以具备包含用于改性hdl的定量的改性hdl结合蛋白的分析用试剂。另外,该试剂盒可以包含用于上述定量操作的载体、elisa板、显色底物或抗体等。
[0035]
另外,也可以包含固相化有上述蛋白质的elisa板。例如,也可以作为分析用板提供,该分析用板用于为了对心/血管系统疾病、糖尿病或糖尿病性疾病、它们的风险、或其发展程度进行判定的改性hdl的定量,具备固相化有能够与改性hdl结合的改性hdl结合蛋白的elisa板,改性hdl结合蛋白包含具有因子v的l链部位序列的蛋白质或其突变体。
[0036]
(本实施方式的效果)本实施方式的改性hdl的定量方法与现有技术相比,能够稳定且准确地对改性hdl进行定量。本实施方式能够稳定且准确地进行定量是指,相对于以往的方法根据试样而检测灵敏度本身存在差异的情况、检测灵敏度较低,本实施方式的方法能够与试样的条件、例如改性hdl以外的含有物等无关地以恒定的较高灵敏度对改性hdl进行定量。
[0037]
本实施方式的改性hdl的定量方法能够进行改性hdl的稳定且准确的定量,从而能够用于疾病、它们的风险、发展程度的判定。作为疾病,被认为与hdl相关的疾病广泛地成为
对象,例如可列举为心/血管系统疾病、糖尿病或糖尿病性疾病。作为心/血管系统疾病,尤其是可列举为因动脉硬化或其发展而产生的心肌梗塞或脑中风。
[0038]
(本实施方式的用途)本实施方式的改性hdl的定量方法以及分析用试剂例如可以用于在体液中的hdl的定量中通过测定改性hdl来诊断患上上述的心/血管系统疾病和/或患上糖尿病或糖尿病性疾病的方法。
[0039]
作为诊断方法,例如也可以在上述试样中的改性hdl的测定中,根据改性hdl相对于总hdl量的比率的变化,来诊断患有上述疾病的风险和/或它们的发展程度。在该诊断方法中,还包含使用蛋白质的标准品、健康体液试样等作为标准品,制作标准曲线、对比表等,将基于诊断对象的检体试样的定量结果与标准曲线、对比表等进行比较而用于诊断的过程等。另外,也可以用于高血压、睡眠呼吸暂停综合征之类的与肥胖相关的疾病的患病、患病风险和/或其发展程度的判定以及诊断。
[0040]
(第二实施方式)在第二实施方式中,形成改性hdl、改性hdl结合蛋白以及lox-1蛋白的复合体,并通过免疫分析对该复合体进行定量。需要说明的是,对于与第一实施方式相同的构成,在附图中标注相同的附图标记并省略说明。
[0041]
换言之,相对于试图通过对改性hdl与lox-1蛋白的复合体进行检测来进行定量的现有技术,本实施方式试图通过进一步借助改性hdl结合蛋白而稳定性、可靠性更高地进行检测。在本实施方式中,可以通过对使用了lox-1蛋白的现有技术中进行的方法、设备等进行改良来进行定量。
[0042]
lox-1是本发明的发明人发现的分子(sawamura t et al.nature 386,73-77,1997),已知为凝集素样氧化ldl受体的一种。lox-1的详细结构也已明确,已知为细胞膜一次贯通型的膜蛋白,具备凝集素样的结构域,该凝集素样结构域为氧化ldl的识别部位(日本特开平9-98787号公报等);血液中也存在可溶性的成分;经修饰的高密度脂蛋白(hdl)作为lox-1的配体而发挥作用等(日本特开2012-100585号公报、日本特许第6231307号公报等)。
[0043]
上述lox-1蛋白例如也优选使用重组lox-1蛋白。在此,重组lox-1蛋白是指通过基因重组表达而得到的lox-1蛋白。重组lox-1蛋白也可以根据需要导入与其他结构的融合、突变。
[0044]
在上述的免疫分析中,改性hdl、改性hdl结合蛋白与lox-1蛋白的复合体的定量可以使用所谓的夹心elisa来进行。将本实施方式的定量法的概要示于图2。作为该定量法,例如,使lox-1蛋白50固相化在板40a上。使改性hdl结合蛋白20与该板40a上的lox-1蛋白50结合。通过向该板40a注入来自体液的试样,使改性hdl10同该lox-1蛋白50与改性hdl结合蛋白20的复合体结合。接着,可以利用与上述的改性hdl或上述复合体结合的抗体30对板40a上的复合体进行定量。抗体30也可以使用抗因子-v抗体。
[0045]
在本实施方式中,可以具备使用血清作为试样并在上述试样中添加上述改性hdl
结合蛋白的工序。可以通过将该试样添加到上述的固相化有lox-1的elisa板中,形成在elisa板上的lox-1上结合有改性hdl结合蛋白以及改性hdl的复合体,利用上述的与改性hdl或上述复合体结合的抗体对elisa板上的结合体进行定量。
[0046]
需要说明的是,用于本实施方式的定量方法的分析用试剂可以包含用于具有病理学活性的改性hdl的定量的重组lox-1蛋白。如上所述,该分析用试剂的重组lox-1蛋白与改性hdl相互作用,因此能够通过免疫分析对改性hdl、改性hdl结合蛋白与lox-1的复合体进行改性hdl的定量。
[0047]
另外,本实施方式的分析用试剂也可以作为具备多个上述构成的试剂盒来提供。例如,该试剂盒可以具备包含用于改性hdl的定量的改性hdl结合蛋白的分析用试剂以及包含lox-1蛋白的分析用试剂。实施例
[0048]
以下,示出实施例。需要说明的是,本发明并不限定于实施例。
[0049]
(试验例1)(基于因子v的改性hdl检测灵敏度的验证)首先,调查因子v对改性hdl与作为改性hdl的受体的lox-1的结合的影响。在固相化有lox-1的板中添加包含改性hdl的血浆或血清试样,进行利用改性hdl的抗体(抗apoa1抗体)对lox-1与改性hdl的复合体进行检测的试验。此时,如果通过在试样中添加因子v,检测灵敏度依赖于因子v的添加量而提高,并且能够得到稳定的检测灵敏度,则能够将因子v与改性hdl的结合的机理用于改性hdl的定量。
[0050]
elisa法按照以下的步骤进行。使重组人lox-1(61-273aa)以0.15μg/孔固相化在384孔板上。用pbs清洗两次后,用1%酪蛋白-na进行封闭。用pbs清洗三次后,将添加有因子v的血浆或血清试样在室温下温育2小时。试样稀释液使用了1%酪蛋白-na、10mm hepes、150mm nacl、ph7.4、100μm apmsf。用pbs清洗三次,添加制备成1μg/ml的抗apoa1抗体(鸡#1),在室温下温育1小时。用pbs清洗三次,添加稀释4000倍的hrp标记抗鸡igy抗体,在室温下温育1小时。抗体反应后,用pbs清洗五次,将tmb溶液(bio-rad公司制造)添加到板中,在室温下使其反应。用2m硫酸使反应停止,对450nm的吸光度进行测定。改性hdl浓度(ng/ml)使用将通过硫酸铜氧化的氧化hdl作为标准品而制作的标准曲线来计算。
[0051]
将基于elisa法的检测结果示于图3。图3中的(a)、(b)、(c)、(d)、(e)分别表示关于从不同的受试者(a、b、c、d、e)采集的血浆(plasma)以及血清(serum)的结果。纵轴的complex(复合体)表示相对于针对被固相化的lox-1而形成了某种复合体的改性hdl(包括lox-1改性hdl的结合借助了其他蛋白质的改性hdl),抗apoa1抗体所检测出的浓度,横轴表示添加的因子v的浓度。关于血清,如图3中的(a)、(b)、(c)、(d)、(e)所示,在从受试者a、b、c、d、e采集的检体的全部五个例子中,改性hdl的检测灵敏度依赖于因子v的添加量而上升。关于血浆,根据所采集的检体的不同,存在未观察到因添加量而产生的差异较大的情况和大致依赖于添加量而上升的情况。根据上述结果,认为,对于含有物质比血浆少的血清而言,由于几乎不包含因子v等经由lox-1与改性hdl的结合的蛋白质,因此通过添加该因子v而介导了该结合。另一方
面,认为,血浆中有时包含因子v等介导lox-1与改性hdl的结合的蛋白质,但其含量根据检体及其采集、保存方法等而各不相同,添加因子v所产生的影响不同。上述结果表明,因子v与改性hdl结合,改性hdl与lox-1的结合经由因子v进行,进行了该结合的复合体的检测灵敏度依赖于因子v的添加量而提高。
[0052]
(试验例2)根据lox-1相对于板的固相化的有无来调查检测灵敏度,由此调查了由因子v引起的检测灵敏度的上升是否是针对lox-1、因子v以及改性hdl的复合体而发生的。图4表示使用从上述a、b、c、d、e采集的各血浆作为试样,以达到1μg/ml的方式加入因子v蛋白的情况(plasma+fv)以及没有加入因子v蛋白的情况(plasma),作为板使用将lox-1固相化的板(lox-1immobilized)以及没有进行固相化的板(non coat),其他与试验例1同样地通过elisa法进行了检测的结果。图5表示使用从上述a、b、c、d、e采集的各血清作为试样,以达到1μg/ml的方式加入因子v蛋白的情况(serum+fv)以及没有加入因子v蛋白的情况(serum),其他与图4同样地进行了检测的结果。图6表示使用从上述a、b、c、d、e采集的各血浆作为试样,以达到10μg/ml的方式加入因子v蛋白的情况以及没有加入因子v蛋白的情况,其他与图4同样地进行了检测的结果。图7表示使用从上述a、b、c、d、e采集的各血清作为试样,以达到10μg/ml的方式加入因子v蛋白的情况以及没有加入因子v蛋白的情况,其他与图5同样地进行了检测的结果。
[0053]
根据图4~图7,若使用没有将lox-1固相化的板,则无论是在试样中加入有因子v的情况下还是在没有加入的情况下,检测量都看不到差异。根据该结果,示出了就因子v而言,lox-1、因子v以及改性hdl结合而形成复合体,使检测量增加。对图4和图5、图6和图7进行比较,相对于使用了血浆的图4、图6,在使用了血清的图5、图7中,通过添加因子v,检测量变高。据认为该结果也与试验例1同样地,被认为是血清中不包含的物质通过因子v的添加而得到了补充。
[0054]
(试验例3)由于因子v与改性hdl结合,因此尝试是否能够使因子v直接固相化在板上来进行改性hdl的定量。
[0055]
首先,将以0~10μg/ml的方式溶解在pbs(-)中的因子v添加到板上,通过基于抗因子v抗体的elisa法,尝试能否在板上进行固相化。以如下条件进行。固相化:人因子v各浓度封闭:1%酪蛋白-na中,2hr室温检测:第一抗体anti-fv-lc(ahv-5101)1μg/ml、1hr、室温第二抗体anti-mouse igg-hrp、1:4000、1%酪蛋白-na中、1hr室温
[0056]
将结果示于图8。示出了能够大致依赖于浓度地相对于板进行因子v的固相化。
[0057]
接着,对该因子v固相化elisa板进行未改性的hdl(nhdl)以及改性hdl的结合的试验。改性hdl使用通过硫酸铜使hdl氧化而成的氧化hdl,即cu
2+-oxhdl。使因子v固相化在384孔板(greiner公司制造)上。用pbs清洗两次后,用1%酪蛋白-na进行封闭。用pbs清洗三次后,将用试样稀释液(1%酪蛋白-na,10mm hepes,150mm nacl,ph7.4,100μm apmsf)制备成1μg/ml的nhdl或cu
2+-oxhdl在室温下温育2小时。用pbs清
洗三次,添加制备成1μg/ml的抗apoa1抗体(鸡#1),在室温下温育1小时。用pbs清洗三次,添加稀释4000倍的hrp标记抗鸡igy抗体,在室温下温育1小时。抗体反应后,用pbs清洗五次,将tmb溶液(bio-rad公司制造)添加到板中,在室温下使其反应。用2m硫酸使反应停止,对450nm的吸光度进行测定。
[0058]
将结果示于图9。依赖于在板上的因子v固相化量,改性hdl的检测量变高。另一方面,nhdl的检测量没有较大的变化。根据该结果,示出了该板能够用于改性hdl的检测。
[0059]
(试验例4)使用与试验例3同样地进行了调整的因子v固相化板,对人血浆以及血清中的改性hdl进行检测。使用从受试者x、y采集的血浆以及血清的检体,通过elisa法进行改性hdl的定量。使因子v固相化在384孔板(greiner公司制造)上。用pbs清洗两次后,用1%酪蛋白-na进行封闭。用pbs清洗三次后,将血浆或血清试样在室温下温育2小时。用pbs清洗三次,添加制备成1μg/ml的抗apoa1抗体(鸡#1),在室温下温育1小时。用pbs清洗三次,添加稀释4000倍的hrp标记抗鸡igy抗体,在室温下温育1小时。抗体反应后,用pbs清洗五次,将tmb溶液(bio-rad公司制造)添加到板中,在室温下使其反应。用2m硫酸使反应停止,对450nm的吸光度进行测定。
[0060]
将结果示于图10。关于从受试者x采集的检体,示于图10中的(a),关于从受试者y采集的检体,示于图10中的(b)。与现有技术中的lox-1固相化的情况不同,在血浆和血清中测定值几乎没有差异,即,对于血浆,也与检体无关地观察到稳定的检测灵敏度的高低。该技术与将lox-1固相化的技术相比灵敏度较高,另外,示出了与使用了lox-1以及因子v的夹心法相比,不仅能够容易地进行定量,而且能够对血浆以及血清这两者稳定且可靠地以较高的灵敏度进行定量。
[0061]
以上,对本发明的几个实施方式进行了说明,但这些实施方式是作为例子而提示的,并不意图对发明的范围进行限定。这些实施方式能够以其他各种方式实施,在不脱离发明的主旨的范围内,能够进行各种省略、置换、变更。这些实施方式及其变形包含在发明的范围、主旨中,同样地包含在权利要求书所记载的发明及其均等的范围内。工业实用性
[0062]
根据本发明,可得到能够比以往更稳定且准确地对改性hdl进行定量的改性hdl的定量方法、以及用于该定量方法的分析用试剂。该定量方法以及分析用试剂尤其是能够用于对患上心/血管系统疾病、患上糖尿病以及糖尿病性疾病的风险或发展程度的判定等。附图标记说明
[0063]
10:改性hdl;20:改性hdl结合蛋白;21:l链部位;22:h链部位;30:抗体;40、40a:板;50:lox-1蛋白。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1