一种基于质谱法评估免疫沉淀实验效果的方法及系统与流程
1.本发明属于生物技术领域,更具体地,涉及一种基于质谱法评估免疫沉淀实验效果的方法及系统。
背景技术:
2.免疫沉淀(ip,immunoprecipitation)是一种常用的生物技术实验方法,常用于进行特定蛋白的亲和纯化或蛋白相互作用的研究。但很多免疫沉淀实验并不能获得理想的结果,并且免疫沉淀实验成功与否,也需要通过特定方法进行验证。
3.目前最常用的免疫沉淀实验效果验证方法是免疫印迹。简单来说,免疫沉淀实验后获得的蛋白样品,经过聚丙烯酰胺凝胶电泳、转膜、封闭后,依次以针对诱饵蛋白的一级抗体和针对一级抗体的二级抗体进行孵育,通过底物化学发光进行显影,根据诱饵蛋白分子量对应位置是否显影出条带验证免疫沉淀实验是否成功,并基于显影颜色深浅评估所用抗体的亲和富集效率。
4.但是,显影条带位置仅能代表其对应蛋白的分子量,只能判断抗体特异性结合的是某一特定分子量的蛋白,无法确定该抗体是针对诱饵蛋白特异性结合,而且受抗体本身性质和生产质量的影响,难以避免抗体轻链、抗体重链即其他非特异性结合的条带,这些条带若分子量与诱饵蛋白相近,会干扰诱饵蛋白的显影,无法获得有效的验证结果;另外,显影颜色深浅也会受多种因素影响,如样品上样量、抗体孵育时间、抗体浓度、曝光时间,以显影颜色深浅来评估抗体亲和富集效率容易产生较大的偶然误差,评估准确性较差。
5.而且免疫印迹实验仅能对特定蛋白进行检测和分析,无法整体评估样品中的蛋白情况,也无法对样品用量和不同样品间的整体差异进行评估,难以评估样品用量和对照组设置情况,另外,免疫印迹实验流程复杂,步骤较多,难以标准化,其结果很大程度上取决于实验操作人员的技能和熟练度。因此,探究一种可以快速准确定量评估免疫沉淀实验效果的方法尤为重要。
技术实现要素:
6.针对现有技术的以上缺陷或改进需求,本发明提供了一种基于质谱法评估免疫沉淀实验效果的方法及系统,其目的在于基于质谱法评估免疫沉淀实验效果,由此解决现有免疫印迹法评估周期长、准确性较差和难标准化的技术问题。
7.为实现上述目的,按照本发明的一个方面,提供了一种基于质谱法评估免疫沉淀实验效果的方法,其包括以下步骤:
8.(1)免疫沉淀蛋白预处理:将免疫沉淀实验获得的免疫沉淀蛋白,采用清洗液清洗、蛋白酶酶解以及脱盐处理,获得可供质谱直接检测的肽段和/或蛋白样品;
9.(2)质谱检测:将步骤(1)获得的肽段和/或蛋白样品进行质谱检测,获取质谱图谱的原始数据,搜库解析图谱原始数据,获得肽段和/或蛋白鉴定和定量数据;所述数据包括第1项评估指标样品中总蛋白鉴定和定量情况以及第2项评估指标诱饵蛋白定量数据在总
蛋白定量列表中的排名;
10.(3)依据步骤(2)获得的评估指标数据,按照如下评估原则进行评估:
11.样品中总蛋白鉴定和定量情况越好,判断免疫沉淀实验样本量越多,效果越好;
12.诱饵蛋白的定量数据在所有蛋白定量数值中排名越高,判断免疫沉淀实验亲和富集效率和特异性越好。
13.优选地,所述基于质谱法评估免疫沉淀实验效果的方法,其所述第1项评估指标和第2项评估指标,具体按照如下原则进行评估:
14.①
蛋白鉴定数量和/或总离子色谱图峰面积大于预设阈值,则判断第1项评估指标通过评估,反之,则未通过;
15.所述蛋白鉴定数量预设阈值在300至1500间取值,所述总离子色谱图峰面积预设阈值在2e8至1e10间取值;
16.②
诱饵蛋白的定量数据在所有蛋白定量数据中的排名小于预设阈值,则判断通过第2项评估指标通过评估,反之,则未通过;
17.所述诱饵蛋白的定量数据在所有蛋白定量数据中的排名的预设阈值在3%至10%取值;
18.上述两项评估指标均通过,则判断免疫沉淀实验成功;若第1项评估指标未通过,则判断免疫沉淀实验样本量不足;若第2项评估指标未通过,则判断免疫沉淀实验亲和富集效率不足。
19.优选地,所述基于质谱法评估免疫沉淀实验效果的方法,其在设置对照组的情况下,所述数据,还包括第3项评估指标诱饵蛋白定量数据在免疫沉淀实验组样品与对照组样品中的差异以及第4项评估指标诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名,并按照如下评估原则进行评估:
20.诱饵蛋白在实验组与对照组间的定量差异越显著,判断免疫沉淀实验亲和富集效率越高;
21.诱饵蛋白在免疫沉淀实验组与对照组间的差异程度排名越高,判断免疫沉淀实验亲和富集特异性越好。
22.优选地,所述基于质谱法评估免疫沉淀实验效果的方法,其所述第3项评估指标和第4项评估指标,具体按照如下评估原则进行评估:
23.③
所述诱饵蛋白在实验组与对照组间的定量差异倍数高于预设阈值、定量差异显著性p值或p值校正值低于预设阈值,则判断第3项评估指标通过,反之,则未通过,若第3项评估指标未通过,则判断免疫沉淀实验亲和富集效率不足;
24.所述诱饵蛋白在实验组与对照组间的定量差异倍数的预设阈值在2至10取值;所述定量差异显著性p值或p值校正值的预设阈值为0.01或0.05;
25.④
诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名小于预设阈值,则判断通过第4项评估指标,反之,则未通过,若第4项评估指标未通过,则判断免疫沉淀实验亲和富集特异性不足;
26.所述诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名的预设阈值在1%至3%,或3至10间取值。
27.优选地,所述基于质谱法评估免疫沉淀实验效果的方法,其在设置对照组的情况
下,所述数据,还包括第5项评估指标免疫沉淀实验组样品和对照组样品中总蛋白鉴定和定量差异,按照如下原则进行评估:
28.实验组与对照组整体定量差异越小,判断对照组设置合理性越好。
29.优选地,所述基于质谱法评估免疫沉淀实验效果的方法,其所述第5项评估指标,具体按照如下原则进行评估:
30.⑤
蛋白鉴定数量差异和/或总离子色谱图峰面积差异小于预设阈值,和/或蛋白定量相关系数大于预设阈值,则判断第5项评估指标通过,反之,则未通过;若第5项评估指标通过,判断对照组实验设置合理;
31.所述蛋白鉴定数量差异的预设阈值在5%至40%取值;所述总离子色谱图峰面积差异的预设阈值在5%至40%取值;所述蛋白定量相关系数的预设阈值在0.6至0.95取值。
32.按照本发明的另一方面,还提供了一种免疫沉淀实验效果评估系统,其包括数据获取模块、判断模块和评估结果显示模块;
33.所述数据获取模块,用于获取待评估免疫沉淀蛋白的肽段和/或蛋白鉴定和定量数据,所述蛋白鉴定和定量数据,包括蛋白鉴定数量、肽段鉴定数量、样品检测总信号值和总离子色谱图峰面积中一种或多种组合参数;ibaq、lfq intensity、intesnity、谱图数、nsaf和saf中一种或多种组合参数;并将数据传输给判断模块;
34.所述判断模块,用于依据接收的数据,按照如下原则进行判断:
35.①
蛋白鉴定数量和/或总离子色谱图峰面积大于预设阈值,则判断第1项评估指标通过评估,反之,则未通过;所述蛋白鉴定数量预设阈值在300至1500间取值;所述总离子色谱图峰面积预设阈值在2e8至1e10间取值;
36.②
诱饵蛋白的定量数据在所有蛋白定量数据中的排名低于预设阈值,则判断第2项评估指标通过评估,反之,则未通过;所述诱饵蛋白的定量数据在所有蛋白定量数据中的排名的预设阈值在3%至10%取值;并将判断结果提交给评估结果显示模块;
37.所述评估结果显示模块,用于依据判断结果进行显示,具体如下:
38.在没有设置对照组情况下:
39.第1项评估指标若通过,显示免疫沉淀实验样本量达标,若未通过,显示免疫沉淀实验样本量不足;
40.第2项评估指标若通过,显示免疫沉淀实验亲和富集效率达标,若未通过,显示免疫沉淀实验亲和富集效率不足;
41.若免疫沉淀实验样本量和免疫沉淀实验亲和富集效率均达标,说明免疫沉淀实验成功,若对应评估指标未通过,说明免疫沉淀实验在对应方面存在缺陷,需要改进。
42.优选地,所述免疫沉淀实验效果评估系统,其所述数据获取模块,在设置对照组实验的情况下,还用于获取定量差异倍数、定量差异显著性p值和定量差异显著性p值校正值中一种或多种组合参数以及诱饵蛋白定量差异排名;
43.所述判断模块,还按照如下原则判断:
44.③
所述诱饵蛋白在实验组与对照组间的定量差异倍数高于预设阈值、定量差异显著性p值或p值校正值低于预设阈值,则判断第3项评估指标通过,反之,则未通过,若第3项评估指标未通过,则判断免疫沉淀实验亲和富集效率不足;所述诱饵蛋白在实验组与对照组间的定量差异倍数的预设阈值在2至10取值;所述定量差异显著性p值或p值校正值的预
设阈值为0.01或0.05;
45.④
诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名小于预设阈值,则判断通过第4项评估指标,反之,则未通过,若第4项评估指标未通过,则判断免疫沉淀实验亲和富集特异性不足;所述诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名的预设阈值在1%至3%,或3至10间取值。
46.优选地,所述免疫沉淀实验效果评估系统,其所述数据获取模块,在设置对照组实验的情况下,还用于获取蛋白鉴定数量差异和蛋白定量相关系数中一种或多种参数;
47.所述判断模块,还按照如下原则判断:
48.⑤
蛋白鉴定数量差异和/或总离子色谱图峰面积差异小于预设阈值;和/或蛋白定量相关系数大于预设阈值,则判断第5项评估指标通过评估,反之,则未通过;
49.所述蛋白鉴定数量差异的预设阈值在5%至40%取值;所述总离子色谱图峰面积差异的预设阈值在5%至40%取值;所述蛋白定量相关系数的预设阈值在0.6至0.95取值。
50.优选地,所述免疫沉淀实验效果评估系统,其所述评估结果显示模块,在设置对照组情况下,显示结果还包括如下:
51.第3项评估指标若未通过,显示免疫沉淀实验亲和富集效率达标,若未通过,显示免疫沉淀亲和富集效率不足;
52.第4项评估指标若通过,显示免疫沉淀实验亲和富集特异性达标,若未通过,显示免疫沉淀实验亲和富集特异性不足;
53.第5项评估指标若通过,显示对照组实验设置合理,若未通过,显示对照组实验设置不合理;
54.若免疫沉淀实验所得样本量、亲和富集效率、亲和富集特异性和对照组设置合理性均达标,评估结果为免疫沉淀实验效果理想,若对应评估指标未通过,判断免疫沉淀实验在对应方面存在缺陷,需要改进。
55.总体而言,通过本发明所构思的以上技术方案与现有技术相比,由于基于质谱法检测获得的解析质谱图谱数据与免疫沉淀实验结果的关联性评估免疫沉淀实验效果,能够取得下列有益效果:
56.本发明提供的基于质谱法评估免疫沉淀实验效果的方法,依据质谱检测获得的质谱图谱解析数据,按照相关评估原则进行评估,可以快速评估免疫沉淀实验效果,能够实现快速、准确定量的评估免疫沉淀实验效果,而且该方法可标准化。
附图说明
57.图1是基于质谱法的免疫沉淀效果评估流程图;
58.图2是实施例1中免疫沉淀实验的免疫印迹验证结果;
59.图3是实施例2中免疫沉淀实验获得的样品的质谱定量结果展示图;
60.图4是实施例3中免疫沉淀实验样品的质谱定量结果展示图。
具体实施方式
61.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于
限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
62.术语:
[0063]“免疫沉淀”是利用抗体特异性反应纯化富集目的蛋白的一种方法,其与“ip”、“co-ip”、“免疫共沉淀”、“immunoprecipitation”、“co-immunoprecipitation”可互换使用。
[0064]“免疫沉淀蛋白”指免疫沉淀实验后富集得到的蛋白,通常包括靶标诱饵蛋白和非特异性富集及清洗残留的背景蛋白。其中免疫沉淀实验的蛋白可来源于各种生物系统,包括但不限于各种动植物细胞模型、动植物组织、细菌、真菌,只要这些生物系统中包含免疫沉淀实验需富集的靶标诱饵蛋白即为本发明所述的免疫沉淀蛋白。
[0065]
免疫沉淀中使用的“抗体”以最宽的含义使用且包括各种抗体结构,包括但不限于单克隆抗体、多克隆抗体、多特异性抗体(诸如双特异性抗体)和抗体片段,只要它们表现出期望的免疫沉淀活性。
[0066]
免疫沉淀中使用的“微珠”以最宽的含义使用且包含各种类型和命名方式,包括但不限于beads、琼脂糖微珠、磁性微珠、琼脂糖珠、磁珠、magnetic beads、dynabeads、agarose beads和sepharose beads,只要它们表现出期望的抗体结合能力。
[0067]
现有的免疫沉淀实验效果评估最常用的方法是免疫印迹,该方法包括凝胶电泳、转膜、封闭、一抗孵育、二抗孵育、以及显影等步骤,操作繁琐、实验验证周期长达2天,且该方法仅能评估特定分子量蛋白,容易受抗体本身性质和生产质量的影响,也只能粗略定量评估,准确性较差,而且无法整体评估样品中的蛋白情况,也无法对样品用量和不同样品间的整体差异进行评估,难以评估样品用量和对照组设置情况。
[0068]
质谱法是一种基于肽段离子质核比(m/z)分析蛋白的方法,其操作简便、可自动化分析,能够实现标准化操作,质谱检测可以基于蛋白的氨基酸序列对蛋白进行鉴定,不会受分子量相近的其他蛋白的干扰,而且质谱法检测不依赖于抗体,检测结果不受限于抗体本身的性质和生产质量的影响,但质谱检测可以获得大量不同类型的分析数据,目前不明确这些质谱数据能否用于评估以及该如何来评估免疫沉淀实验效果,而我们通过实验发现质谱数据中的部分数据可以用于评估免疫沉淀实验效果,并建立了一种基于质谱法评估免疫沉淀实验效果的方法。
[0069]
本发明提供了一种基于质谱法评估免疫沉淀实验效果的方法,包括以下步骤:
[0070]
(1)免疫沉淀蛋白预处理:将免疫沉淀实验获得的免疫沉淀蛋白,经预处理后获得可供质谱直接检测的肽段和/或蛋白样品;
[0071]
所述免疫沉淀蛋白,包括但不限于微珠-蛋白混合物、蛋白沉淀、蛋白溶液和蛋白胶条,只要这些蛋白是来源于免疫沉淀实验的蛋白样品,含有抗体亲和富集获得的蛋白成分;
[0072]
所述预处理,包括且不限于清洗液清洗、蛋白酶酶解和脱盐处理;只要经过预处理,能够将不同形式蛋白样品转化为可供质谱直接检测的肽段或蛋白样品,可采用多种方式对免疫沉淀蛋白样品进行预处理;
[0073]
(2)质谱检测:将步骤(1)获得的肽段和/或蛋白样品进行质谱检测,获取质谱图谱的原始数据;搜库解析图谱原始数据,获得肽段和/或蛋白鉴定和定量数据;所述数据包括
第1项评估指标样品中总蛋白鉴定和定量情况以及第2项评估指标诱饵蛋白定量数据在总蛋白定量列表中的排名,简称“诱饵蛋白定量排名”;
[0074]
所述获得肽段和/或蛋白鉴定和定量数据,采用质谱定量方法获得相关数据;
[0075]
所述质谱定量方法,包括但不限于非标记定量、dia定量、tmt稳定同位素标记定量和silac标记定量,只要能够基于质谱检测获得肽段和蛋白的鉴定和定量信息即可;
[0076]
所述质谱检测,使用的质谱仪器包括但不限于maldi-tof、q-tof、obitrap、timstof以及包含这些质谱仪器的液质联用系统(lc-ms/ms)。
[0077]
(3)依据步骤(2)获得的评估指标数据,按照如下评估原则进行评估:
[0078]
样品中总蛋白鉴定和定量情况越好,判断免疫沉淀实验样本量越多,效果越好;
[0079]
诱饵蛋白的定量数据在所有蛋白定量数值中排名越高,判断免疫沉淀实验亲和富集效率和特异性越好。
[0080]
所述样品中总蛋白鉴定和定量情况,采用参数包括蛋白鉴定数量、肽段鉴定数量、样品检测总信号值、总离子色谱图峰面积中一种或多种组合;所述诱饵蛋白定量数据在总蛋白定量列表中的排名,采用参数包括ibaq、lfq intensity、intensity、谱图数、nsaf、saf中一种或多种组合;具体按照如下评估原则进行评估:
[0081]
①
蛋白鉴定数量和/或总离子色谱图峰面积大于预设阈值,则判断第1项评估指标通过评估,反之,则未通过;
[0082]
所述蛋白鉴定数量预设阈值在300至1500间取值,所述总离子色谱图峰面积预设阈值在2e8至1e10间取值;
[0083]
优选地,所述基于质谱法评估免疫沉淀实验效果的方法,针对模式物种和人源组织、细胞体系下的免疫沉淀实验,其所述蛋白鉴定数量预设阈值取值500;以thermo公司系列高分辨质谱仪进行质谱检测,其所述总离子色谱图峰面积预设阈值设置为5e8;
[0084]
②
诱饵蛋白的定量数据在所有蛋白定量数据中的排名低于预设阈值,则判断第2项评估指标通过评估,反之,则未通过;所述诱饵蛋白的定量数据在所有蛋白定量数据中的排名的预设阈值在3%至10%取值;
[0085]
优选地,所述基于质谱法评估免疫沉淀实验效果的方法,其所述诱饵蛋白的定量数据在所有蛋白定量数据中的排名的预设阈值设置为5%;
[0086]
上述两项评估指标均通过,则判断免疫沉淀实验成功;若第1项评估指标未通过,则判断免疫沉淀实验样本量不足;若第2项评估指标未通过,则判断免疫沉淀实验亲和富集效率不足。
[0087]
优选地,所述基于质谱法评估免疫沉淀实验效果的方法,其在设置对照组的情况下,所述数据,还包括第3项评估指标诱饵蛋白定量数据在免疫沉淀实验组样品与对照组样品中的差异以及第4项评估指标诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名,并按照如下评估原则进行评估:
[0088]
诱饵蛋白在实验组与对照组间的定量差异越显著,判断免疫沉淀实验亲和富集效率越高;
[0089]
诱饵蛋白在免疫沉淀实验组与对照组间的差异程度排名越高,判断免疫沉淀实验亲和富集特异性越好。
[0090]
所述第3项评估指标和第4项评估指标,具体按照如下评估原则进行评估:
[0091]
③
所述诱饵蛋白在实验组与对照组间的定量差异倍数高于预设阈值、定量差异显著性p值或p值校正值低于预设阈值,则判断第3项评估指标通过,反之,则未通过,若第3项评估指标未通过,则判断免疫沉淀实验亲和富集效率不足;
[0092]
所述诱饵蛋白在实验组与对照组间的定量差异倍数的预设阈值在2至10取值;所述定量差异显著性p值或p值校正值的预设阈值为0.01或0.05;
[0093]
优选地,所述定量差异倍数预设阈值设置为4;所述定量差异显著性p值和p值校正值预设阈值设置为0.05;
[0094]
④
诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名小于预设阈值,则判断通过第4项评估指标,反之,则未通过,若第4项评估指标未通过,则判断免疫沉淀实验亲和富集特异性不足;所述诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名的预设阈值在1%至3%,或3至10间取值。
[0095]
优选地,所述诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名的预设阈值设置为5。
[0096]
所述基于质谱法评估免疫沉淀实验效果的方法,其在设置对照组的情况下,所述数据,还包括第5项评估指标免疫沉淀实验组样品和对照组样品中总蛋白鉴定和定量差异,按照如下原则进行评估:
[0097]
实验组与对照组整体定量差异越小,判断对照组设置合理性越好。
[0098]
所述第5项评估指标,具体按照如下原则进行评估:
[0099]
⑤
蛋白鉴定数量差异和/或总离子色谱图峰面积差异小于预设阈值,和/或蛋白定量相关系数大于预设阈值,则判断第5项评估指标通过,反之,则未通过;若第5项评估指标通过,判断对照组实验设置合理;
[0100]
所述蛋白鉴定数量差异的预设阈值在5%至40%取值;所述总离子色谱图峰面积差异的预设阈值在5%至40%取值;所述蛋白定量相关系数的预设阈值在0.6至0.95取值。
[0101]
优选地,所述蛋白鉴定数量差异的预设阈值为20%;所述总离子色谱图峰面积差异的预设阈值为20%;所述蛋白定量相关系数的预设阈值为0.8。
[0102]
上述5项评估指标中:
[0103]
第1项样品中总蛋白鉴定和定量情况,用于评估免疫沉淀实验所得样本总蛋白量是否足够,第1项通过评估,判断免疫沉淀实验所得样本总蛋白量足够,反之,则判断免疫沉淀实验所得样本总蛋白量不足;
[0104]
第2项,诱饵蛋白定量数据在总蛋白定量列表中的排名,用于评估免疫沉淀实验的亲和富集效率和特异性;若第2项通过评估,判断免疫沉淀实验的亲和富集效率和特异性达标,反之,则不达标;
[0105]
第3项诱饵蛋白定量数据在免疫沉淀实验组样品与对照组样品中的差异,用于评估免疫沉淀实验的亲和富集效率;若第3项通过评估,则判断免疫沉淀实验的亲和富集效率达标,反之,则不达标;
[0106]
第4项诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名,用于评估免疫沉淀实验亲和富集的特异性;若第4项通过评估,则判断免疫沉淀实验亲和富集的特异性达标,反之,则不达标;
[0107]
第5项,诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名、免疫沉淀实
验组样品和对照组样品中总蛋白鉴定和定量差异,用于评估对照组实验设置的合理性;若第5项通过评估,则判断对照组实验设置合理,反之,则不合理。
[0108]
其中在未设置对照组的免疫沉淀实验中仅能进行第1项和第2项评估;
[0109]
在设置对照组情况,免疫沉淀实验的亲和富集效率的评估,以第3项评估结果为准;免疫沉淀实验亲和富集特异性的评估,以第4项评估结果为准;
[0110]
若免疫沉淀实验所得样本量、亲和富集效率、亲和富集特异性、对照组设置合理性均评估通过,判断免疫沉淀实验效果理想;若对应评估指标未通过,判断免疫沉淀实验在对应方面存在欠缺,建议改进优化。
[0111]
另一方面,本发明还提供了一种免疫沉淀实验效果评估系统,所述评估系统,包括数据获取模块、判断模块和评估结果显示模块;
[0112]
所述数据获取模块,用于获取待评估免疫沉淀蛋白的肽段和/或蛋白鉴定和定量数据,所述蛋白鉴定和定量数据,包括蛋白鉴定数量、肽段鉴定数量、样品检测总信号值和总离子色谱图峰面积中一种或多种组合参数;ibaq、lfq intensity、intensity、谱图数、nsaf、saf中一种或多种组合参数;并将数据传输给判断模块;
[0113]
所述判断模块,用于依据接收的数据,按照如下原则进行判断:
[0114]
①
蛋白鉴定数量和/或总离子色谱图峰面积大于预设阈值,则判断第1项评估指标通过评估,反之,则未通过;所述蛋白鉴定数量预设阈值在300至1500间取值;所述总离子色谱图峰面积预设阈值在2e8至1e10间取值;
[0115]
②
诱饵蛋白的定量数据在所有蛋白定量数据中的排名低于预设阈值,则判断第2项评估指标通过评估,反之,则未通过;所述诱饵蛋白的定量数据在所有蛋白定量数据中的排名的预设阈值在3%至10%取值;并将判断结果提交给评估结果显示模块;
[0116]
所述评估结果显示模块,用于依据判断结果进行显示,具体如下:
[0117]
在没有设置对照组情况下:
[0118]
第1项评估指标若通过,显示免疫沉淀实验样本量达标,若未通过,显示免疫沉淀实验样本量不足;
[0119]
第2项评估指标若通过,显示免疫沉淀实验亲和富集效率达标,若未通过,显示免疫沉淀实验亲和富集效率不足;
[0120]
若免疫沉淀实验样本量和免疫沉淀实验亲和富集效率均达标,说明免疫沉淀实验成功,若对应评估指标未通过,说明免疫沉淀实验在对应方面存在缺陷,需要改进。
[0121]
所述数据获取模块,在设置对照组实验的情况下,还用于获取定量差异倍数、定量差异显著性p值、定量差异显著性p值校正值中一种或多种组合参数;诱饵蛋白定量差异排名;
[0122]
所述判断模块,还按照如下原则判断:
[0123]
③
所述诱饵蛋白在实验组与对照组间的定量差异倍数高于预设阈值、定量差异显著性p值或p值校正值低于预设阈值,则判断第3项评估指标通过,反之,则未通过,若第3项评估指标未通过,则判断免疫沉淀实验亲和富集效率不足;所述诱饵蛋白在实验组与对照组间的定量差异倍数的预设阈值在2至10取值;所述定量差异显著性p值或p值校正值的预设阈值为0.01或0.05;
[0124]
④
诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名小于预设阈值,则
判断通过第4项评估指标,反之,则未通过,若第4项评估指标未通过,则判断免疫沉淀实验亲和富集特异性不足;所述诱饵蛋白在免疫沉淀实验组与对照组样品间差异程度的排名的预设阈值在1%至3%,或3至10间取值;
[0125]
更优选,还用于获取蛋白鉴定数量差异和蛋白定量相关系数中一种或多种参数;
[0126]
所述判断模块,还按照如下原则判断:
[0127]
⑤
蛋白鉴定数量差异和/或总离子色谱图峰面积差异小于预设阈值;和/或蛋白定量相关系数大于预设阈值,则判断第5项评估指标通过评估,反之,则未通过;
[0128]
所述蛋白鉴定数量差异的预设阈值在5%至40%取值;所述总离子色谱图峰面积差异的预设阈值在5%至40%取值;所述蛋白定量相关系数的预设阈值在0.6至0.95取值。
[0129]
所述评估结果显示模块,在设置对照组情况下,显示结果还包括如下:
[0130]
第3项评估指标若未通过,显示免疫沉淀实验亲和富集效率达标,若未通过,显示免疫沉淀亲和富集效率不足;
[0131]
第4项评估指标若通过,显示免疫沉淀实验亲和富集特异性达标,若未通过,显示免疫沉淀实验亲和富集特异性不足;
[0132]
第5项评估指标若通过,显示对照组实验设置合理,若未通过,显示对照组实验设置不合理;
[0133]
若免疫沉淀实验所得样本量、亲和富集效率、亲和富集特异性和对照组设置合理性均达标,说明免疫沉淀实验效果理想,若对应评估指标未通过,说明免疫沉淀实验在对应方面存在缺陷,需要改进。
[0134]
以下为实施例:
[0135]
实施例1未设置对照实验的免疫沉淀效果评估
[0136]
本实施例为thp-1细胞中针对tbk1蛋白的免疫沉淀实验进行评估,操作流程如图1所示,具体包括以下步骤:
[0137]
(1)获取免疫沉淀实验后包含磁性微珠和亲和富集蛋白的混合沉淀,预处理如下:
[0138]
混合沉淀以200μl清洗液(150mm nacl,50mm tris-hcl,ph 7.5)清洗3次;
[0139]
以100μl酶解反应液(150mm nacl,50mm tris-hcl,ph 7.5,10mm dtt,5ng/μltrypsin,2m urea)37℃孵育混合沉淀30min;
[0140]
向上述混合溶液中加入碘乙酰胺至终浓度50mm,暗室37℃震荡孵育过夜;
[0141]
磁力架分离沉淀和溶液,取上清,加入三氟乙酸至终浓度0.5%,终止酶解反应;
[0142]
以ziptip c18脱盐柱对上述溶液进行脱盐,真空旋干仪抽干后以0.1%甲酸溶液复溶上述肽段样品,以easy-nlc 1200高效液相色谱与q exactive hf质谱仪串联的液质联用系统进行检测,获取质谱图;
[0143]
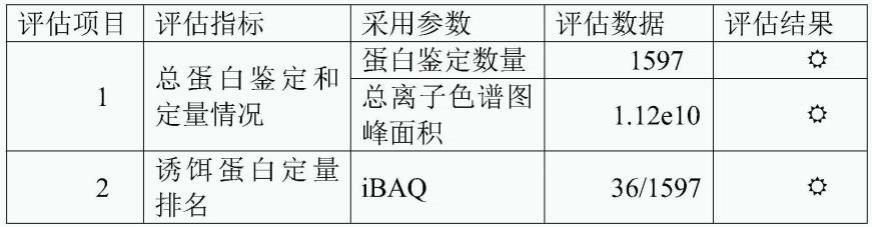
(2)质谱检测获得的谱图原始数据以maxquant软件进行搜库解析,获得蛋白和肽段定量信息,用于评估免疫沉淀实验效果,本实施例为未设置对照组的免疫沉淀实验,仅能进行第1项和第2项指标的评估,按照评估指标评估原则,免疫沉淀效果评估结果如下:
[0144][0145]
表中判断“通过评估”,表中判断“未通过评估”,下同。
[0146]
上表中的结果,具体评估如下:
[0147]
第1项评估指标采用参数为蛋白鉴定数据和总离子色谱图峰面积,其中蛋白鉴定数量的评估数据为1597,1597>500,总离子色谱图峰面积的评估数据为1.12e10,1.12e10>5e8,则判断第1项评估指标通过,判断该次免疫沉淀实验样本量达标;
[0148]
第2项评估指标采用参数为ibaq,ibaq的评估数据为36/1597,排名2.25%,排名在前5%内,则第2项评估指标评估通过,判断亲和富集特异性和富集效率达标;
[0149]
在未设置对照组免疫沉淀实验条件下,上述两项评估指标均通过评估,判断该免疫沉淀实验成功;另外,免疫印迹的验证如图2所示,也证实了采用本评估方法评估免疫沉淀实验效果的有效性。
[0150]
实施例2设置对照组实验的免疫沉淀效果评估
[0151]
本实施例评估hek293细胞中针对cchfv病毒flag标签np蛋白的免疫沉淀实验,以空白对照igg与hek293细胞进行免疫沉淀实验作为对照组,实验组和对照组免疫沉淀实验均进行3次重复,具体包括如下步骤:
[0152]
(1)获取免疫沉淀实验后的包含磁性微珠和亲和富集蛋白的混合沉淀,预处理如下:
[0153]
混合沉淀以200μl pbs溶液(150mm nacl,50mm tris-hcl,ph 7.5)清洗3次;
[0154]
以50μl反应液(1%sdc/100mm tris-hcl,ph 8.5/10mm tcep/40mm caa)95℃孵育混合沉淀10min;
[0155]
磁力架分离沉淀和溶液,取上清,加入等体积水,冷却至室温后加入1μg胰酶,37℃震荡孵育过夜;
[0156]
以含有sdb填料的微量层析柱对上述溶液进行脱盐,真空旋干仪抽干后-80℃保存待用;
[0157]
以0.1%甲酸溶液复溶上述肽段样品,以easy-nlc 1200高效液相色谱与q exactive hf质谱仪串联的液质联用系统进行检测,获取质谱图;
[0158]
(2)将步骤(1)质谱检测获得的谱图原始数据以maxquant软件进行搜库解析,获得蛋白和肽段定量信息,本实施例共评估5项指标,按照评估指标评估原则,免疫沉淀效果评估结果如下:
[0159][0160][0161]
本实施例共评估5项指标,其中第1项评估指标,采用参数为蛋白鉴定数量,评估数据为1558>500,则第1项评估指标通过,判断该次免疫沉淀实验样本量达标;
[0162]
第2项评估指标,采用参数为lfq intensity,评估数据为592/1558,排名37.99%,大于5%,即诱饵蛋白定量排名不在前5%,则第2项未通过评估,判断亲和富集特异性和富集效率不达标;
[0163]
第3项评估指标,采用参数为定量差异倍数和定量差异显著性p值,评估数据中定量差异倍数为52.07,大于4;p值为0.000316,小于0.01,则第3项评估指标通过评估,判断免疫沉淀实验亲和富集效率达标;
[0164]
第4项评估指标,评估数据为诱饵蛋白定量差异排名第1,在排名前5内,则第4项评估指标通过评估,判断免疫沉淀实验亲和富集效率达标;
[0165]
第5项评估指标,采用参数为蛋白鉴定数量差异和蛋白定量相关系数,其中蛋白鉴定数量差异的评估数据cv=8.34%,小于20%,各样品两两之间的蛋白定量相关系数的评估数据为分布在0.846-0.924,均大于0.8,则第5项评估指标通过评估,判断对照组实验设置的合理。
[0166]
第3、4项评估指标的评估结果优先级高于第2项,即在第2项评估结果与第3项评估结果和第4项评估指标相悖时,以第3项和第4项评估结果为准;
[0167]
综上所述,上述5项评估指标中第1、3、4、5项指标均通过,判断该免疫沉淀实验样品蛋白量、亲和富集效率、亲和富集特异性和对照组设置合理性均达标,说明该免疫沉淀实验成功。
[0168]
本实施例检测的质谱定量数据展示如图3所示。图中每个点判断一个鉴定到的蛋白,点的横纵坐标分别从差异倍数和t检验差异显著性2方面展示蛋白在实验组和对照组间的差异。越是接近右上角的点,其对应蛋白在实验组中相比对照组富集程度越显著。该图判断在本次免疫沉淀实验中,诱饵蛋白np是富集效率和富集特异性最好的蛋白。
[0169]
实施例3未通过评估的免疫沉淀实验
[0170]
本实施例评估红曲酶菌中针对flag标签a0a507r1l7蛋白的免疫沉淀实验,以表达
空白flag标签的红曲酶菌进行免疫沉淀实验作为对照组。免疫沉淀实验后获得包含琼脂糖微珠和亲和富集蛋白的混合沉淀,通过以下步骤获得用于评估的质谱检测数据:
[0171]
1.混合沉淀以200μlpbs溶液(150mm nacl,50mm tris-hcl,ph 7.5)清洗3次;
[0172]
2.以50μl反应液(1%sdc/100mm tris-hcl,ph 8.5/10mm tcep/40mm caa)95℃孵育混合沉淀10min;
[0173]
3. 1000g离心分离沉淀和溶液,取上清,加入等体积水,冷却至室温后加入1μg胰酶,37℃震荡孵育过夜;
[0174]
4.以ziptip c18脱盐柱对上述溶液进行脱盐,真空旋干仪抽干后-80℃保存待用;
[0175]
5.以0.1%甲酸溶液复溶上述肽段样品,以easy-nlc 1200高效液相色谱与q exactive plus质谱仪串联的液质联用系统进行检测;
[0176]
6.质谱检测获得的谱图原始数据以maxquant软件进行搜库解析,获得蛋白和肽段定量信息。
[0177]
获得基于质谱法的蛋白和肽段定量数据后,免疫沉淀效果评估结果如下:
[0178][0179][0180]
本实施例进行了5项指标的评估,每项指标选择一项参数。其中第2、3、4项评估均未通过,判断该免疫沉淀实验富集特异性和富集效率均较差,说明免疫沉淀实验不成功。
[0181]
图4展示本次免疫沉淀蛋白的质谱检测结果。图中每个点判断一个鉴定到的蛋白,横坐标和纵坐标分别通过实验组与对照组间的差异倍数和富集蛋白的信号强度展示免疫沉淀实验的亲和富集效率和特异性。本实验中未能鉴定到免疫沉淀的目标诱饵蛋白,判断亲和富集特异性和富集效率均较差,免疫沉淀实验不成功。
[0182]
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1